
【题目】某校化学课外兴趣小组的同学欲测定某品牌味精中食盐的含量。下面是该小组所进行的实验步骤:
①称取某品牌袋装味精样品10.0 g放入烧杯中,并加适量蒸馏水溶解;
②______________________________________;
③______________________________________;
④用蒸馏水洗涤沉淀2~3次;
⑤将沉淀烘干、称量,测得固体质量4.90 g。
根据上述实验步骤回答下列问题:
(1)请你在上面的空格内补齐所缺的实验步骤②、③。
(2)实验③所用的玻璃仪器有____________。
(3)检验沉淀是否洗净的方法是________________。
(4)若味精商标上标注:“谷氨酸钠含量≥80.0%,NaCl含量≤20.0%”,则此样品是否合格?________(填“合格”或“不合格”)。
【答案】加入硝酸酸化的硝酸银溶液于样品溶液中,直到不再产生沉淀为止 过滤 漏斗、玻璃棒、烧杯 取少量最后一次洗涤液于试管中,加入稀盐酸,若无浑浊现象,说明沉淀已洗净 合格
【解析】
(1)测定味精中食盐含量操作顺序:称取样品溶解,加入硝酸酸化的硝酸银溶液至不再产生沉淀,过滤后洗涤、烘干、称量,测得沉淀固体质量。
(2)过滤用到的玻璃仪器有漏斗、玻璃棒、烧杯。
(3)检验沉淀是否洗净的方法是:取少量最后一次洗涤液于试管中,加入稀盐酸,若无浑浊现象,说明沉淀已洗净。
(4)要测定食盐的含量,必须根据Cl-的量进行计算。
(1)测定味精中食盐含量操作顺序:称取样品溶解,加入硝酸酸化的硝酸银溶液至不再产生沉淀,过滤后洗涤、烘干、称量,测得沉淀固体质量,故答案为:加入硝酸酸化的硝酸银溶液于样品溶液中,直到不再产生沉淀为止 ;过滤 ;
(2)实验③是过滤操作,所用的玻璃仪器有:漏斗、玻璃棒、烧杯,故答案为:漏斗、玻璃棒、烧杯;
(3)检验沉淀是否洗净的方法是:取少量最后一次洗涤液于试管中,加入稀盐酸,若无浑浊现象,说明沉淀已洗净 ;故答案为:取少量最后一次洗涤液于试管中,加入稀盐酸,若无浑浊现象,说明沉淀已洗净 ;
(4)当得沉淀AgCl的质量为4.90 g时,含Cl-的质量为![]() ×4.90 g≈1.21 g,则NaCl的质量为
×4.90 g≈1.21 g,则NaCl的质量为![]() ×58.5 g≈1.99 g,则食盐的含量为
×58.5 g≈1.99 g,则食盐的含量为![]() ×100%=19.9%<20.0%,样品合格,故答案为:合格。
×100%=19.9%<20.0%,样品合格,故答案为:合格。


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】在正规化学试卷的开始处总有“可能用到的相对原子质量”一项,如H:1 C:12 Cl:35.5 S:32 Cu:64等.请问这些数值准确的说法应该是( )
A.某种核素的相对原子质量
B.某种核素的近似相对原子质量
C.某种元素的平均相对原子质量
D.某种元素的平均相对原子质量的近似值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学过程对应的方程式表示正确的是 ( )
A. 碳酸氢钠溶液的水解:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B. 醋酸的电离:CH3COOH=CH3COO-+H+
C. 碳酸钙的溶解平衡CaCO3(s) ![]() Ca2+(aq)+CO32-(aq)
Ca2+(aq)+CO32-(aq)
D. 硫化钠溶液呈碱性的原因:S2-+H2O![]() H2S+2OH-
H2S+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C5H10O3的有机物,一定条件下具有如下性质:
①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应②在浓硫酸存在下,能脱水生成两种结构不同的能使溴水褪色的物质③在浓硫酸存在下,能生成一种分子式为C5H8O2的五元环状化合物,则C5H10O3的结构简式为( )
(已知:![]() )
)
A. HOCH2COOCH2CH2CH3 B. CH3CH(OH)CH2CH2COOH
C. CH3CH(OH)CH(CH3)COOH D. HOCH2CH2CHCH2COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R 为周期表前四周期原子序数依次增大的五种元素,X 与其他四种元素不同周期不同主族,M原子最外层2p轨道上有两个未成对电子,Y 易与M形成两种常见的化合物,R 在周期表的第9列。回答下列问题:
(1)R 基态原子M 能层的电子排布式为_________________,其原子核外共有_________种能量的电子。
(2)Y、M均可与X形成18e-的分子,其中属于极性分子的为_____________(填化学式),分子中Y、M 两种原子杂化方式依次为___________、_________________。
(3)Z 与M可形成的两种常见酸根离子的几何构型为__________、____________。
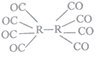
(4)R可形成原子簇化合物R2(CO)8,其沸点为52℃,不溶于水,易溶于乙醇、苯、二硫化碳等,是一种重要的有机合成催化剂,其结构如图,则该化合物属于_________晶体,该晶体中存在的作用力有___________(填标号)。
a.离子键 b.配位键 Cσ键 d.π键 e.氢键 f.范德华力
(5)单质R的晶胞有两种:417℃以下的晶胞结构如图1,417℃以上的晶胞结构如图2,后者配位数是_____________。若前者晶胞参数为ɑpm和c pm,单质R的摩尔质量为Mg·mol-1,阿伏加德罗常数为NA,则前者晶体密度p=_________g·cm-3(列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组对某葡萄酒中SO2的含量进行检测,按下图连接好仪器。回答下列问题:

Ⅰ.样品蒸馏
取20.00mL样品和250 mL水置于仪器A中,仪器B是去掉塞子的碘量瓶,向其中装人25mL 乙酸铅溶液,然后向仪器A中加入10 mL盐酸,立即盖塞蒸馏;当碘量瓶中的液体约200 mL时,将插入碘量瓶液面下的导管向上提起并将导管置于液面上方1cm 处,再蒸馏2min左右;最后用少量蒸馏水冲洗碘量瓶中的导管,并将冲洗液并入碘量瓶中。同时做空白实验(即不加样品情况下按同法操作,防止实验误差)。
已知:SO2+H2O+Pb(CH3COO)2=PbSO3↓+2CH3COOH。
(1)仪器A 的名称是_________________ 。
(2)实验中使用的碘量瓶最适宜的规格是_________ (填标号)。
a.100 mL b.250 mL c.500 mL d.1000 mL
(3)如果实验最后未用少量蒸馏水冲洗碘量瓶中的导管,会导致测定结果__________(填“偏高”“ 偏低”或“不影响”)。
Ⅱ.滴定操作
向取下的碘量瓶中加入10 mL盐酸和1mL淀粉溶液,摇匀后用0.01mol·L-1的碘标准溶液滴定,记录消耗的碘标准溶液的体积为V( 单位为mL)。
(4)滴定终点的现象是_____________________,该滴定反应的离子方程式是______________。
Ⅲ.结果分析
(5)甲组4 次实验测得V分别为
实验 | 1 | 2 | 3 | 4 |
V/mL | 9.98 | 12.00 | 10.02 | 10.00 |
据此可计算此葡萄酒中SO2的含量为_______mg·L-1
乙组认为甲组实验不严谨,可能会有误差,因为甲组未做_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年我国通过蛟龙一号在东海试采可燃冰成功,可燃冰的主要成分是甲烷。下列说法不正确的是( )
A.甲烷属于烃类B.甲烷是天然气的主要成分
C.甲烷能发生取代反应D.甲烷能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以酸性氢氧燃料电池为电源进行电解的实验装置如图所示。下列说法正确的是( )
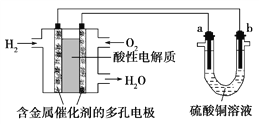
A. 燃料电池工作时,正极反应为O2+2H2O+4e-===4OH-
B. a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
C. 电解过程中SO42— 移向b极
D. a、b两极若是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中的一些问题常涉及化学知识,下列叙述正确的是
A.棉花的主要成分是纤维素
B.过多食用糖类物质如淀粉等不会致人发胖
C.淀粉在人体内直接水解生成氨基酸,供人体组织的营养需要
D.纤维素在人体消化过程中起重要作用,纤维素可以作为人类的营养物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com