
| A��NH4NO3��Һ�����Ե�ԭ��NH4++H2O=NH3?H2O+H+ |
| B����ͭ����ʱ�����Դ�����������Ǵ�ͭ���缫��ӦʽΪ��Cu-2e-=Cu2+ |
| C������������Һ�еμ�����Ba��OH��2��Һ�����ӷ���ʽ��2H++SO42-+Ba2++2OH-=2H2O+BaSO4�� |
D��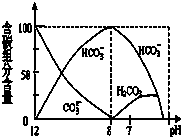 ��ͼ����0.1 mol?L-1Na2CO3��Һ����μ���0.1 mol?L-1 HCl���� pH=7ʱ�����ӷ���ʽ��H++HCO3-=CO2��+H2O |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ�����Ҵ����ױ����屽 |
| B����ȼ�շ������Ҵ����������Ȼ�̼ |
| C����̼������Һ�����Ҵ���������������� |
| D����ά���������ڿ�ˮ��Ϊ�����ǣ��ʿ��������Ӫ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c��NH4+����c��Cl-����c��OH-����c��H+�� |
| B��c��NH4+��=c��Cl-����c��OH-��=c��H+�� |
| C��c��Cl-����c��NH4+����c��OH-����c��H+�� |
| D��c��Cl-����c��NH4+����c��H+����c��NH4+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ԭ������A��B |
| B����������A��B |
| C�����Ӱ뾶A-��B2+ |
| D��ԭ�Ӱ뾶A��B |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| A��C3N3��OH��3��HNCOΪͬһ���� |
| B��HNCO��һ�ֺ�ǿ�������� |
| C��1 mol NO2�ڷ�Ӧ��ת�Ƶĵ���Ϊ24 mol |
| D����Ӧ��N2���������������ǻ�ԭ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
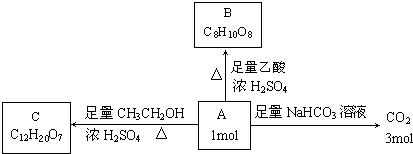
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com