
����Ŀ���Ժ��ܷϴ�������Ҫ�ɷ�ΪCo��Fe��SiO2��Ϊԭ�ϣ���ȡ�����ܵ��������£�
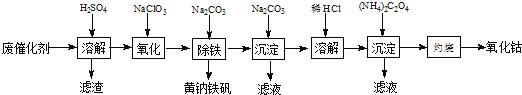
��1���ܽ⣺�ܽ����ˣ�������ϴ��2��3�Σ�ϴҺ����Һ�ϲ�����Ŀ����_________________��������������Ҫ�ɷ���_________��д��ѧʽ����
��2�����������Ƚ��������¼���NaClO3����Fe2+������Fe3+�������ӷ���ʽ_________________��
��֪�����軯�ػ�ѧʽΪK3[Fe(CN)6]�������軯�ػ�ѧʽΪK4[Fe��CN��6]3H2O��
3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2������ɫ������
4Fe3++3[Fe(CN)6]4-=Fe4[Fe(CN)6]3������ɫ������
ȷ��Fe2+�Ƿ�������ȫ�ķ�����______________�����ɹ�ѡ����Լ������軯����Һ�������軯����Һ�����ۡ�KSCN��Һ��
��3������������������Na2CO3������ȣ����ɻ�������[Na2Fe6(SO4)4(OH)12]������д���÷�Ӧ�Ļ�ѧ����ʽ______________��
��4�����������ɳ�����ʽ̼����[(CoCO3)23Co(OH)2]��������ϴ�ӣ�ϴ�ӵIJ�����______________��
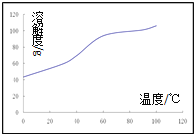
��5���ܽ⣺CoCl2���ܽ��������ͼ��ʾ���ʽ̼�����м�������ϡ���ᣬ���ȱ߽�������ȫ�ܽ������ȹ��ˣ���ԭ����______________��
��6�����գ�ȷ��ȡ����CoC2O41.470g���ڿ����г�����յ�0.830g�����ܣ�д�������ܵĻ�ѧʽ_________��
���𰸡�����ܵ�Ԫ�ص������� SiO2 6Fe2++6H++ClO3-�T6Fe3++Cl-+3H2O ȡ���������Һ�������Թ��У��μӼ������軯����Һ��������ɫ�������ɣ���Fe2+��ȫ���������� 3Fe2(SO4)3+6H2O+6Na2CO3=Na2Fe6(SO4)4(OH)12��+5Na2SO4+6CO2�� ��©���м�������ˮ����û����������ʹ��Һ�������ظ�����2��3�� ��ֹ���¶Ƚ��ͣ�CoCl2�������� Co2O3
��������
������ͼ��֪�����ܷϴ����м���ϡ���ᣬ�ܺ��������ᷴӦ����Ӧ�Ļ�ѧ����ʽΪCo+H2SO4=CoSO4+H2����Fe+H2SO4=FeSO4+H2��������������ϡ�����Ӧ�����ˣ������Dz��ܵĶ������裬����Һ�������ܡ��������������������Ļ����Һ������Һ�м��������ƣ������ƾ��������ԣ����������½��������������������ӣ���Ӧ����Һ�м���̼���ƣ�������ҺpHΪ2������Һ�е�������ת��Ϊ��������[Na2Fe6��SO4��4��OH��12]������ȥ�����ˣ�����Һ�м�������̼���ƣ�������ҺpHΪ7���õ�̼���ܳ��������ˣ��������ܽ�̼���ܳ���������������Һ�м������泥��õ������ܳ��������ˣ����ղ����ܳ����������ܳ����������������Ӧ���������ܣ��ݴ˷������
(1)ϴҺ����Һ�ϲ������ϴ�Ӻ���Һ���ܵ������ʣ���SiO2������ϡ���ᣬ����������Ҫ�ɷ���SiO2��
(2)�������ӱ���������������������ӣ�1molr����������ʧȥ1mol�ĵ��ӣ���1mol����������ӵõ�6mol�ĵ��ӣ����ݵ��ӵ�ʧ�غ㣬��֪���ӷ���ʽΪ��6Fe2++6H++ClO3-�T6Fe3++Cl-+3H2O��ȡ���������Һ�������Թ��У��μӼ������軯����Һ��������ɫ�������ɣ���Fe2+��ȫ����������
(3)������������̼���Ʒ���˫ˮ��õ�������������ѧ��Ӧ����ʽΪ��3Fe2(SO4)3+6H2O+6Na2CO3=Na2Fe6(SO4)4(OH)12��+5Na2SO4+6CO2����
(4)����ϴ�ӵķ�������©���м�������ˮ����û����������ʹ��Һ�������ظ�����2��3�Σ�(5)CoCl2���ܽ�����߿�֪�����¶ȵ����ߣ�CoCl2���ܽ���������Գ��ȹ��ˣ���ֹ�¶Ƚ����Ȼ���������
(6)CoC2O4������Ϊ1.470g������֪����Ϊ0.01mol��CoԪ������Ϊ0.59g��������������Ϊ0.83g������������Ԫ������Ϊ0.83g-0.59g=0.24g������������Coԭ����Oԭ�����ʵ���֮��Ϊ0.01mol��(0.24/16)��2��3����Co������ΪCo2O3��


 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�������A��B��C������ס��ҡ����Լ�����D��E��F��G��H������֮����ת����ϵ��ͼ��ʾ(ͼ����Щ��Ӧ��������ͷ�Ӧ������û�б��)����ʾ:�ƾvɫ��������������

��ش��������⣺
(1)д���������ʵĻ�ѧʽ��B______����______��H______��
(2)����Ҫ��ش�
��D��Һ��F��Һ�ڿ����л�ϵ�����_______��
�ڷ�Ӧ�����ӷ���ʽ________��
�۷�Ӧ�����ӷ���ʽ________��
�ܷ�Ӧ��ѧ����ʽ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£������������Ϊ 1.0 L �ĺ����ܱ������з�����Ӧ��2CH3OH(g)![]() CH3OCH3(g)��H2O(g)
CH3OCH3(g)��H2O(g)
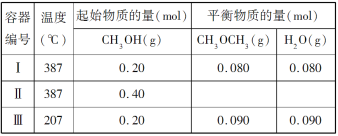
����˵����ȷ���ǣ� ��
A.�÷�Ӧ������ӦΪ���ȷ�Ӧ
B.�ﵽƽ��ʱ���������е� CH3OH ����������������е�С
C.�������з�Ӧ����ƽ������ʱ����������еij�
D.����ʼʱ���������г��� CH3OH 0.15 mol��CH3OCH3 0.15 mol �� H2O 0.10 mol����Ӧ�� ������Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£�������NO2��O2���Թܵ�����ˮ���У���ַ�Ӧ��ʣ����������Ϊԭ������������![]() ����ԭ���������NO2��O2�����֮����
����ԭ���������NO2��O2�����֮����
A.8��1B.7��3C.1��7D.4��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������ء�
I.K2Cr2O7�����ڼ��˾���Ƿ�ƺ��ʻ��Cr2O72-(��ɫ)+CH3CH2OH��Cr3+(��ɫ)+CH3COOH(δ��ƽ��
��1����̬Crԭ�ӵļ۵��ӹ������ʽΪ__��
��2��CH3COOH����������Ԫ�صĵ縺���ɴ�С��˳��Ϊ__��̼ԭ�ӵĹ���ӻ�����Ϊ__��������������������Ŀ֮��Ϊ__��
��3����֪Cr3+�ȹ���Ԫ��ˮ�����ӵ���ɫ�����ʾ��
���� | Sc3+ | Cr3+ | Fe2+ | Zn2+ |
ˮ�����ӵ���ɫ | ��ɫ | ��ɫ | dz��ɫ | ��ɫ |
�����ԭ�ӽṹ�Ʋ�Sc3+��Zn2+��ˮ������Ϊ��ɫ��ԭ��Ϊ__��
II.ZnCl2Ũ��Һ�����ڳ�ȥ��������������������FeO��Ӧ�ɵ�Fe[Zn(OH)Cl2]2��Һ��
��4��Fe[Zn(OH)Cl2]2��Һ�в����ڵ�������������__(��ѡ����ĸ)��
A.���Ӽ� B.���ۼ� C.������ D.��λ�� E.���»��� F.���
��Һ��[Zn(OH)Cl2]-�ĽṹʽΪ__��
III.п������������Ԫ��֮һ����ѻ���ʽ��ͼ1�������ṹ��ͼ2��
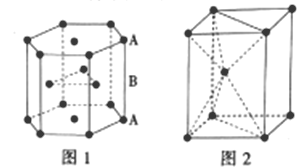
��5��п�Ķѻ���ʽΪ__����λ��Ϊ__��
��6����пԭ�ӵİ뾶Ϊapm�������ӵ�������ֵΪNA����п������ܶ�Ϊ___g/cm3(�ú�a�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ũҵ�����벻�����ʣ���ѧ����ʹ�õ��ʣ�����������ʵ�ʹ���ʣ������ܹ����õر�����������ش��������⣺
(1)��N2ת��Ϊ����������Ĺ��̳�Ϊ�̵�
�� �˹��̵�����N2��NH3�� N2����_________��Ӧ
�� ��Ȼ��̵����ɽ�����N2ת��ΪCa(NO3)2�ȵ��ʣ�ת��;������(ת�������Լ�����������ȥ)��N2��NO��NO2��HNO3![]() Ca(NO3)2��д��NO��NO2��HNO3�Ļ�ѧ����ʽ__________��__________����HNO3ת��ΪCa(NO3)2���о����ֲ�ͬ����Ļ�����M_______(д��ѧʽ)��
Ca(NO3)2��д��NO��NO2��HNO3�Ļ�ѧ����ʽ__________��__________����HNO3ת��ΪCa(NO3)2���о����ֲ�ͬ����Ļ�����M_______(д��ѧʽ)��
(2)��ѧ�����ر��桢ʩ�õ���
�� NH4HCO3�����������棬ԭ����__________(д��ѧ����ʽ)��
�� �̬���ʲ�������Է��ϻ��ʹ�ã���NH4ClΪ��д��������Ӧ�����ӷ���ʽ________��
(3)����ʩ�õ��ʽ����´�����NH3�������ߣ��Ӿ��������γɡ�(NH4)2SO4�������ijɷ�֮һ�����γɹ�������ͼ��ʾ(ת�������Լ�����������ȥ)��
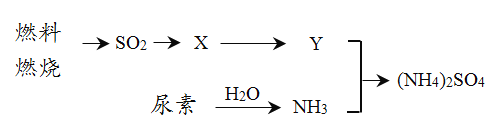
�� X������______��_______�� Y��___________��
�� ����CO(NH2)2��һ�ֳ��û��ʣ�������H2O������������ԭ��Ӧ�ͷų�NH3��������CԪ�ػ��ϼ�Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. �����ܽ�ˮ���е�CaCO3�� CaCO3 + 2H+= Ca2++ H2O + CO2��
B. ���Ե缫��ⱥ��MgCl2��Һ�� Mg2++2Cl�� + 2H2O ![]() Mg(OH)2�� + H2�� + Cl2��
Mg(OH)2�� + H2�� + Cl2��
C. ��������Һ��ͨ��������CO2��![]() +H2O+CO2��
+H2O+CO2�� +
+![]()
D. ��������Һ������ȩ�е�ȩ����CH3CHO��![]() ��2OH��
��2OH��![]() CH3COONH4��H2O��2Ag����3NH3��
CH3COONH4��H2O��2Ag����3NH3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£���224 L HCl��������635 mLˮ�У�����������ܶ�Ϊ1.18 g��cm��3���Լ��㣺
(1)����������������������ʵ���Ũ�ȷֱ���_______��_______��
(2)ȡ����������100 mL��ϡ����1.18 L������ϡ��������ʵ���Ũ����_______��
(3)��40.0 mL 0.065 mol��L��1Na2CO3��Һ�У�����(2)��ϡ�͵�ϡ���ᣬ�ӱ�����ʹ��Ӧ������CO2���壬����ϡ��������������_______mL��
(4)��������NaOH��Ʒ1 g(��Ʒ������Na2CO3��ˮ)������50 mL 2 mol��L��1�������У���ַ�Ӧ����Һ�����ԣ��кͶ����������ȥ40 mL 1 mol��L��1��NaOH��Һ�������кͺ����Һ�����յõ�_______�˹��塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ײʱ����ȫ�����з�����Ӧ��10NaN3+2KNO3��K2O+5Na2O+16N2��������������Ȼ�ԭ�����1.75mol���������жϲ���ȷ����
A. ����44.8L N2����״����
B. ��0.25 mol KNO3����ԭ
C. ת�Ƶ��ӵ����ʵ���Ϊ1.75mol
D. ��������Nԭ�ӵ����ʵ���Ϊ3.75mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com