
【题目】含氮化合物在生产、生命活动中有重要的作用。回答下列问题:
(1)已知4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H1=-alkJ/mol,4NH3(g)+6NO(g)=5N2(g)+6H2O(g)△H2=-bkJ/mol,H2O(1)=H2O(g)△H3=+ckJ/mol,写出在298K时,氨气燃烧生成N2的热化学方程式___________。
(2)肌肉中的肌红蛋白(Mb)可与O2结合生成MbO2:Mb(aq)+O2(g)![]() MbO2(aq),其中k正和k逆分别表示正反应和逆反应的速率常数,即V正=k正·c(Mb)·P(O2),V逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]:
MbO2(aq),其中k正和k逆分别表示正反应和逆反应的速率常数,即V正=k正·c(Mb)·P(O2),V逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]:
P(O2) | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
α(MbO2%) | 50.0 | 67.0 | 80.0 | 85.0 | 88.0 | 90.3 | 91.0 |
①计算37℃、P(O2)为2.00kPa时,上述反应的平衡常数K=___________。
②导出平衡时肌红蛋白与O2的结合度(α)与O2的压强[P(O2)]之间的关系式α=___________(用含有k正、k逆的式子表示)。
(3)构成肌红蛋白的甘氨酸(NH2CH2COOH)是一种两性物质,在溶液中以三种离子形式存在,其转化关系如下:
![]()
![]()
![]()
![]()
![]()
在甘氨酸溶液中加入酸或碱,三种离子的百分含量与的关系如图所示:
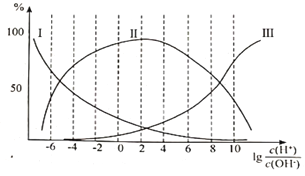
①纯甘氨酸溶液呈___________性;当溶液呈中性时三种离子的浓度由大到小的顺序为___________。
②向![]() =8的溶液中加入过量HCl时,反应的离子方程式为___________。
=8的溶液中加入过量HCl时,反应的离子方程式为___________。
③用电位滴定法可测定某甘氨酸样品的纯度.
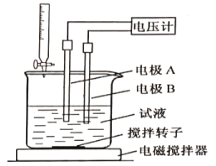
称取样品150mg,在一定条件下,用0.1000mol/L的高氯酸溶液滴定(与甘氨酸1︰1发生反应),测得电压变化与滴入HClO4溶液的体积关系如下图。做空白对照实验,消耗HClO4溶液的体积为0.25mL,该样品的纯度为___________%(计算结果保留一位小数)
【答案】4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H=![]() kJ/mol 2.00
kJ/mol 2.00 ![]() 酸 H3N+CH2COO->H2NCH2COO->H3N+CH2COOH H2NCH2COO-+2H+=H3N+CH2COOH 85.0
酸 H3N+CH2COO->H2NCH2COO->H3N+CH2COOH H2NCH2COO-+2H+=H3N+CH2COOH 85.0
【解析】
(1) 根据盖斯定律,将三个热化学方程式叠加,可得相应的热化学方程式;
(2)①根据平衡常数的含义,结合37℃、P(O2)为2.00kPa时a(MbO2)计算平衡常数;
②根据反应达到平衡时,V正=V逆,结合平衡常数定义式进行变性,可得表达式;
(3)①根据甘氨酸的存在形式与溶液酸碱性的关系,先判断I、II、III分别为H2NCH2COO-、H3N+CH2COO-和H3N+CH2COOH,若只含有H3N+CH2COO-,此时lg![]() ,结合溶液的Kw可判断溶液的pH、确定溶液的酸碱性;当溶液呈中性时,lg
,结合溶液的Kw可判断溶液的pH、确定溶液的酸碱性;当溶液呈中性时,lg![]() =0,根据图示判断微粒浓度大小;
=0,根据图示判断微粒浓度大小;
②根据lg![]() =8时,微粒存在有H2NCH2COO-、H3N+CH2COOH,盐酸过量,H2NCH2COO-反应变为H3N+CH2COOH,书写反应方程式;
=8时,微粒存在有H2NCH2COO-、H3N+CH2COOH,盐酸过量,H2NCH2COO-反应变为H3N+CH2COOH,书写反应方程式;
③结合滴定突跃时溶液体积读数与空白读数差,计算出消耗高氯酸的体积,利用n=cV计算出高氯酸的物质的量,根据恰好反应时甘氨酸与高氯酸的物质的量的比是1:1,计算出甘氨酸质量,利用甘氨酸质量与样品质量差计算得到甘氨酸的纯度。
(1) ①4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H1=-alkJ/mol,
②4NH3(g)+6NO(g)=5N2(g)+6H2O(g)△H2=-bkJ/mol,
③H2O(1)=H2O(g)△H3=+ckJ/mol,将①×3+②×2-③×30,整理可得热化学方程式:4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H=![]() kJ/mol;
kJ/mol;
(2)①37℃、P(O2)=2.00kPa时,结合度为80%,化学平均常数K=![]() kPa-1;
kPa-1;
②由结合度的定义式可知,反应达平衡时,V正=V逆,所以K=![]() ,可求出c(MbO2)=
,可求出c(MbO2)=![]() ,代入结合度定义式
,代入结合度定义式![]() =
=![]() 可得a=
可得a=![]() ;
;
①甘氨酸的三种存在形式:H3N+CH2COOH、H3N+CH2COO-和H2NCH2COO-应分别在强酸性至强碱性中存在,由此判断,图中I、II和III分别为H2NCHCOO-、H3N+CH2COO-和H3N+CH2COOH,当lg![]() =-8时,溶液显碱性,溶液中存在的主要是H2NCH2COO-,它与过量的HCl反应生成H3N+CH2COOH。由图可知纯甘氨酸溶液呈酸性(实际在5.9左右),溶液呈中性时,lg
=-8时,溶液显碱性,溶液中存在的主要是H2NCH2COO-,它与过量的HCl反应生成H3N+CH2COOH。由图可知纯甘氨酸溶液呈酸性(实际在5.9左右),溶液呈中性时,lg![]() =0,中性时H3N+CH2COO-> H2NCH2COO->H3N+CH2COOH;②根据lg
=0,中性时H3N+CH2COO-> H2NCH2COO->H3N+CH2COOH;②根据lg![]() =8时,微粒存在有H2NCH2COO-、H3N+CH2COOH,由于加入的盐酸过量,所以,发生反应H2NCH2COO-变为H3N+CH2COOH,反应方程式为H2NCH2COO-+2H+=H3N+CH2COOH;
=8时,微粒存在有H2NCH2COO-、H3N+CH2COOH,由于加入的盐酸过量,所以,发生反应H2NCH2COO-变为H3N+CH2COOH,反应方程式为H2NCH2COO-+2H+=H3N+CH2COOH;
根据滴定曲线的突跃范围,消耗HClO4溶液17.25mL,减去空白实验的0.25mL,实际消耗滴定液17.00mL。n(HClO4)= 0.1000mol/L×0.01700L=0.0017mol,则n(甘氨酸)=0.0017mol,甘氨酸的质量为m(甘氨酸)=0.0017mol×75g/mol=0.1275g,所以甘氨酸的纯度为:(0.1275g÷0.150g)×100%=85.0%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列各项叙述中,正确的是( )
A.Na、Mg、Al的未成对电子数依次增多
B.价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素
C.2p和3p轨道形状均为哑铃形,能量也相等
D.氮原子的最外层电子排布图:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应C(s)+CO2(g)![]() 2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:
2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:
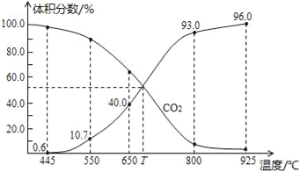
已知气体分压(P分)=气体总压(P总)×体积分数,下列说法不正确的是
A.550℃时,若充入惰性气体,v正,v逆均减小,平衡不移动
B.650℃时,反应达平衡后CO2的转化率为25.0%
C.T℃时,若充入等体积的CO2和CO,平衡向不移动
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=23.04P总
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于![]() 的说法正确的是
的说法正确的是
A. 所有原子可能都在同一平面上 B. 最多只可能有9个碳原子在同一平面
C. 有7个碳原子可能在同一直线 D. 只可能有5个碳原子在同一直线
查看答案和解析>>
科目:高中化学 来源: 题型:
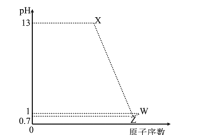
【题目】已知短周期元素M、N、P、Q最高价氧化物对应水化物分别为X、Y、Z、W,M是短周期中原子半径最大的元素,常温下X、Z、W均可与Y反应,M、P、Q的原子序数及0.1mol/LX、Z、W溶液的pH如图所示。下列说法正确的是( )
A.N原子的电子层数与最外层电子数相等
B.M的离子半径小于N的离子半径
C.P氢化物稳定性大于Q氢化物稳定性
D.X、W两物质含有的化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的数目是
①12.0g熔融的NaHSO4中含有的阳离子数为0.2NA
②1mol Na2O 和Na2O2混合物中含有的阴、阴离子总数是3NA
③常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
④7.8g![]() 中含有的碳碳双键数目为0.3NA
中含有的碳碳双键数目为0.3NA
⑤用1L1.0 mol/LFeCl3溶液制备氢氧化铁胶体,所得氢氧化铁胶粒的数目为NA
⑥1mol SO2与足量O2在一定条件下充分反应生成SO3,共转移2NA个电子
⑦在反应KIO3+6HI=KI+3I2 +3H2O 中,每生成3molI2转移的电子数为5NA
⑧常温常压下,17 g甲基(-14CH3)中所含的中子数为9NA
A. 3 B. 4 C. 5 D. 6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋(Bi)位于元素周期表中第ⅤA族,其价态为+3时较稳定,铋酸钠(NaBiO3)溶液呈无色。现取一定量的硫酸锰(MnSO4)溶液,向其中依次滴加下列溶液,对应的现象如表所示:

在上述实验条件下,下列结论正确的是
A.BiO3-的氧化性强于MnO4-
B.H2O2被高锰酸根离子还原成O2
C.H2O2具有氧化性,能把KI氧化成I2
D.在KI-淀粉溶液中滴加铋酸钠溶液,溶液一定变蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯(烧杯内有水)中:在(1)中加入CaO,在(2)中不加其他任何物质,在(3)中加入NH4Cl晶体,发现(1)中红棕色变深,(3)中红棕色变浅。[已知反应2NO2(红棕色) N2O4(无色)]

下列叙述正确的是( )
A.2NO2N2O4是放热反应
B.NH4Cl溶于水时放出热量
C.烧瓶(1)中平衡混合气体的平均相对分子质量增大
D.烧瓶(3)中气体的压强增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某烧碱样品的纯度(含有的少量可溶性杂质不与酸反应),某同学进行滴定实验。回答下列问题
(1)烧碱样品溶液的配制:用_____(填仪器名称,下同)准确称取烧碱样品wg,用新煮沸并冷却的蒸馏水在_____中溶解,完全溶解并冷却后,全部转移至250mL的_____中并定容。
(2)滴定:
Ⅰ.用移液管(或碱式滴定管)量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂;
Ⅱ.将物质的量浓度为mmolL﹣1的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1mL;
Ⅲ.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2mL
①锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去H2SO4标准溶液的体积_____(填“偏大”“偏小”或“无影响”)。
②步骤Ⅲ的操作中锥形瓶下垫一张白纸的作用是_____。
③步骤Ⅱ中液面应调整到_____,尖嘴部分应_____。
④若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响_____(填“偏高”“偏低”或“无影响”,其他操作均正确)。
(3)烧碱样品的纯度为_____(用含w、m、V1、V2的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com