
【题目】若阿伏加德罗常数为NA,下列说法正确的是( )
A.在60gSiO2中,含Si—O键的数目是2NA
B.32gN2H62+和C2H6的混合物中,共含有电子数为18NA
C.标准状况下,22.4L NO与11.2L O2混合物容器中共有NA个NO2分子
D.1L 0.1mol/L Na2SO4溶液中,含有的离子数不是3NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C![]() 2AlN+3CO.下列叙述正确的是( )
2AlN+3CO.下列叙述正确的是( )
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol电子
C.氮化铝中氮元素的化合价为﹣3
D.氮化铝晶体属于分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: 2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+ ![]() O2(g)△H=-226kJ/mol
O2(g)△H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
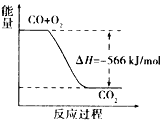
A. CO 的燃烧热为566kJ/mol
B. 上图可表示由CO生成CO2的反应过程和能量关系
C. 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) △H<-452 kJ/mol
D. CO2(g)与Na2O2(s)反应放出452kJ 热量时,电子转移数为1.204×1024 (个)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铍铜是力学、化学综合性能良好的合金,广泛应用于制造高级弹性元件。以下是从某废旧铍铜元件(含BeO25%、CuS71%、少量FeS和SiO2)中回收铍和铜两种金属的流程。

已知:I.铍、铝元素处于周期表中的对角线位置,化学性质相似
Ⅱ.常温下:Ksp[Cu(OH)2]=2.2×10-20 Ksp[Fe(OH)3]=4.0×10-38 K sp[Mn(OH)2]=2.1×10-13
(1)滤液A的主要成分除NaOH外,还有__(填化学式)。写出反应I中含铍化合物与过量盐酸反应的离子方程式__。
(2)①溶液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,选择合理步骤并排序__。
a加入过量的 NaOH b.通入过量的CO2 c加入过量的氨水 d.加入适量的HCl e.过滤 f洗涤
②从BeCl2溶液中得到BeCl2固体的操作是__。
(3)MnO2能将金属硫化物中的硫元素氧化为单质硫,若用浓HNO3代替MnO2溶解金属硫化物,缺点是__(任写一条)。
(4)溶液D中含c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.01mol·L-1,逐滴加入稀氨水调节pH可依次分离,首先沉淀的是__(填离子符号),为使铜离子开始沉淀,常温下应调节溶液的pH值大于__。
(5)取铍铜元件1000g,最终获得Be的质量为81g,则产率是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是 ( )

①食盐水 ②KNO3溶液 ③适量稀硫酸铜溶液 ④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
A.①③⑤B.①②⑥C.①②⑤D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某模拟"人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是
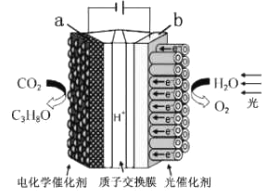
A. 该装置将化学能转化为光能和电能
B. 该装置工作时,H+从b极区向a极区迁移
C. 每生成1 mol O2,有44 gCO2被还原
D. a电极的反应为:3CO2+ 16H+-18e-= C3H8O+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示:挤压胶头滴管(装有液体)a,将液体加入到广口瓶(装有另一种物质)中,两装置中的气球(干瘪)b都有明显地胀大(忽略液体体积对气球影响,以及外界和广口瓶间热量的传递影响)。则所用试剂不可能是( )
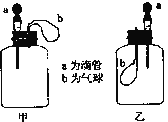
A.H2O和CaO(固体);乙:H2O和NH4NO3(固体)
B.甲:盐酸和Na2O2(固体);乙:亚硫酸钠溶液和氯气
C.甲:NaOH溶液和CO2;乙:盐酸和NaHCO3溶液
D.甲:浓H2SO4和蔗糖(固体);乙:H2O和NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是利用盐桥电池从某些含碘物质中提取碘的两个装置,下列说法中正确的是( )
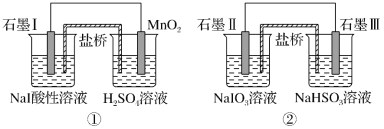
A.两个装置中,石墨I和石墨Ⅱ均作负极
B.碘元素在装置①中被还原,在装置②中被氧化
C.装置①中MnO2的电极反应式为MnO2+2H2O+2e-=Mn2++4OH-
D.装置①、②中的反应生成等量的I2时,导线上通过的电子数之比为1∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下Ka(CH3COOH)>Ka(HClO)、Ksp(AgCl)>Ksp(AgBr)。下列分析不正确的是( )
A.将10 mL 0.1 mol/L Na2CO3溶液逐滴滴加到10 mL 0.1 mol/L盐酸中:c(Na+)>c(Cl-)>c(CO32-)>c(HCO3-)
B.现有①200 mL 0.1 mol/L NaClO溶液,②100 mL0.1 mol/L CH3COONa溶液,两种溶液中的阴离子的物质的量浓度之和:②>①
C.向0.1 mol/L NH4Cl溶液中加入少量NH4Cl固体:![]() 比值减小
比值减小
D.将AgBr和AgCl的饱和溶液等体积混合,再加入足量AgNO3浓溶液:产生的AgCl沉淀多于AgBr沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com