
����Ŀ����.ʵ����ѡ������KMnO4��Һ��H2C2O4��Һ��Ӧ��̽��Ӱ�컯ѧ��Ӧ���ʵ����أ�
ʵ��ǰ��������KMnO4����Һ�ζ�δ֪Ũ�ȵIJ���
��1����ƽ��Ӧԭ�����ӷ���ʽ��
___MnO4-�� __H2C2O4��___��___Mn2���� ___CO2����____H2O
��2��̽��Ӱ�컯ѧ��Ӧ���ʵ�����
ʵ�� ��� | H2C2O4��Һ | ����KMnO4��Һ | �¶� | ||
Ũ��/mol��L��1 | ���/mL | Ũ��/mol��L��1 | ���/mL | ||
�� | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
�� | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
�� | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
a.̽���¶ȶԻ�ѧ��Ӧ����Ӱ���ʵ������_______(���ţ���ͬ)��̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ����Ӱ���ʵ������_______��
b.���Һ��ɫʱ���ɴ�С��˳����_____________��
c.���ij��ʵ��(����)ʱ��Һ��Mn2�����ʵ�����ʱ���ϵ��ͼ��ʾ���������n(Mn2��)�ڷ�Ӧ��ʼʱ�仯����һ��ʱ����������������Ҫԭ��_______��

��. ������KMnO4��Һ�ζ������ʵ�Na2C2O4��Ʒ����֪���ʲ���KMnO4��H2SO4��Һ��Ӧ����
ʵ�鲽�裺ȷȡ1 g Na2C2O4��Ʒ�����
��3�����������ҺӦװ��____�ζ����С���������ʽ��������ʽ����
��4���ζ����յ�ʱ��ʵ�������ǣ�_________��
��5��������Ʒ��Na2C2O4�Ĵ�����______%��
���𰸡�2 5 6H�� 2 10 8 �ں͢� �ٺ͢� �٣��ڣ��� Mn2���Ը÷�Ӧ�д����� ��ʽ �������һ�θ��������Һ����Һ����ɫ��Ϊ��ɫ�Ұ���Ӳ���ɫ 67
��������
(1)Mn�Ļ��ϼ���+7�۱�Ϊ+2�ۣ�C�Ļ��ϼ���+3�۱�Ϊ+4�ۣ���������к�2��̼ԭ�ӣ�����С������Ϊ10��Mn��ϵ��Ϊ2�������ϵ��Ϊ5��������̼Ϊ10�����������غ㶨�ɣ���ԭ���غ㣬ˮ��ϵ��Ϊ8���Ƴ�ȱ�ٵ�����Ϊ6H����
��2����̽���¶ȶԻ�ѧ��Ӧ����Ӱ�죬������������ͬ��ֻ�ı��¶ȣ��۷�Ӧ��ʼʱ����Ӧ���ʼ�������Ӧ����죬��ͼ����ʾ������Mn2������������죬������Mn2����������������죬��Mn2���Ը÷�Ӧ�д����ã�
1)Mn�Ļ��ϼ���+7�۱�Ϊ+2�ۣ�C�Ļ��ϼ���+3�۱�Ϊ+4�ۣ���������к�2��̼ԭ�ӣ�����С������Ϊ10��Mn��ϵ��Ϊ2�������ϵ��Ϊ5��������̼Ϊ10�����������غ㶨�ɣ���ԭ���غ㣬ˮ��ϵ��Ϊ8���Ƴ�ȱ�ٵ�����Ϊ6H������Ϊ��2��5��6H����2��10��8��
��2����̽���¶ȶԻ�ѧ��Ӧ����Ӱ�죬������������ͬ��ֻ�ı��¶ȣ���ʵ����Ϊ�ڢۣ�ͬ���ɵ�̽����Ӧ��Ũ�ȵ�ʵ����Ϊ�٢ڣ�
�ڷ�Ӧ����Խ����ɫʱ��Խ�̣���Ӧ�����ɴ�С��˳��Ϊ���ۢڢ٣���ɫʱ��Ϊ���٣��ڣ��ۣ�
�۷�Ӧ��ʼʱ����Ӧ���ʼ�������Ӧ����죬��ͼ����ʾ������Mn2������������죬������Mn2����������������죬��Mn2���Ը÷�Ӧ�д����ã�
��.������KMnO4��Һ����������ǿ�����ԣ�������ʽ�ζ���ʢ�Ÿ���Һ��
������KMnO4��Һ���Ϻ�ɫ���ζ�Na2C2O4��Һ���Ϊ��ɫ���ζ��յ��������������һ�θ��������Һָʾ����������Ϊ���������һ�θ��������Һ����Һ����ɫ��Ϊ��ɫ�Ұ���Ӳ���ɫ���۸������ӷ�Ӧʽ��n��Na2C2O4����n��KMnO4��=5��2��n��KMnO4��=0.016mol/L��25.00 L/1000����20mL��Һ��n��Na2C2O4��=0.001mol����100mL����Ʒ��Һ�к�������0.005mol��m��Na2C2O4��=0.67g����Ϊ��Ʒ������Ϊ1g������Ʒ�Ĵ���Ϊ��67%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�þ�����������ת����ϵ��

����˵���������
A.����I�����ڱ���NH4Cl��Һ
B.����I��ʹ��ˮCuSO4����ɫ
C.��ҺI����Һ�����¾�����Cu��Ӧ
D.�ڹ�������Һ�м���KI��Һ�ɲ�����ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������г��˼������ʣ��������ʵ������д�±���
���� | ͬλ�� | ͬ�������� | ͬ���칹�� | ͬϵ�� |
��� | _____ | _____ | _____ | _____ |
��CH(CH3)3��CH3CH2CH(CH3)2
��C(CH3)4��CH3CH2CH(CH3)2
��CH4��CH3CH2CH3
�ܽ��ʯ��ʯī��
��H��D��T ��
��12C��13C��14C ��
���Ҵ�(CH3CH2OH)�ͼ���(CH3OCH3)��
�����(18O3)������(16O18O )��
�� ��
��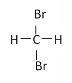
�� H216O��H218O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ҫ200mL 0.100mol��L-1 NaOH��Һ������ʱ�IJ���ʵ�������ͼ��ʾ������˵����ȷ���ǣ� ��
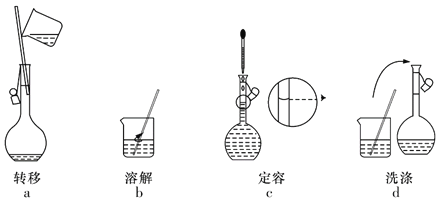
A.ʵ�������õ��IJ��������У�100mL����ƿ���ձ�������������ͷ�ιܵ�
B.ʵ������������ȷ˳��Ϊdabc
C.����ƿ��Ҫ������ˮϴ�ӣ������ſ���
D.����ʱ������������ƿ�Ŀ̶��ߣ���ʹ��õ�NaOH��ҺŨ��ƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣����е�ÿ����ĸ����һ��Ԫ�أ������Ҫ��ش����⡣
�� ���� | ��A | 0 | |||||||
1 | a | ��A | ��A | ��A | ��A | ��A | ��A | ||
2 | b | c | d | ||||||
3 | e | f | g |
��1��Ԫ��g��Ԫ�����ڱ���λ��Ϊ____________________��
��2��b��g����Ԫ�ص�ԭ�Ӱ뾶��С��ϵ��b______g������>������<����.
��3����ԭ�Ӹ�����Ϊ1��1��1��a��b��c����Ԫ����ɵĹ��ۻ�����X�����γ�4�Թ��õ��Ӷԣ���X�ĽṹʽΪ______________��
��4��f�������������e������������Ӧ��ˮ��������Һ�з�Ӧ�����ӷ���ʽΪ_________________________��
��5��A��B��D��E������������Ԫ����ɵĻ��������֮���ת����ϵ��ͼ��ʾ�����ֲ�������ȥ����A��B��D����ɫ��Ӧ���ʻ�ɫ��ˮ��Һ��Ϊ���ԡ���ش�
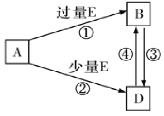
��E�ĵ���ʽΪ_______________��B�Ļ�ѧʽΪ____________________��
��A�еĻ�ѧ������Ϊ____________________
����Ȼ���д���B��D��H2O��һ�������ᾧ���ɵĹ��塣ȡһ�����ù�������ˮ���100mL��Һ�������Һ�н��������ӵ�Ũ��Ϊ0.5mo/L����ȡ��ͬ�����Ĺ���������������ٷ����仯��ʣ����������Ϊ___________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ���ǣ� ��
A.0.1mol/L��NaHC2O4��Һ�д��ڣ�c(Na+) + c(H+)=c(HC2O4) + c(C2O42-) +c(OH)
B.0.1 mol/L��NaHX��ҺpHΪ4������Һ�У�c(HX)��c(H2X)��c(X2)��c(H+)��c(OH)
C.25��ʱ��pH=8��CH3COONa��Һ�У�c(CH3COOH)ԼΪ106 mol/L
D.��0.1mol/L�� NaF��Һ�У�c(HF)��c(F)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˹�������ӡ�M�������ػ���ɹ���������������������Ԥ������������õ����ػ��ʹ�õ�����Һ��Ϊȼ�ռ���Һ��Ϊ�������ĸ��ܵ����ƽ�������֪��
��1��H2(g)=H2(l) ��H1=-0.92kJ��mol-1
��2��O2(g)=O2(l) ��H2=-6.84kJ��mol-1
��3����ͼ��
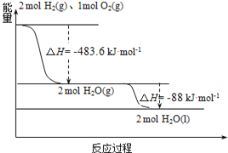
����˵����ȷ���ǣ� ��
A. 2mol H2(g)��1molO2(g)�������������2molH2O(g)�������������
B. �����Һ��ȼ�յ��Ȼ�ѧ����ʽΪ��2H2(l)+O2(l)=2H2O(g) ��H=-474.92kJ��mol-1
C. ������ȼ����Ϊ��H=-241.8kJ��mol-1
D. H2O(g)���H2O(l)�Ĺ����У��ϼ����յ�����С�ڳɼ��ų�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵�����йػ�ѧ����ı�����ȷ����( )
A. �ڻ�̬�����ԭ���У�p�����������һ������s�����������
B. ��̬Feԭ�ӵ���Χ�����Ų�ͼΪ![]()
C. ����Ԫ�ص縺�Աȵ�Ԫ�ش���ԭ�ӵ�һ�����ܱȵ�ԭ�ӵ�һ�����ܴ�
D. ����ԭ�Ӻ�������Ų����ص㣬Cu��Ԫ�����ڱ���λ��s��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ԫ��X��Y��Z��W���������������ˮ�ɵ�������Һ��0.01mol/L����������ҺpH���Ԫ��ԭ�Ӱ뾶�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
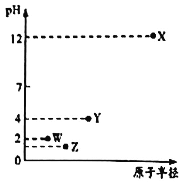
A.�����Ӱ뾶��X>Y>Z>W
B.Z��X�γɵĻ������ˮ��ҺpH>7
C.��̬�⻯����ȶ��ԣ�Z>W>Y
D.X��Y������������Ӧ��ˮ����ǡ���к�ʱ����Һ�е�������2��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com