
【题目】实验室需要200mL 0.100mol·L-1 NaOH溶液,配制时的部分实验操作如图所示,下列说法正确的是( )
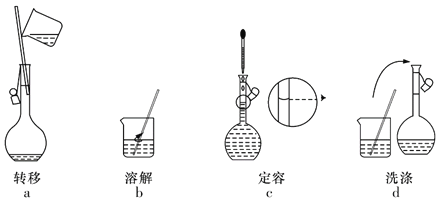
A.实验中需用到的玻璃仪器有:100mL容量瓶、烧杯、玻璃棒、胶头滴管等
B.实验操作步骤的正确顺序为dabc
C.容量瓶需要用自来水洗涤,干燥后才可用
D.定容时,若俯视容量瓶的刻度线,则使配得的NaOH溶液浓度偏高
科目:高中化学 来源: 题型:
【题目】如图所示,800 ℃时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是
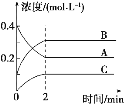
A. 发生的反应可表示为2A(g)![]() 2B(g)+C(g)
2B(g)+C(g)
B. 前2 min A的分解速率为0.1 mol/(L·min)
C. 开始时,正、逆反应同时开始
D. 2 min时,A、B、C的浓度之比为2∶3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图,下列关于该有机物的说法正确的是
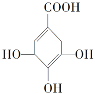
A.分子式为C7H6O5
B.分子中含有两种官能团
C.该物质能发生加成反应,氧化反应和取代反应
D.在水溶液中羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,将20mL3xmol·L-1Na3AsO3、20mL3xmol·L-1I2和20mLNaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-(aq)![]() AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43- 与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是
AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43- 与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是
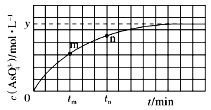
A. 溶液的pH不再变化
B. 2v正(I-)=v逆(AsO33-)
C. c(AsO43-)/c(AsO33-)不再变化
D. c(I-)=2ymol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛合金材料在航海航天等工业有十分重要的用途。钛(Ti)常温下与酸、碱均不反应,但高温下能被空气氧化。由钛铁矿(主要成分是FeO和TiO2)提取金属钛的主要工艺流程如图所示。

请回答下列问题:
(1)步骤①发生氧化还原反应,其氧化剂是___________。
(2)步骤②中发生的化学反应方程式为____________________________________________。
(3)步骤③需在氩气环境中进行,目的是__________________________________________。
(4)金属钛中常混有少量镁,提纯时可用稀硫酸除去少量的镁,其理由是___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是25 ℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是
化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
Ksp或Ka | Ksp=1.8×10-10 | Ksp=9.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
A. H2CO3、HCO3-、CH3COO-、ClO- 在溶液中可以大量共存
B. 等体积等浓度的CH3COONa和NaClO中离子总数:CH3COONa <NaClO
C. 向浓度均为1.0×10-3 mol·L-1的KCl和K2CrO4混合溶液中滴加1.0×10-3 mol·L-1的AgNO3溶液,CrO42―先形成沉淀
D. 向0.1 mol·L-1 CH3COOH溶液中滴加NaOH溶液中至c(CH3COOH):c(CH3COO-)=5∶9,此时溶液的pH=5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室选用酸性KMnO4溶液与H2C2O4溶液反应来探究影响化学反应速率的因素:
实验前先用酸性KMnO4标准溶液滴定未知浓度的草酸
(1)配平反应原理离子方程式:
___MnO4-+ __H2C2O4+___→___Mn2++ ___CO2↑+____H2O
(2)探究影响化学反应速率的因素
实验 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度 | ||
浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
a.探究温度对化学反应速率影响的实验编号是_______(填编号,下同),探究反应物浓度对化学反应速率影响的实验编号是_______。
b.混合液褪色时间由大到小的顺序是_____________。
c.测得某次实验(恒温)时溶液中Mn2+物质的量与时间关系如图所示,请解释“n(Mn2+)在反应起始时变化不大,一段时间后快速增大”的主要原因:_______。

Ⅱ. 用酸性KMnO4溶液滴定含杂质的Na2C2O4样品(已知杂质不与KMnO4和H2SO4溶液反应)。
实验步骤:准确取1 g Na2C2O4样品,配成
(3)高锰酸钾溶液应装在____滴定管中。(填“酸式”或“碱式”)
(4)滴定至终点时的实验现象是:_________。
(5)计算样品中Na2C2O4的纯度是______%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是降低润滑油凝固点的高分子有机化合物,其结构简式为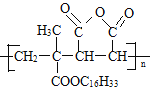 ,用石油裂解气合成M的路线图如图:
,用石油裂解气合成M的路线图如图:
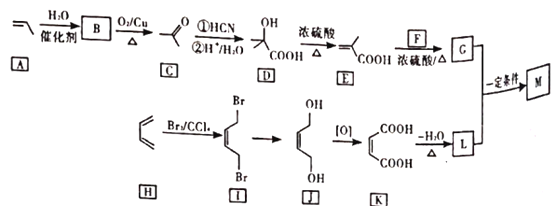
回答下列问题:
(1)B的化学名称为______。
(2)F的分子式为_____。
(3)G中官能团的名称是_____,G与L在一定条件下生成M的反应类型为____。
(4)I→J的反应方程式为_____。
(5)写出2种符合条件的C的同分异构体的结构简式____。(核磁共振氢谱为三组峰,峰面积比为3:2:1;已知双键和羟基相连时物质不稳定)
(6)设计由苯乙烯为起始原料制备![]() 的合成路线(无机试剂任选)____。
的合成路线(无机试剂任选)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨硼烷(NH3·BH3)电池可在常温下工作,装置如图所示。未加入氨硼烷之前,两极室质量相等,电池反应为NH3·BH3+3H2O2==NH4BO2+4H2O 。已知H2O2足量,下列说法正确的是( )

A. 正极的电极反应式为2H++2e-===H2↑
B. 电池工作时,H+通过质子交换膜向负极移动
C. 电池工作时,正、负极分别放出H2和NH3
D. 工作足够长时间后,若左右两极室质量差为1.9 g,则电路中转移0.6 mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com