
����Ŀ����1�����ʵ���������Ϊb%��KOH��Һ������������ȥagˮ������������� 2b%�����ΪVmL�����ʱ��Һ�����ʵ���Ũ��Ϊ___________�����𰸱���Ϊ�����ʽ��
��2����6mol/L������(��=1.19g/cm3)50mLϡ�ͳ�3mol/L������(��=1.10g/cm3)�����ˮ�����Ϊ__________mL��
��3���ܶ�Ϊ1.19g/cm3�����ᣬ��������Ϊ25%���������õ������ˮϡ�ͺ�������Һ�����ʵ���������_______����������������С����������������12.5%��
��4����֪20��ʱ������NaCl��Һ���ܶ�Ϊ��g/cm3�����ʵ���Ũ��Ϊc mol/L����NaCl��Һ���ܽ��Ϊ_________g�����𰸱���Ϊ�����ʽ��
��5����ͬ������NO2��N2O4��������֮��Ϊ_______��������֮��Ϊ_______________��
��6�����õ����ű�ʾ��ѧ����ʽCaH2+2H2O=Ca(OH)2+2H2������ת�Ƶķ������Ŀ___________��
��7������������NaOH��Һ����NH4HCO3��Һ�У���Ӧ�Ļ�ѧ����ʽ__________________������NaOH��Һ���������NH4HCO3��Һ�У���Ӧ�����ӷ���ʽΪ__________________��
���𰸡� ![]() mol/L 50.5 ����
mol/L 50.5 ���� ![]() 1:1 1:1
1:1 1:1 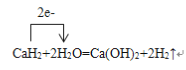 2NaOH+ 2NH4HCO3=Na2CO3+(NH4)2CO3+2H2O NH4++HCO3-+2OH-=CO32-+NH3��H2O+H2O
2NaOH+ 2NH4HCO3=Na2CO3+(NH4)2CO3+2H2O NH4++HCO3-+2OH-=CO32-+NH3��H2O+H2O
����������1����b%����������Һ������Ϊx������ǰ�����ʵ��������䣬��x��b%=��x-a����2b%����ã�x=2ag��2b%������������Һ�к����������ص����ʵ���Ϊ��![]() =
=![]() %mol��������Һ�����ʵ���Ũ��Ϊ��
%mol��������Һ�����ʵ���Ũ��Ϊ��![]() =
=![]() mol��L��1��
mol��L��1��
��2������ϡ�Ͷ��ɣ�ϡ��ǰ���������ʵ������䣬��ϡ�ͺ���������Ϊ50mL��6mol��L��1/3mol��L��1==100mL��Ũ���������Ϊ50mL��1.19g��mL��1=59.5g��ϡ���������Ϊ100mL��1.1g��mL��1=110g������ˮ������Ϊ110g-59.5g=50.5g������Ҫ����ˮ�����Ϊ50.5g/1g��mL��1=50.5mL��
��3����Ũ��������ΪV���ܶ�Ϊ�ѣ�Ũ����ϡ�ͺ��ܶ�Ϊ�ѣ�ϡ����ϡ��ǰ����Һ�����ʵ��������䣬��ϡ�ͺ�����������=![]() ��������ܶȴ���ˮ���ܶȣ�Ũ��Խ���ܶ�Խ�����Ԧѣ�Ũ��>�ѣ�ϡ��������
��������ܶȴ���ˮ���ܶȣ�Ũ��Խ���ܶ�Խ�����Ԧѣ�Ũ��>�ѣ�ϡ��������![]() >12.5%��
>12.5%��
��4��20��ʱ��1L����NaCl��Һ���ܽ���Ȼ��Ƶ�����Ϊ58.5cg����Һ����Ϊ1000�ѣ�����¶����Ȼ��Ƶ��ܽ��Ϊ��S=![]() ��100g=
��100g=![]() g��
g��
��5������ͬ������NO2��N2O4Ϊ1g��������֮��Ϊ![]() ��23��
��23��![]() ��46=1��1��������֮��=������֮��=1��1��
��46=1��1��������֮��=������֮��=1��1��
��6�����õ����ű�ʾ��ѧ����ʽCaH2+2H2O=Ca(OH)2+2H2������ת�Ƶķ������Ŀ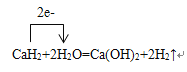
��7��HCO3��������ǿ��NH4����NaOH����HCO3����Ӧ������NH4����Ӧ������NaOH��Һ����������NH4HCO3��Һ�У�NaOHֻ��HCO3����Ӧ����Ӧ�Ļ�ѧ����ʽ2NaOH+ 2NH4HCO3=Na2CO3+(NH4)2CO3+2H2O������������NaOH��Һ����NH4HCO3��Һ�У���Ӧ�����ӷ���ʽΪNH4++HCO3-+2OH-=CO32-+NH3��H2O+H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ϸ���л�������������������
A. ��֬������ϸ���ز����ٵ�֬�� B. �����ԭ�����ۡ���ά�صĵ��嶼��������
C. DNA �� RNA ����Я���Ŵ���Ϣ D. ����ø�ı����ǵ����ʣ����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ�
A. ��һ��������ԭ��Ӧ�У���������������ǿ����������
B. ��һ��������ԭ��Ӧ�У���ԭ����Ļ�ԭ�����ڻ�ԭ��
C. amolH2SO4�У�����b����ԭ�ӣ����ӵ��������Ա�ʾΪb/4a/mol
D. ����0.05mol/LNa2CO3��Һ90mL����Na2CO3����5.3g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡһ������NaOH��Һͨ��CO2���ټ��������Һ����μ���0.1mol/L�����ᣬ����CO2������������������֮��Ĺ�ϵ��ͼ��ʾ������˵����ȷ����

A. ԭ��Һ��NaOH�����ʵ���Ϊ0.75mol
B. ͨ��CO2�����õ���Һ���ʳɷ�ΪNaOH��Na2CO3
C. ͨ��CO2�����õ���Һ�к���2.5��10-3mol NaHCO3
D. ԭ��Һͨ��CO2��״����Ϊ112mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����t��ʱ��Ag2CrO4���ٺ�ɫ����ˮ�еij����ܽ�ƽ��ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp=4��10-10������˵������ȷ���ǣ� ��

A. ��t��ʱ��Ag2CrO4��KspΪ1��10-8
B. �ڱ�����Һ�м���K2CrO4��ʹ��Һ��Y�㵽Z��
C. ��t��ʱ��Ag2CrO4��s��+2Cl����aq��![]() 2AgCl��s��+CrO42����aq��ƽ�ⳣ��K=6.25��107
2AgCl��s��+CrO42����aq��ƽ�ⳣ��K=6.25��107
D. ��t��ʱ����0.001mol/L AgNO3��Һ�ζ�20mL 0.001mol/L KCl��0.001mol/L��K2CrO4�Ļ����Һ��Cl���ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڵ��NaClˮ��Һ������������ȷ���� (����)
A. ���ʱ�������õ��������������õ�������
B. ����������������Һ�е���KI��Һ����Һ����ɫ
C. ����������������Һ�е����̪��Һ����Һ����ɫ
D. ���һ��ʱ���ȫ�����Һת�Ƶ��ձ��У���ֽ������Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���谢���ӵ�������ֵΪNA������˵������ȷ����
A�� 17g������14CH3������������Ϊ9NA
B�����³�ѹ�£�2.8 g��ϩ�ͱ�ϩ�Ļ������������̼ԭ����Ϊ0.2NA
C��0.1molC5H12�����к��е�C��C����Ϊ0.5NA
D����״���£�2.24L��������������ȫȼ������CO2������Ϊ0.8 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������˹������Ī������ʵ����2006��ɹ��ϳ���118�ų���Ԫ�أ����۲쵽������˲���1����ʱ�䡣��Ԫ�ط���Ϊ��Uuo��������Ϊ293��������������ȷ����
A. ��Ԫ��ԭ�Ӻ��⺬��118�����ӣ�������175������
B. ��Ԫ�����ڵ�������
C. ��Ԫ��һ����һ�ֽ���Ԫ��
D. ��Ԫ��λ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����agij�����к��еķ�����Ϊb����cg����������ʵ����ǣ� ��
A. bc/(aNA)mol B. ac/(bNA)mol C. ab/(cNA)mol D. b/(acNA)mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com