
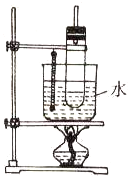
 实验室制取硝基苯常用如图装置:
实验室制取硝基苯常用如图装置:| 溴化铁 |
| 溴化铁 |


科目:高中化学 来源: 题型:
| 组号 | 反应温度/℃ | Na2S2O3 | H2SO4 | H2O体积/mL | ||
| 体积/mL | 浓度/(mol?L-1) | 体积/mL | 浓度/(mol?L-1) | |||
| A | 10 | 5 | 0.2 | 5 | 0.1 | 10 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | 10 |
| C | 30 | 5 | 0.1 | 10 | 0.1 | 5 |
| D | 30 | 5 | 0.2 | 5 | 0.2 | 10 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
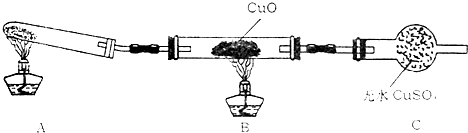
| H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 特征信息 |
| A | 其中一种原子核内只有质子没有中子 |
| B | 其原子的L层电子数是K层的3倍 |
| C | 其阳离子与B的阴离子具有相同的电子层结构, 且核电荷数与B相差3 |
| D | 其原子的最外层电子数等于电子层数,且是地壳 中含量较多的元素之一 |
| E | 单质为黄绿色气体,可用于制造漂白粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
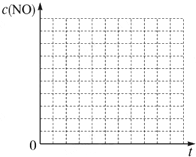 请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):| 实验编号 | T/℃ | NO初始浓度/mol?L-1 | CO初始浓度/mol?L-1 | 催化剂的比表面积/m2?g-1 |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
查看答案和解析>>
科目:高中化学 来源: 题型:

A、 、HCHO和 、HCHO和 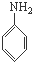 |
B、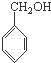 、CH3OH和 、CH3OH和 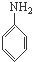 |
C、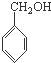 、HCHO和 、HCHO和 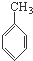 |
D、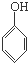 、CH3CHO和 、CH3CHO和 |
查看答案和解析>>
科目:高中化学 来源: 题型:
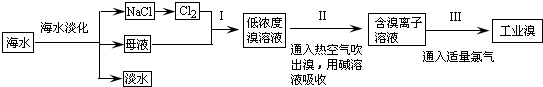
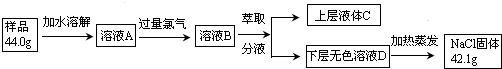
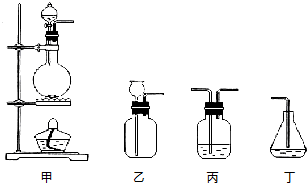
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解稀硫酸,实质上是电解水,故溶液酸性不变 |
| B、电解池内发生的反应均为自发进行的氧化还原反应 |
| C、电解硫酸钠溶液,在阴极和阳极上析出产物的物质的量之比为1:2 |
| D、电解氯化铜溶液,在阴极和阳极上析出产物的物质的量之比为1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com