
����Ŀ���о�����NOx��SO2����������Ҫ�ɷ֡�
I��NOx��Ҫ��Դ������β�����������û�ѧ����������ת��Ϊ���������ʡ�
��֪��N2(g)+O2(g)![]() 2NO(g) ��H=+180 kJ�� mol��1
2NO(g) ��H=+180 kJ�� mol��1
2CO(g)+O2(g)![]() 2CO2(g) ��H=��564 kJ�� mol��1
2CO2(g) ��H=��564 kJ�� mol��1
(1)2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) ��H=___________���÷�Ӧ��___________�����Է�����(����¡����¡��������¶ȡ�)
2CO2(g)+N2(g) ��H=___________���÷�Ӧ��___________�����Է�����(����¡����¡��������¶ȡ�)
(2)T��ʱ���������ʵ�����NO��CO�����ݻ�Ϊ2L���ܱ������У������¶Ⱥ�������䣬��Ӧ����0��5min��NO�����ʵ�����ʱ��仯����ͼ��ʾ��
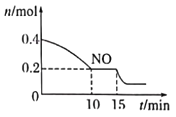
����֪��ƽ��ʱ����ķ�ѹ=����������������ϵ����ѹǿ��T��ʱ�ﵽƽ�⣬��ʱ��ϵ����ѹǿΪ��=14MPa����T��ʱ�÷�Ӧ��ѹ��ƽ�ⳣ��Kp=___________MPa��1��ƽ������������г���NO��CO2��0.1mol��ƽ�⽫___________(��������ҡ���")�ƶ�
��15minʱ�����ı���練Ӧ����������n(NO)������ͼ��ʾ�ı仯����ı������������___________(����ĸ)
A������ B������COŨ�� C��������� D��С�������
��SO2��Ҫ��Դ��ú��ȼ�ա�ȼ����������������Ǽ��ٴ����к�������Ⱦ�Ĺؼ���
(1)��֪��������ĵ��볣��ΪKa1=2.0��10��2��Ka2=6.0��10��7����NaSO3��Һ��___________(����ԡ��������ԡ����ԡ�)
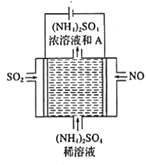
(2)��ͼ��ʾ�ĵ��װ�ã��ɽ������е�NO��SO2ת��Ϊ����泥��Ӷ�ʵ�ַ����Ļ��������á�ͨ��NO�ĵ缫��ӦʽΪ___________����ͨ���N���Ϊ4.48L(�����)��������һ���缫ͨ��SO2������������ӦΪ__________g��
���𰸡���744 kJ��mol��1 ���� 0.125(��1/8) �� BD ���� 6H����NO��5e��===NH4+��H2O 32
��������
���ݸ�˹���ɺ���G=��HT��S<0��𣻸�������ʽ, ��ѧƽ�ⳣ��K ��Qc�Ĺ�ϵ�����жϣ����� 15minʱ,�ı�ijһ����,NO�����ʵ�������,˵��ƽ��������Ӧ�����ƶ�,��ϻ�ѧƽ���Ӱ�����ط���������HSO3�ĵ���ƽ�ⳣ����ˮ��ƽ�ⳣ����С�жϣ����ݵ��װ�õ�ʧ������Ŀ�غ���м��㡣
��1�����ݸ�˹���ɢ�N2(g)+O2(g)![]() 2NO(g) ��H=+180 kJ�� mol��1 ��2CO(g)+O2(g)
2NO(g) ��H=+180 kJ�� mol��1 ��2CO(g)+O2(g)![]() 2CO2(g) ��H=��564 kJ�� mol��1,���ٵã�2NO(g)+2CO(g)
2CO2(g) ��H=��564 kJ�� mol��1,���ٵã�2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) ��H= (564180)kJmol1=744kJmol1���÷�ӦΪ���������С�ķ��ȷ�Ӧ������H<0����S<0�����¶ȴ��ڵ�����������G=��HT��S<0�����Է����У��ʴ�Ϊ��744kJmol1�����£�
2CO2(g)+N2(g) ��H= (564180)kJmol1=744kJmol1���÷�ӦΪ���������С�ķ��ȷ�Ӧ������H<0����S<0�����¶ȴ��ڵ�����������G=��HT��S<0�����Է����У��ʴ�Ϊ��744kJmol1�����£�
(2)����ͼ1֪,2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g)��
2CO2(g)+N2(g)��
��ʼ(mol) 0.4 0.4 0 0
ת��(mol) 0.2 0.2 0.2 0.1
ƽ��(mol) 0.2 0.2 0.2 0.1
����ֵ���������ֱ��ǣ�![]() ��
��![]() ��
��![]() ��
��![]() ��,Kp=
��,Kp=![]() =(14��
=(14��![]() )2��(14
)2��(14![]() )/ [(14��
)/ [(14��![]() )2��(14��
)2��(14��![]() )2]=0.125�����ݢٵķ���,��ѧƽ�ⳣ��K=
)2]=0.125�����ݢٵķ���,��ѧƽ�ⳣ��K=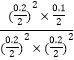 =5,���������г���NO��CO2��0.3mol����ʱ��Ũ����Qc=
=5,���������г���NO��CO2��0.3mol����ʱ��Ũ����Qc=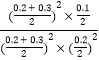 =5=K�����ƽ�ⲻ�ƶ����ʴ�Ϊ��0.125������
=5=K�����ƽ�ⲻ�ƶ����ʴ�Ϊ��0.125������
��15minʱ���ı�ijһ���أ�NO�����ʵ������٣�˵��ƽ��������Ӧ�����ƶ���
A. ����Ӧ�Ƿ��ȷ�Ӧ�����£�ƽ�����淴Ӧ�����ƶ���NO�����ʵ�������A����
B. ����CO��Ũ�ȣ�ƽ��������Ӧ�����ƶ���NO�����ʵ�����С����B��ȷ��
C. �����������ѧƽ�ⲻ�ƶ�����C����
D. ��С������������൱������ѹǿ��ƽ��������Ӧ�����ƶ���NO���ʵ�����С����D��ȷ��
�ʴ�Ϊ��BD��
��(1)����HSO3��ˮ�ⳣ��K=Kw/Ka1=5.0��1013<Ka2=6.0��107,˵��HSO3�ĵ���ƽ�ⳣ������ˮ��ƽ�ⳣ������HSO3����Һ�����ԣ��𰸣����ԣ�/span>
(2)���ݵ��װ�ã�NO��SO2ת��Ϊ����泥�˵��NOת����NH4+����NO�������Ϸ�����ӦNO+6H++5e=NH4++H2O��������ӦʽΪSO2+2H2O2e=4H++SO42,���ݵ�ʧ������Ŀ�غ㣬��2NO10e5SO2����SO2�����ʵ���Ϊ��n(SO2)=5/2n(NO)=4.48L/22.4Lmol-1��5/2=0.5mol��SO2������Ϊ64g/mol��0.5mol=32g���ʴ�Ϊ��6H����NO��5e��===NH4+��H2O��32��


 Ӣ�ŵ��ϵ�д�
Ӣ�ŵ��ϵ�д� ������������Ծ�ϵ�д�
������������Ծ�ϵ�д� �������Ӳ�ϵ�д�
�������Ӳ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������PAA��![]() �����и���ˮ�ԣ���״PAA�ڿ�ѹ�ԡ���ˮ�Եȷ�����������PAA����״PAA���Ʊ������ǣ�����ϩ����NaOH�кͣ���������������a���������ۺϡ��䲿�ֽṹƬ�����£�
�����и���ˮ�ԣ���״PAA�ڿ�ѹ�ԡ���ˮ�Եȷ�����������PAA����״PAA���Ʊ������ǣ�����ϩ����NaOH�кͣ���������������a���������ۺϡ��䲿�ֽṹƬ�����£�
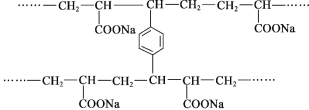
����˵������ȷ���ǣ� ��
A. ����PAA�ĵ��岻����˳���칹����
B. ������a�Ľṹ��ʽ��![]()
C. �γ���״�ṹ�Ĺ��̷����˼Ӿ۷�Ӧ
D. PAA�ĸ���ˮ���롪COONa�й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�У����巴Ӧ��ȱ������ֱ���ԭ����
A.������¶���ڿ�����Ѹ�ٱ䰵
B.¶���ڿ����еĹ������ƹ�����
C.���������Ȼ����ϣ�������������
D.���������������Թܵ�����ˮ���У��Թ���Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��36.5gHCl�ܽ���1Lˮ��(ˮ���ܶȽ���Ϊ1 gmL-1)��������Һ���ܶ�Ϊ�� gmL-1����������Ϊw�����ʵ���Ũ��Ϊc gmL-1��NA��ʾ�����ӵ�����������˵����ȷ����( )
A.������Һ�����ʵ���Ũ�ȣ�c=1 gmL-1
B.������Һ�к���NA��HCl����
C.36.5 gHCl����ռ�е����Ϊ22.4L
D.������Һ����������: w=![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ǹ�Ч�Ŀ�ű��ҩ��Ϊ��ɫ��״���壬�����ڱ�ͪ���ȷºͱ��У��״����Ҵ������ѡ�ʯ�����п��ܽ⣬��ˮ�м������ܣ��۵�Ϊ156-157��C�����ȶ��Բ��֪�����ѷе�Ϊ35��C����ȡ�����ص���Ҫ����Ϊ��

�����йش˹��ղ����������( )
A.�����Ŀ�����������������ѵĽӴ��������������ؽ�ȡ��
B.��������Ҫ�õ��IJ���������©�������������ձ�
C.�����������������������������صķе����ϴ�
D.���������Ҫ���̼�ˮ�ܽ⣬����Ũ������ȴ�ᾧ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����Һ�пɷ������·�Ӧ����16H����10Z����2![]() ===2X2����5Z2��8H2O����2M2����R2===2M3����2R������2R����Z2===R2��2Z�����ɴ��ж�����˵���������( )
===2X2����5Z2��8H2O����2M2����R2===2M3����2R������2R����Z2===R2��2Z�����ɴ��ж�����˵���������( )
A��������ǿ��˳��Ϊ��![]() <Z2<R2<M3��
<Z2<R2<M3��
B����ԭ��ǿ��˳��Ϊ��X2��<Z��<R��<M2��
C��ZԪ���ڷ�Ӧ���б��������ڢ��б���ԭ
D�������¿ɷ�����Ӧ2M2����Z2===2M3����2Z��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���ṹ��ʽΪ ��������������ȷ����(����)
��������������ȷ����(����)
A. 1 mol ���л����ڼ��Ⱥʹ��������£�����ܺ�4 mol H2��Ӧ
B. ���л�����ʹ��ˮ��ɫ��Ҳ��ʹ����KMnO4��Һ��ɫ
C. ���л�������������Һ������ɫ����
D. ���л�����һ���������ܷ�����ȥ��Ӧ��ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��þ��ϡ����ķ�ӦΪ��Mg�� HNO3(ϡ)���� Mg(NO3)2�� NO���� H2O
(1)��ƽ������ѧ����ʽ������˫���ŷ�����ʾ�÷�Ӧ�е���ת�Ƶķ������Ŀ��________
(2)�÷�Ӧ�У���ԭ������_________��HNO3������______________��ѡ������ԭ����������������������������������������
(3)����Ӧ������ת�Ƶĵ���Ϊ0.6 mol����ԭ���������ʵ���Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��̬����������ܶȸߡ��ɱ��ͣ��乤��ԭ����ͼ��ʾ�����е缫 a���ò���ʯīϩ��S8���ϣ���ط�ӦΪ��16Li+xS8=8Li2Sx��2��x��8��������˵��������ǣ� ��

A. ��ع���ʱ�������ɷ�����Ӧ��2Li2S6+2Li++2e-=3Li2S4
B. ��ع���ʱ�����·������ 0.02 mol ���ӣ��������ϼ��� 0.14 g
C. ʯīϩ��������Ҫ����ߵ缫a�ĵ�����
D. ��س��ʱ��Խ���������Li2S2����Խ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com