
【题目】已知五种元素的原子序数大小顺序为C>A>B>D>E,A、C同周期,B、C同主族。A与B形成的离子化合物A2B中所有离子的电子数相等,其电子总数为30;D和E可形成4核10个电子的分子。
试回答下列问题:
(1)写出这五种元素的名称:A___,B____,C___,D__,E___。
(2)用电子式表示离子化合物A2B的形成过程___。
(3)按要求表示下列化合物的原子构成关系:
①D元素形成单质的电子式___;
②E与B形成化合物的电子式___;
③A、B、E形成化合物的电子式___;
④D与E两元素按原子数目比为1∶3和2∶4构成分子M和N,M的电子式___,N的结构式___。
【答案】钠 氧 硫 氮 氢 ![]()
![]()
![]() 或
或![]()
![]()
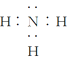
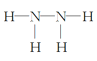
【解析】
A与B形成离子化合物A2B,A2B中所有离子的电子数相同,且电子总数为30,所以每个离子都有10个电子,由化学式的结构可知,B带2个单位负电荷,A带1个单位正电荷,所以A是Na元素,B是O元素,因为A、C同周期,B与C同主族,所以C为S元素;D和E可形成4核10电子的分子,每个原子平均不到3个电子,可知其中一定含有氢原子,分子中有4个原子核共10个电子,一定是NH3,结合原子序数D>E,可知D是N元素,E是H元素。
(1)由分析可知:A是Na,B为O,C是S,D是N,E为H,故答案为:钠、氧、硫、氮、氢;
(2)A2B是Na2O,由钠离子与氧离子形成的离子化合物,Na2O的形成过程为![]() ,故答案为:
,故答案为:![]() ;
;
(3)①D为N元素,其单质为氮气,两个氮原子间形成叁键,D元素形成单质的电子式![]() ;故答案为:
;故答案为:![]()
②H与O形成的化合物H2O、H2O2,形成化合物的电子式![]() 或
或![]() ;故答案为:
;故答案为:![]() 或
或![]() ;
;
③Na、O、H形成的化合物NaOH为离子化合物,电子式![]() ;故答案为:
;故答案为:![]() ;
;
④D与E两元素按原子数目比为1∶3和2∶4构成分子M和N,M为NH3,中心原子氮形成三个共价键,N为N2H4分子中两个氮原子形成非极性共价键,M的电子式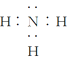 ,N的结构式
,N的结构式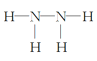 。故答案为:
。故答案为: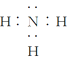 ;
;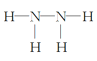 。
。


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数。下列说法正确的是
A. 标准状况下,22.4LCH4中含有氢原子数目为4NA
B. 1molNa2O2中含有的阴离子和阳离子的数目都是2NA
C. 0.1mol/LCu(NO3)2溶液中含有的NO3-数目为0.2NA
D. 28gN2中所含的原子数目是NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2—CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。下列说法中正确的是( )
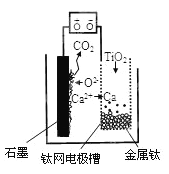
A. 将熔融CaF2—CaO换成Ca(NO3)2溶液也可以达到相同目的
B. 阳极的电极反应式为:C+2O2--4e-=CO2↑
C. 在制备金属钛前后,整套装置中CaO的总量减少
D. 石墨为阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和H2是工业上最常用的合成气,该合成气的制备方法很多,它们也能合成许多重要的有机物。回答下列问题:
(1)制备该合成气的一种方法是以CH4和H2O为原料,有关反应的能量变化如图所示。
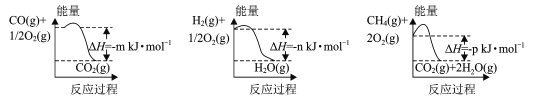
CH4 (g)与H2O(g)反应生成CO(g)和H2 (g)的热化学方程式为____。
(2)工业乙醇也可用CO和H2合成,常含一定量甲醇,各国严禁使用成本低廉的工业酒精勾兑食用酒,但一般定性的方法很难检测出食用酒中的甲醇。有人就用硫酸酸化的橙色K2Cr2O7溶液定量测定混合物中甲醇的含量,甲醇与酸性K2Cr2O7溶液反应生成CO2、Cr2(SO4)3等物质,写出其化学方程式 ___________。
(3)为了检验由CO和H2合成气合成的某有机物M的组成,进行了如下测定:将1.84gM在氧气中充分燃烧,将生成的气体混合物通过足量的碱石灰,碱石灰 增重4. 08 g,又知生成CO2和H2O的物质的量之比为3:4。则M中碳、氢、氧原子个数之比为____。
(4) CO2和H2合成甲醇涉及以下反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g) H=-49.58kJ/mol。在反应过程中可以在恒压的密闭容器中,充入一定量的CO2和H2,测得不同温度下,体系中CO2的平衡转化率与压强的关系曲线如图所示:
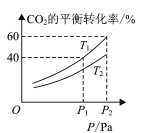
①反应过程中,表明反应达到平衡状态的标志是______;
A.生成3mol O-H键,同时断裂3mol H-H键 B.容器中气体的压强不再变化
C.容器中气体的平均摩尔质量不变 D.CH3OH的浓度不再改变
②比较T1与T2的大小关系:T1 ___T2 (填“<”、“=”或“>”)。
③在T1和P2的条件下,向密闭容器中充入1mol CO2和3mol H2,该反应在第5 min时达到平衡,此时容器的容积为2.4 L,则该反应在此温度下的平衡常数为____,保持T1和此时容器的容积不变,再充入1mol CO2和3mol H2,设达到平衡时CO2的总转化率为a,写出一个能够解出a的方程或式子 ___(不必化简,可以不带单位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温下使NH2COONH4 ( s) ![]() 2NH3 (g)+CO2 (g)达到平衡,不可以判断该反应达到化学平衡的是 ( )
2NH3 (g)+CO2 (g)达到平衡,不可以判断该反应达到化学平衡的是 ( )
A. V正(NH3) =2V逆(CO2)B. 密闭容器中氨气的体积分数不变
C. 密闭容器中总压强不变D. 密闭容器中混合气体的密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[选修3——物质结构与性质] 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)在Y的最高价氧化物分子中,Y原子轨道的杂化类型是_______________。
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是_______________________;Z的氢化物在固态时的密度比在液态时还小,其原因是_________
(3)Y与Z可形成YZ42-。
①YZ42-的空间构型为________________(用文字描述)。
②写出一种与YZ42-互为等电子体的分子的化学式:_________________。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的
数目为_______。
(5)X与Y所形成化合物晶体的晶胞如图所:
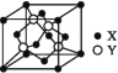
①在该晶体中,X离子的配位数为__________,与Y距离最近且距离相等的Y原子的数目为________。
②该晶胞的边长为a cm,该晶体的密度为__________________ g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废气、汽车尾气排放出的SO2、NOx等,是形成雾霾的重要因素。霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾。
(1)NOx和SO2在空气中存在下列平衡:
2NO(g)+ O2(g)![]() 2NO2(g) △H= —112 kJ·mol-1
2NO2(g) △H= —112 kJ·mol-1
2SO2(g)+ O2 (g) ![]() 2SO3(g) △H= —196 kJ·mol-1
2SO3(g) △H= —196 kJ·mol-1
SO2通常被NO2进一步氧化,生成SO3和一种无色有毒的气体。请写出NO2和SO2反应的热化学方程式______________。
(2) 常温下,烟气中SO2被NaOH溶液吸收可得到NaHSO3、Na2SO3等。
①已知Na2SO3水溶液显碱性,原因是____________(写出主要反应的离子方程式),该溶液中c(Na+)____ 2c(SO32-)+ c(HSO3-)(填“>”“<”或“=”)。
②常温下,0.1mol/L的NaHSO3溶液的PH=6,则c(SO32-)—c(H2SO3)= ______ mol/L(填写准确数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向200mLFeCl3与HCl的混合溶液中,分别加入一定量成分均匀的Fe、Cu混合固体,充分反应后剩余固体的质量及放出气体的体积(标准状况下测得)如下表所示。
加入固体质量/g | 9.00 | 18.0 | 27.0 |
剩余固体质量/g | 3.20 | 9.60 | 15.8 |
放出气体体积/L | 0 | 1.12 | 2.24 |
试计算:
(1)原混合液中c(Cl-)=____。
(2)混合固体中n(Fe):n(Cu)=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系。
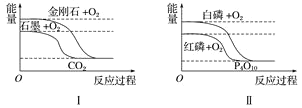
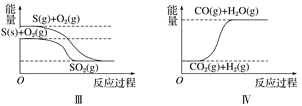
据此判断下列说法中正确的是 ( )
A. 白磷比红磷稳定
B. 石墨转变为金刚石是吸热反应
C. S(g)+O2(g)=SO2(g) ΔH1 S(s)+O2(g)=SO2(g) ΔH2 则ΔH1>ΔH2
D. CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com