
【题目】下列反应中说明NH3既有还原性,又有碱性的是( )
A. 4NH3+5O2![]() 4NO+6H2O B. NH3+HNO3=NH4NO3
4NO+6H2O B. NH3+HNO3=NH4NO3
C. 8NH3+3Cl2=N2+6NH4Cl D. 2NH3+3CuO![]() 3Cu+N2+3H2O
3Cu+N2+3H2O
【答案】C
【解析】
还原性是指物质所含元素的化合价升高,碱性是指能跟酸性物质反应。NH3中N的化合价为-3价,H的化合价为+1价,说明氨气具有还原性,只能是NH3中-3价的N化合价升高,说明氨气具有碱性,是指NH3能跟酸性物质反应,据此分析。
A.4NH3+5O2![]() 4NO+6H2O中NH3中-3价的N被O2氧化,氨气具有还原性,不表现氨气的碱性,A错误;
4NO+6H2O中NH3中-3价的N被O2氧化,氨气具有还原性,不表现氨气的碱性,A错误;
B. NH3+HNO3=NH4NO3中,反应前后化合价未变,该反应不是氧化还原反应,不合题意,B错误;
C.8NH3+3Cl2=N2+6NH4Cl反应的本质为3Cl2+2NH3=N2+6HCl①,过量的NH3与HCl反应,HCl+NH3=NH4Cl②,将①+②×6得:3Cl2+8NH3=N2+6NH4Cl。①为氧化还原反应,NH3中-3价的N被Cl2氧化,NH3表现还原性;②为非氧化还原反应,NH3跟酸性气体HCl物质反应,NH3表现碱性,符合题意,C正确;
D.2NH3+3CuO![]() 3Cu+N2+3H2O中NH3-3价的N被CuO氧化,氨气具有还原性,但是不表现氨气的碱性,D错误;
3Cu+N2+3H2O中NH3-3价的N被CuO氧化,氨气具有还原性,但是不表现氨气的碱性,D错误;
故合理选项是C。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】25℃时,向100 mL 0.1 mol·L-1 NH4HSO4溶液中滴加0.1 mol·L-1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图。下列说法不正确的是

A. a点时溶液的pH<1
B. a点到b点的过程中,溶液的导电能力增强
C. c点关系式:c(NH4+)+c(Na+)=2c(SO42-)
D. b点时离子浓度大小顺序为: c(SO42-)=c(Na+)>c(NH4+)> c(H+)> c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)![]() 2SO3(g) △H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) △H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是

A. 图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响
B. 图Ⅱ表示的是t1时刻通入氦气增大体系压强对反应速率的影响
C. 图Ⅱ表示的t1时刻加入催化剂后对反应速率的影响
D. 图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛被称为“第三金属”,其制取原料为金红石(TiO2),制取步骤为:
TiO2 → TiCl4 ![]() Ti
Ti
已知:①C(s)+O2(g)===CO2(g) ΔH1 ②2CO(g)+O2(g)===2CO2(g) ΔH2
③TiO2(s)+2Cl2(g)===TiCl4(s)+O2(g) ΔH3
则反应TiO2(s)+2Cl2(g)+2C(s)===TiCl4(s)+2CO(g)的ΔH为
A. ΔH3+2ΔH1+2ΔH2 B. ΔH3+2ΔH1+ΔH2
C. ΔH3+2ΔH1-ΔH2 D. ΔH3+2ΔH1-2ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施是为了降低化学反应速率的是
A.食品放在冰箱中贮藏B.工业炼钢用纯氧代替空气C.合成氨工业中使用催化剂D.在加热条件下,用氢气还原氧化铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10 mL 1 mol L-1NaOH洛液稀释到100 mL,再取出5 mL稀释后的溶液,则这5 mL溶液中溶质的物质的量浓度是
A.0.05 mol L-1B.0.25 mol L-1C.0.1 mol L-1D.0.5 mol L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图海水综合利用的工业流程图,判断下列说法正确的是
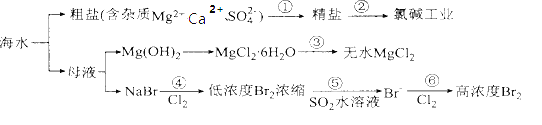
已知:MgCl26H2O受热生成Mg(OH)Cl和HCl气体等.
A.过程①加入的药品顺序为:Na2CO3溶液→BaCl2溶液→NaOH溶液→过滤后加盐酸
B.过程②通过氧化还原反应可产生1种单质
C.在过程③中将MgCl26H2O直接灼烧得到MgCl2
D.在过程④、⑥反应中每氧化0.2molBr-需消耗标准状况下2.24LCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A. HCl和NaOH反应的中和热△H=-57.3 kJ·mol1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ·mol1
B. 甲烷的标准燃烧热ΔH=-890.3 kJ·mol1,则CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH<-890.3 kJ·mol1
C. 已知:500℃、30MPa下,N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4kJ·mol-1;将1.5 mol H2和过量的N2在此条件下充分反应,放出热量46.2 kJ
2NH3(g) ΔH=-92.4kJ·mol-1;将1.5 mol H2和过量的N2在此条件下充分反应,放出热量46.2 kJ
D. CO(g)的燃烧热是283.0kJ·mol1,则2CO2(g) ===2CO(g)+O2(g)反应的△H=+566.0 kJ·mol1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com