
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 18g2H2O中含有的中子数为10NA
B. 11.2 LCl2与足量NaOH 溶液反应时转移的电子数为0.5 NA
C. 1mol·L-1的Fe2(SO4)3溶液中含有的SO42-数为3 NA
D. 7 g 乙烯和丁烯的混合气体中所含的碳原子数是0.5 NA
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
【题目】某同学做如下实验,以探究反应中的能量变化。
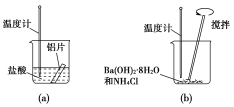
(1)在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是________热反应;(b)中温度降低,由此可以判断(b)中反应是________热反应。
(2)写出铝与盐酸反应的离子方程式:_______________。
(3)根据能量守恒定律,(b)中反应物的总能量应该________生成物的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1) 在这些元素中,化学性质最不活泼的是:_________(填具体元素符号,下同),②③⑤元素的原子半径由大到小的顺序为______________________ 。
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是____________/span>,碱性最强的化合物的电子式是:______________________________。
(3) 最高价氧化物是两性氧化物的元素是____;写出该氧化物与氢氧化钠反应的离子方程式_____。
(4) 用电子式表示元素④与⑥的化合物的形成过程:______________,该化合物属于__________(填 “共价”或“离子”)化合物。
(5)写出①与③形成的化合物的电子式____、结构式为___,该化合物的晶体属于_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的某种方法过程如图所示:
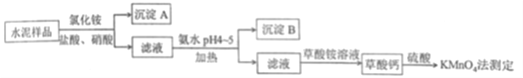
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是_____________,还可使用__________代替硝酸。
(2)沉淀A的主要成分是________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为____________。
(3)加氨水过程中加热的目的是_____。沉淀B的主要成分为_______、_________(填化学式)。
Ⅱ、已知25℃时草酸的电离常数为K1=5.0×10-2,K2=5.4×10-5.草酸钙的Kap=4.0×10-8.碳酸钙的Ksp=2.5×10-9.不同温度下水的离子积常数见下表:
t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
Kw/10-14 | 0.134 | 0.292 | 0.681 | 1.00 | 2.92 | 5.57 | 38.0 | 55.0 |
(1)计算25℃时KHC2O4溶液的水解平衡常数Kb=_____;写出水溶液中草酸的电离方程式_____;常温下将0.2mol/L的KOH溶液10mL与0.2mol/L的草酸溶液20mL混合后溶液显________性。(填“酸性”“中性”或“无法确定”)
(2)25℃时向20mL草酸钙的饱和溶液中逐滴加入8.0×10-4mol/L的碳酸钾溶液10mL,能否产生沉淀,_______(填“能”或“否”). 碳酸钙转化为草酸钙的离子方程式为______,列式计算该反的平衡常数K=_________。
(3)90℃时,将0.005mol/L的氢氧化钙溶液20mL与0.0012mol/L的草酸溶液20mL混合,则混合后溶液的pH______。(可能用到的对数:lg38=1.6,lg26=2.4,lg2=0.3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3、和FeO)得到绿矾(FeSO4·7H2O),在通过绿矾制备铁黄[FeO(OH)]的流程如下:
![]()
已知:FeS2和铁黄均难溶于水
下列说法不正确的是
A. 步骤①,最好用硫酸来溶解烧渣
B. 步骤②,涉及的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+
C. 步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D. 步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】居民所用石油液化气的主要成分是丁烷,在使用过程中,常有一些杂质以液态沉积于钢瓶中,这些杂质可能是( )
A. 甲烷和丙烷 B. 丁烷和甲醛 C. 乙烷和丁烷 D. 戊烷和己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 糖类化合物都具有相同的官能团 B. 酯类物质是形成水果香味的主要成分
C. 油脂的皂化反应生成脂肪酸和丙醇 D. 蛋白质的水解产物都含有羧基和羟基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 在加热、甲醛、饱和(NH4)2SO4溶液、X射线作用下,蛋白质都会发生变性
B. 氨基酸、蛋白质、油脂都含有C、H、O、N四种元素
C. 生活中食用的食醋、植物油、动物蛋白等物质都是混合物
D. 乙烯、聚乙烯、苯均能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为常见温室气体,B为淡黄色氧化物,C为常见液体,D为黄绿色气体单质,相互反应的关系如右图所示,M的水溶液能杀菌消毒。下列有关叙述正确的是
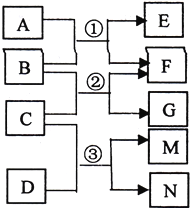
A. 4.4gA含有4.4NA个质子
B. 7.8gB与足量A发生反应①,共转移0.2NA电子
C. 反应③的离子方程式为:Cl2+H2O![]() 2H++Cl-+ ClO-
2H++Cl-+ ClO-
D. M的电子式为:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com