
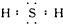 ��������Hԭ�Ӻ�Sԭ��֮����ڼ��Լ�������ΪV�νṹ������������IJ��غϣ�����Ϊ���Է��ӣ�
��������Hԭ�Ӻ�Sԭ��֮����ڼ��Լ�������ΪV�νṹ������������IJ��غϣ�����Ϊ���Է��ӣ�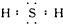 �����ԣ����ԣ�
�����ԣ����ԣ� 


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c��A2-��+c��OH-��=c��H2A��+c��H+�� |
| B��c��HA-����c��A2-����c��H2A�� |
| C��c��HA-����c��H+����c��OH-�� |
| D��c��HA-����c��OH-����c��A2-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ӧ�б������뱻��ԭ��Ԫ�أ���ԭ�ӵ����ʵ���֮��Ϊ1��2 |
| B��NF3��NH3��ѧ���ʵIJ�ͬ����F��H��Ԫ�طǽ����ԵIJ������� |
| C��NF3һ��й©������NaOH��Һ���ܣ�ֻ��NaF��NaNO3��H2O���� |
| D������Ӧ��ת��0.2mol���ӣ������ɵ�NO�������ԼΪ4.48L����״���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1����һ���Ϊ10L�������У�ͨ��һ������CO��H2O���� 800��ʱ�������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H��0��CO��H2O�����ʵ���Ũ�ȱ仯��ͼ��ʾ����
��1����һ���Ϊ10L�������У�ͨ��һ������CO��H2O���� 800��ʱ�������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H��0��CO��H2O�����ʵ���Ũ�ȱ仯��ͼ��ʾ����| C����I-��/mol?L-1 | C����Fe3+��/mol?L-1 | v/mol?L-1?s-1 | |
| �� | 0.20 | 0.80 | 0.032k |
| �� | 0.60 | 0.40 | 0.144k |
| �� | 0.80 | 0.20 | 0.128k |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
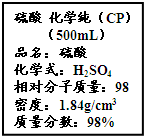 ��Ҫ���������С�⣮
��Ҫ���������С�⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| t�� | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com