
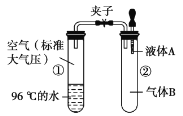
【题目】如图所示,夹子开始处于关闭状态,将液体A滴入试管②中与气体B充分反应,打开夹子,可发现试管①中的水立刻沸腾了。则液体A和气体B的组合不可能是下列选项中的( )
A.氢氧化钠溶液、二氧化碳B.水、氨气
C.氢氧化钠溶液、一氧化氮D.水、二氧化氮
【答案】C
【解析】
水的沸点与压强有关,压强越小水的沸点越低,压强越大水的沸点越高;将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了,说明试管②中气体的压强减小,以此解答该题。
A. 氢氧化钠溶液能吸收二氧化碳气体,打开夹子时①中的气体进入②中,从而使得①中的压强减小,水的沸点降低,水沸腾了,A不符合题意;
B. 氨气易溶于水,①中的压强减小,水的沸点降低,水沸腾,B不符合题意;
C. 一氧化氮和氢氧化钠不反应,打开夹子时①中的压强不变,水的沸点不变仍然是100℃,所以水不能沸腾,C符合题意;
D. 水和二氧化氮反应,使试管②中气体的压强减小,打开夹子时①中的气体进入②中,从而使得①中的压强减小,水的沸点降低,水沸腾,D不符合题意;
故合理选项是C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】留兰香(薄荷中的一种)可用来治疗感冒咳嗽、胃痛腹胀、神经性头痛等,其有效成分为葛缕酮(结构简式如图)。下列有关葛缕酮的说法正确的是
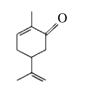
A.葛缕酮的分子式为C10H16O
B.葛缕酮使溴水和酸性KMnO4溶液褪色的原理相同
C.葛缕酮中所有碳原子可能处于同一个平面
D.羟基直接连苯环且苯环上有2个取代基的葛缕酮的同分异构体有12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产铅蓄电池时,在两极板上的铅、锑合金棚架上均匀涂上膏状的PbSO4,干燥后再安装,充电后即可使用,发生的反应是Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O。下列对铅蓄电池的说法错误的是( )
2PbSO4+2H2O。下列对铅蓄电池的说法错误的是( )
A.需要定期补充硫酸
B.工作时铅是负极,PbO2是正极
C.工作时负极上发生的反应是Pb-2e-+SO42-=PbSO4
D.工作时电解质的密度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年10月8日,瑞典皇家科学院宣布将诺贝尔化学奖授予日本科学家下村修、美国科学家马丁沙尔菲与美籍华裔科学家钱永健,以表彰三人因在发现和研究绿色荧光蛋白方面做出的贡献。蛋白质是一类复杂的含氮化合物,每种蛋白质都有其恒定的含氮量[约在14%~18%(本题涉及的含量均为质量分数)],故食品中蛋白质的含量测定常用凯氏定氮法,其测定原理是:
Ⅰ.蛋白质中的氮(用氨基表示)在强热和CuSO4、浓H2SO4作用下,生成一种无机含氮化合物,反应式为:2(-NH2)+H2SO4+2H+![]() ;
;
Ⅱ.该无机化合物在凯氏定氮器中与碱作用,通过蒸馏释放出NH3,收集于H3BO3溶液中,生成(NH4)2B4O7;
Ⅲ.用已知浓度的HCl标准溶液滴定,根据HCl消耗的量计算出氮的含量,然后乘以相应的换算系数,即得蛋白质的含量。
(1)上述原理第Ⅰ步生成的无机含氮化合物化学式为_________;
(2)乳制品的换算系数为6.38,即若检测出氮的含量为1%,蛋白质的含量则为6.38%.不法分子通过在低蛋白含量的奶粉中加入三聚氰胺(Melamine)来“提高”奶粉中的蛋白质含量,导致许多婴幼儿肾结石。
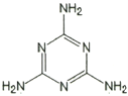
①三聚氰胺的结构如图所示,其化学式为_________,含氮量(氮元素的质量分数)为_________;
②下列关于三聚氰胺的说法中,正确的有_________;
A.三聚氰胺是一种白色结晶粉末,无色无味,所以掺入奶粉后不易被发现
B.三聚氰胺分子中所有原子可能在同一个平面上
C.三聚氰胺呈弱碱性,可以和酸反应生成相应的盐
③假定奶粉中蛋白质含量为16%即为合格,不法分子在一罐总质量为500g、蛋白质含量为0的假奶粉中掺入_________g的三聚氰胺就可使奶粉“达标”。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料,印泥及朱红雕刻漆器等。某温度时,HgS在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
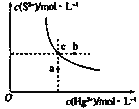
A.向硫化汞的浊液中加入硫化钠溶液,硫化汞的Ksp减小
B.图中a点对应的是饱和溶液
C.向c点的溶液中加入Hg(NO3)2,则c(S2-)减小
D.升高温度可以实现c点到b点的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图是硫酸试剂标签上的部分内容。下列说法正确的是 ( )

A.该硫酸的物质的量浓度为9.2 mol/L
B.1mol锌与足量的该硫酸反应产生2g氢气
C.配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL
D.该硫酸与等体积的水混合所得溶液的物质的量浓度等于9.2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5mol·L-1一元强酸HA溶液和未知浓度的一元强碱BOH溶液以1∶2的体积比混合,所得溶液的c(OH-)=0.1mol·L-1,用此碱溶液中和20mL一元弱酸HC[该酸溶液c(H+)=0.01mol·L-1],当恰好完全反应时,用5mLB溶液,求弱酸HC的电离度____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+,进行以下实验,记录实验结果,并思考改变物质浓度对平衡移动的影响。
2CrO42-(黄色)+2H+,进行以下实验,记录实验结果,并思考改变物质浓度对平衡移动的影响。
实验1:向试管中加入4mL 0.1mol·L-1 K2Cr2O7溶液,再加数滴1mol·L-1 NaOH溶液,观察溶液颜色变化;
实验2:将上述溶液分成两份向其中一份中滴加1mol·L-1 HNO3,观察溶液颜色变化,并和另一份做对比_____。
实验现象 | 实验结论 | |
实验1 | ||
实验2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com