
【题目】下列说法正确的是( )。
A.在一定条件下,等物质的量的乙烯和苯分别和足量氢气发生加成反应,消耗氢气的物质的量之比为![]()
B.与甲烷、乙烯相比,苯的独特性质具体来说是易取代,能加成,难氧化
C.除去乙烷中混有的乙烯,应在一定条件下通入氢气,使乙烯转化为乙烷
D.某有机物的结构简式为![]() ,其分子结构中处在同平面内的原子最多有15个
,其分子结构中处在同平面内的原子最多有15个
【答案】B
【解析】
A.1mol乙烯和1mol氢气发生加成反应;1mol苯和3mol氢气发生加成反应;在一定条件下,等物质的量的乙烯和苯分别和足量氢气发生加成反应,消耗氢气的物质的量之比为1:3,A错误;
B.苯可发生加成反应,条件困难,甲烷光照下发生取代反应,而苯在催化剂条件下发生取代反应,乙烯能被高锰酸钾氧化,而苯不能,与甲烷、乙烯相比,苯的独特性质具体来说是易取代,能加成,难氧化,B正确;
C.乙烷中混有乙烯,若采用通入H2与乙烯反应生成乙烷的方法除去乙烯,H2的量不容易控制,可能会引入H2杂质,C错误;
D.根据苯是平面结构,12个原子共平面,乙烯6个原子共平面,甲烷最多3个原子共平面,推出![]() 分子结构中处在同一平面内的原子最多有17个,D错误;
分子结构中处在同一平面内的原子最多有17个,D错误;
答案选B。


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】甲是短周期元素中原子半径最小的元素,乙的气态氢化物的水溶液显碱性,丙是短周期元素中原子半径最大的元素,丁是地壳中含量最多的金属元素。
(1)写出四种元素的名称:甲______,乙______,丙______,丁______。
(2)乙、丙、丁三种元素的原子半径从大到小的顺序是________(填元素符号,下同)![]() ________
________![]() ________。
________。
(3)写出乙、丙、丁的最高价氧化物对应的水化物相互反应的化学方程式:__________________、__________________、__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组有机化合物中,不论两者以什么比例混合,只要总物质的量一定,则完全燃烧时消耗氧气的质量不变的是( )
A.CH4O,C3H4O5,C2H4O2B.C3H6,C3H8O,C4H8O3
C.C3H8,C4H6,C4H8OD.C2H6,C4H6O,C3H8O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
①离子化合物中一定有离子键,一定没有共价键
②NaHSO4固体中阳离子和阴离子的个数比是1:1
③共价化合物中不含离子键,一定只含共价键
④稳定性:H2O>H2S,沸点:H2O<H2S
⑤NaCl和HCl溶于水破坏相同的作用力
⑥非极性键可能存在于非金属单质中,也可能存在于离子化合物或共价化合物中
A.①②⑥B.①③④⑥C.②③⑥D.①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物与人类生产、生活息息相关。回答下列问题:
(1)氮的氢化物之一肼(N2H4)是一种油状液体,常做火箭燃料,与水任意比互溶,并且沸点高达113℃。在肼分子中N原子的杂化方式是___,肼易溶于水的原因是___,肼的沸点高达113℃的原因是___。
(2)N2F2是氮的氟化物之一,lmol N2F2中含有___mol ![]() 键;N和F中电负性较大的是____。
键;N和F中电负性较大的是____。
(3)氮与钠形成的化合物有Na3N和NaN3。
①Na3N能与水剧烈反应生成NaOH和NH3,则Na3N属于___晶体。
②NaN3用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。反应原理为2NaN3+CuO![]() Na2O+2Cu+3N2↑。写出两种与
Na2O+2Cu+3N2↑。写出两种与![]() 互为等电子体的分子或离子:___(填化学式)。
互为等电子体的分子或离子:___(填化学式)。
(4)Na2O的晶胞结构如图所示,晶胞边长为566pm,晶胞中氧原子的配位数为___,Na2O晶体的密度为___g·cm3(只要求列算式,不必计算出结果) 。
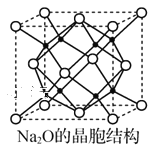
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HPE是合成苯氧基丙酸类除草剂的重要中间体,其合成路线如下:
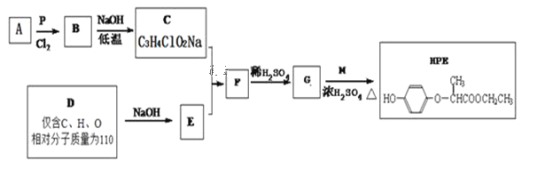
已知:①RCH2COOH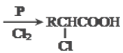
②![]() +RCl
+RCl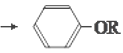 +NaCl
+NaCl
据此回答下列问题:
(1)B中含有的官能团名称为___,D的结构简式为___。
(2)C + E →F的反应类型为___。
(3)M的核磁共振氢谱中各吸收峰的面积之比为___。
(4)写出G+M→HPE的化学方程式___。
(5)X是G的同分异构体,其中满足以下条件的X共有___种,写出其中的任意三种X的结构简式___。
A.苯环上有3个取代基且苯环上的一氯取代物有两种
B.遇FeCl3溶液发生颜色反应
C.X不能与NaHCO3反应产生CO2
D.1molX最多能和3molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即可产生电流,此装置称为甲烷燃料电池。下列叙述中正确的是( )
①通入CH4的电极为正极;
②正极的电极反应式为:O2+2H2O+4eˉ=4OHˉ;
③放电时溶液中的阳离子向正极移动;
④负极的电极反应式为:CH4+10OHˉ-8eˉ=![]() +7H2O;
+7H2O;
⑤电子迁移方向:通入CH4的铂电极→通入O2的铂电极→电解质溶液→通入CH4的铂电极
A.①③⑤B.②③④C.②④⑤D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如右图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。请回答下列问题:
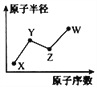
(1)写出四种元素的元素符号:X____ Y____ Z____ W____
(2)HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确___,说明理由__________________________________。
(3)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有漂白消毒杀菌作用,其化学式为________;化合物乙是一种常见的强酸,会因保存不当而变成黄色液体,其原因是_______________________________。把红热的木炭投入黄色液体,剧烈反应,方程式为_____________________,将产生的气体通过澄清石灰水时气体变为无色,但未见有浑浊现象,原因是______________。(写出有关反应的化学方程式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某化学反应A2(g)+2B2(g)=2AB2(g)(AB2的分子结构为B—A—B)的能量变化如图所示,下列有关叙述中正确的是( )
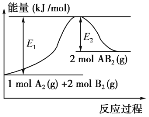
A.该反应的进行一定需要加热
B.该反应的ΔH=-(E1-E2)kJ/mol
C.该反应为吸热反应
D.断裂1molA—A键和2molB—B键放出E1kJ能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com