
����Ŀ����ˮ����þΪ��ɫ��ĩ���׳��⣬������ˮ���۵�323��������ʱͬʱ�ֽ⣬������ϩ���ۺϴ������Ʊ��������¡�
�Ʒ�һ����80%������ˮϡ�ͺ�ˮԡ������60~ 80�����ڽ����·�����������̼��þ��CO2�����ݳ�Ϊֹ���������ȣ����ȹ��ˡ�����Һ�в����������ᣬ���������������õ���ˮ����þ���壬������������������ˮ����þ
(1)̼��þ������������룬������____________________��
(2)��Һ�в������������Ŀ����_____________________��
(3)�������ṩ�IJ�����ѡ���Ҫ�IJ��������ظ�ʹ�ã������Ʒ�һ�С����������IJ��貹����������ȷ��˳���� _________��_______�� �����ţ�
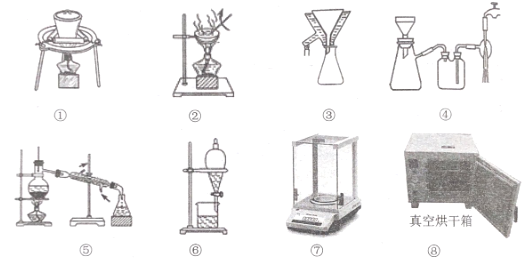
�Ʒ��� ������ˮ����þ���������ϼ��ȣ�������Ӧ�������岽����ȥ��
2Mg(NO3)26H2O+ 14(CH3CO )2O![]() 2Mg(CH3COO )2+ 4NO 2��+ O2��+24CH3COOH
2Mg(CH3COO )2+ 4NO 2��+ O2��+24CH3COOH
(4)����ˮ����þ������ˮ����þ����ͬ���������Ʊ�ʵ�飬���õ���Ʒ��ԭ���� __________________��
(5)�Ը���T��BET)Ϊָʾ�� ���� EDTA�ⶨMg2+������ԭ���÷���ʽ�ɱ�ʾΪ��
EDTA (��ɫ��+Mg-BET (�Ϻ죩= BET (��ɫ��+ Mg-EDTA (��ɫ��
Ϊ�ⶨ��Ʒ���ȣ���ȡ����0.3000 g ����ƿ�У�����100ml ����ˮ������ȫ�ܽ�����l 0mLpH=l 0�İ�-�Ȼ���������Һ����Һ����ǣ��ٵμ�3~ 4 �θ��� T ָʾ�� (BET),��0. l 000molL-1 �� EDTA����Һ�ζ����յ㣬�ظ�������������ƽ������ EDTA ����Һ 20.50mL��
�ٵζ��յ������Ϊ_______________ ��
�ڲ�Ʒ��þԪ�ص���������Ϊ________��������λ��Ч���֣���
(6)���й��ڸ�ʵ��IJ�������� ����ȷ����__________�����ţ���
A. ������������Һ�����ת��������©���н��г���ʱ����ת����Һ��ת�Ƴ���
B. ��ȡһ�������IJ�Ʒʱ����������ƽδ����ˮƽ����ƵõIJ�Ʒƫ��
C. ��ʼ�ζ�ǰ���ζ��ܼ����ҵ�Һ�����ȥ���������������ƫ��
D. ����(5)�IJⶨ������֪��Mg(OH)2������EDTA��Һ
���𰸡����̼��þ�������ʣ���ֹ���ɸ����� Mg(HCO3)2 �����ڲ�Ʒ�ķ�����ᴿ ���� Mg2+ˮ�⣬��ֹ���� Mg(OH)2 �ڢ� ��ߢ�� ����þ�������ᣩ���ȶ����ѷֽ� ���������һ�α���Һ����Һ���Ϻ�ɫ��Ϊ��ɫ���Ұ�����ڲ��ٷ����仯 16.40% ABCD
��������
�Ʒ�һ��(1)̼�������ᷴӦ������̼�����Σ����Ͳ�Ʒ�IJ��ʣ�
(2) Mg2+��ˮ������������þ��
(3)�Ʒ�һ�������������IJ�����ݴ���þ�����ʣ��������ᾧ����ˮ�ֺ�ɲ������������أ�
�Ʒ�����(4)���������ε������ȶ����ֽ�������
(5)�ٸ��ݵζ�ԭ������ʽ�����ʵ���ɫ�仯�жϷ�����
�ڽ�ϵζ����ݣ����ݷ���ʽ����þ��������������������������
(6)A��������������Һ�����ת��������©���н��г���ʱ�����ò�����ת����Һ����ת�Ƴ���
B������Ҫ��ֱ�ڴ������ܸˡ������ˮƽ�������ʹ������мнǣ��ͻ��з�����
C����ʼ�ζ�ǰ���ζ��ܼ����ҵ�Һ�Σ����µζ�ʱ��õı�Һ���ƫ�ͣ�
D������(5)�IJⶨԭ����Mg2+��BET��ת����EDTA��
�Ʒ�һ��(1)̼�������ᷴӦ������̼�����Σ����Ͳ�Ʒ�IJ��ʣ��ʷ�����������̼��þ��ԭ�������̼��þ�������ʣ���ֹ���ɸ����� Mg(HCO3)2 �����ڲ�Ʒ�ķ�����ᴿ��
(2) Mg2+��ˮ������������þ������������������� Mg2+ˮ�⣬��ֹ���� Mg(OH)2��
(3)�Ʒ�һ�������������IJ�����ݴ���þ�����ʣ�������ˮ�������ֽ⣬����������ᾧ��ʹ�ó��˵ķ����������ˮ��ȥ���õ�����þ���壬���ú���佫�ᾧˮ��ɲ�����������������ν��к�ɳ������������أ��ʴ�Ϊ�ڢ�����ߢ����
�Ʒ�����(4)����þ(������)Ҫ�������λ�����θ��ȶ����ѷֽ⣬������ˮ����þ������ˮ����þ����ͬ���������Ʊ�ʵ�飬�õ���������þ�����õ�����þ��
(5)�ٸ��ݵζ�ԭ������ʽ��EDTA (��ɫ)+Mg-BET (�Ϻ�)= BET (��ɫ)+ Mg-EDTA (��ɫ)���ζ�ǰ��ҺΪ�Ϻ�ɫ���ζ���Ϊ��ɫ������ж��յ������Ϊ���������һ�α���Һ����Һ���Ϻ�ɫ��Ϊ��ɫ���Ұ�����ڲ��ٷ����仯����Ϊ�ﵽ�ζ��յ㣻
�ڸ��ݵζ�ԭ������ʽ��EDTA (��ɫ)+Mg-BET (�Ϻ�)= BET (��ɫ)+ Mg-EDTA (��ɫ)���ζ��յ��þԪ��ת����EDTA�У�����þԪ���غ㣬þԪ�ص����ʵ���=EDTA�����ʵ���=0.0205L��0. l 000molL-1=0.00205mol�����Ʒ��þԪ�ص���������Ϊ![]() ��100%=16.40%��
��100%=16.40%��
(6)A��������������Һ�����ת��������©���н��г���ʱ�����ò�������©����ת����Һ��ת�Ƴ�������A��ȷ��
B����ȡһ�������IJ�Ʒʱ����������ƽδ����ˮƽ�����������ʹ������мнǣ��ͻ��з�����������ƽ��ʾ����ֵ������һ����������ֵ�����³���������ƫ��B��ȷ��
C����ʼ�ζ�ǰ���ζ��ܼ����ҵ�Һ�Σ����µζ�ʱ��õı�Һ���ƫ�ͣ�����c��=![]() ��������ƫ�ͣ���C��ȷ��
��������ƫ�ͣ���C��ȷ��
D������(5)�IJⶨԭ����MgԪ����BET��ת����EDTA��˵��Mg(OH)2������EDTA��Һ����D��ȷ��
��ѡABCD��


 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������վ�������Ag2S����ڣ��ɽ������´����������淢�ڵ���������ʢ��ʳ��ˮ������������(��ͼ)��һ��ʱ����ɫ��ȥ���ش��������⣺
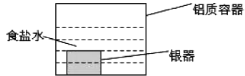
(1)���������վñ������ڣ�����������Ag2S��Ե�ʣ�����������__________��ʴ(���ѧ���绯ѧ��)��
(2)����������Ϊ__________���������ĵ缫��ӦʽΪ____________��
(3)�����������ܷ�Ӧ�Ļ�ѧ����ʽΪ_______________��
(4)�������������е�ʳ��ˮ��Ũ������棬�������������ĵ缫��ӦʽΪ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��L��X��Y��Z��W��ԭ���������ε���������ֻ��һ�ֽ���Ԫ�أ� L��Y��X��Z�ֱ�ͬ���壬��X��Y��Z����Ԫ���γɵĻ�����M�ṹ��ͼ��ʾ���ڹ�ҵ������Ư���ȡ�����������ȷ���� ( )

A.�����Ӱ뾶��Z>W>Y>X>L
B.������M������������
C.Z��W���������Ӧ��ˮ�����Ϊǿ��
D.X��Z��W�ɷֱ���Y�γɺ��зǼ��Թ��ۼ��Ķ�Ԫ���ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����˵����ȷ����
A.pH ��ȵ�����ʹ��ᣬ��ˮϡ����ͬ������c(Cl-)=c(CH3COO- )
B.0.l molL-1 ��ˮ��p H= a�������������Ȼ�粒����ʹ��ҺpH= a+ l
C.���ʵ���Ũ����ȵ� (NH4)2SO4 ��Һ��(NH4) 2CO3��Һ�У� ǰ�ߴ��ں���
ǰ�ߴ��ں���
D.�����ʵ���Ũ�ȵ�����Ĵ�����Һ���������Һ���������������Ʒ�Ӧ���ų����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ծ�Ԥ�����ķϾ���������﮵缫����Ҫ�ɷ�ΪLiFePO4�� Al��C)Ϊԭ�ϣ�����Li2CO3 �IJ��ֹ����������£�
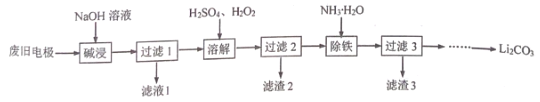
��֪��LiFePO4������ˮ�ͼ�����Һ��������������Һ��Li2CO3����ϡ�ᣬ����ˮ������˵������ȷ����
A.����2����Ҫ�ɷ�ΪC
B.�ܽ�ʱ������Ӧ�����ӷ�Ӧ����ʽ��2LiFePO4+2H++H2O2=2Li++2Fe3++ 2![]() + 2H2O
+ 2H2O
C.�����3����Һ�м��뱥��Na2CO3��Һ��������Li2CO3����
D.��֪��Li2CO3��FePO4x H2O��H2C2O4 ��Ϸ�Ӧ�����»��LiFePO4����������ȫ��Ӧ���ĵ�n(Li2CO3):n(FePO4x H2O):n(H2C2O4)=1:2:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(V2O5)Ϊǿ���������ױ���ԭ�ɸ��ֵͼ�������ڹ�ҵ�����г���������������ý��ʵ�����Ժ�������(��V2O3��CuO��MnO��SiO2��Al2O3���л���)Ϊԭ���Ʊ�V2O5��һ��������ͼ��
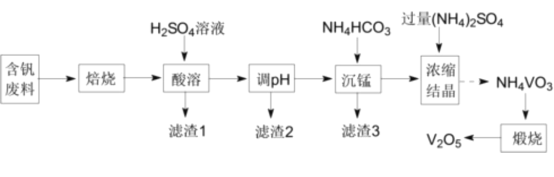
��֪I.25��ʱ�����ܵ���ʵ��ܶȻ����������ʾ��
II.NH4VO3��ˮ�е��ܽ�ȣ�20�桢4.8g��L-1��60�桢24.2g��L-1��
�ش��������⣺
��1������������Ŀ����__��
��2��������1������;Ϊ__(д��һ�ּ���)��
��3������2�ɷ�Ϊ__��ͨ����ʽ����˵���������£�������pH��Ϊ6��Cu2+�Ƿ������ȫ__��(��Һ������Ũ��С��10-5mol��L-1ʱ����Ϊ�����ӳ�����ȫ)
��4�����������轫�¶ȿ�����70��C���ң��¶Ȳ��ܹ�����͵�ԭ��Ϊ___��
��5������3�ɷ�ΪMnCO3����д���������������ӷ���ʽ__��
��6��V2O5����Ҫ��Ӧ�����ڽӴ���������ʱ����SO2����ΪSO3�Ĵ������ô���Ӧ��VO2Ϊ�м������û�ѧ����ʽ��ʾ�ô����̣�__��__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ʺ�����һ����Դ�������ӵ��ڼ�������������ʳ���е�ɫ����ת���õ�

����˵������ȷ����
A.ɫ��������д��ڰ�������Ȼ������γ����Σ����нϸߵ��۵�
B.��ɫ����ˮ��Һ�У���ͨ��������Һ��pHʹ���γɾ�������
C.��һ�������£�ɫ����ɷ������۷�Ӧ
D.�ʺ�����ɫ����ṹ���ƣ�Ҳ�������Ի����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ�������ֵ������˵���У�����ȷ����(����)
A.һ�������£�2.3 g Na��O2��ȫ��Ӧ����3.6 g����ʱʧȥ�ĵ�����0.1NA
B.��⾫��ͭʱ������·��ת��NA�����ӣ������ܽ�32 gͭ
C.�����0.2 mol FeI2����Һ�г���ͨ������������0.1 mol Fe2��������ʱ��ת�Ƶ��ӵ���ĿΪ0.5NA
D.��״���£�п��ijŨ�ȵ�H2SO4��Ӧ����11.2 L���壬��Ӧ��ת�Ƶĵ�����Ϊ6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ȼ����±���������ķ�Ӧ��ͼ��ʾ��(��С���Ӳ�����ȥ)������˵����ȷ����

A. �÷�Ӧ���ڻ��Ϸ�Ӧ
B. b�Ķ��ȴ�����6�ֽṹ
C. 1mol b�������ɱ�������Ҫ6molH2
D. C5H11Cl�Ľṹ��8��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com