
����Ŀ����ͼA��B��C�����ձ��зֱ�ʢ����ͬ���ʵ���Ũ�ȵ�ϡ���ᡣ
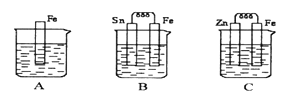
��1��A�з�Ӧ�����ӷ���ʽΪ____________��B��Sn����������ֵ�����_________________��C��ZnƬ�ϵĵĵ缫��ӦʽΪ________������__________��Ӧ���������Ӧ����ԭ��Ӧ������
��2��A��B��C�����ܽ�������ɿ쵽����˳����_________________ ��
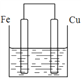
��3������������ȵ���Ƭ��ͭƬ�õ���������������ͭ��Һ�й���ԭ��أ���ͼ��������_________����������Ԫ�ط��ţ���һ��ʱ������缫�������1.2g��������ͨ���ĵ��ӵ����ʵ���Ϊ______mol��
���𰸡� Fe��2H �� =Fe 2�� ��H 2 �� �����ݲ��� Zn - 2e ��= Zn 2�� ������Ӧ B ��A��C Fe 0.02mol
��������(1)�������ᷴӦ�����ӷ���ʽΪ��Fe+2H+=Fe2++H2����B�����������ã���Ϊԭ����������缫��ӦʽΪ��2H++2e-=H2���������ݲ�����C��п�������ã�пΪԭ��ظ���������������Ӧ�������缫��ӦʽΪZn-2e-=Zn2+���ʴ�Ϊ��Fe+2H+=Fe2++H2���������ݲ�����Zn-2e-=Zn2+��������Ӧ��
(2)A������ѧ��ʴ��B��FeΪ������SnΪ������Fe����ʴ��C��ZnΪ������FeΪ������Fe����������A��B��C��������ʴ�����ʣ��ɿ쵽����˳����B��A��C���ʴ�Ϊ��B��A��C��
(3)����ͭ���ã���Ϊԭ��صĸ��������ӴӸ�����������ת��xmol���ӣ�������0.5xmolFe������0.5xmolCu������0.5x��(64+56)=1.2��x=0.02���ʴ�Ϊ��Fe��0.02mol��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�����������˵����ȷ������ ��
A����״���£�5.6L CCl4���еķ�����Ϊ0.25NA
B����״���£�14 g�������еĺ��������Ϊ5NA
C����״���£�22.4 L����ȵ������������Ļ����к��з���������ΪNA
D���ڱ�״���£�18gH2O�����еĵ���������10NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[2015�㶫]��ѧ��������ѧ��������ѧ���������������˵����ȷ����
A��ľ����ά��������������ˮ������ɫ
B��ʳ�û����ͺͼ����嶼�ܷ���ˮ�ⷴӦ
C����װ�ò��Ͼ���ϩ�;�����ϩ��������
D��PX��Ŀ����Ҫ��Ʒ�Զ��ױ����ڱ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�ͼ�DZ�ʾ��Ӧ�仯��������ϵͼ��������ȷ���ǣ� ��
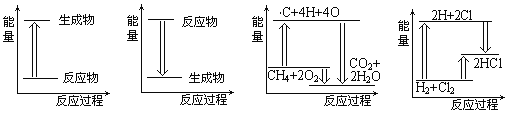
A. п��ϡ����ķ�Ӧ B. ֲ��Ĺ������ C. ��Ȼ��ȼ�� D. H2��Cl2��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��ƻ�������������������ȡ��������Һ���䷴Ӧԭ��Ϊ�������ӷ���ʽ��ʾ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ��������Ũ�����������ط�Ӧ����ȡ��������������Ӧ�Ļ�ѧ����ʽΪ��2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O����Ӧ���У��������������ϼ����ߵ�Ԫ���� �� ��Ӧ��HCl�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ʺ�����һ����Դ�������ӵ��ڼ�������������ʳ���е�ɫ����ת���õ���
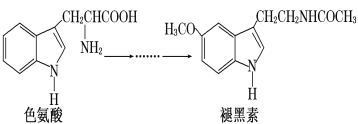
����˵������ȷ����
A��ɫ��������д��ڰ������Ȼ������γ����Σ����нϸߵ��۵�
B����ɫ����ˮ��Һ�У���ͨ��������Һ�� pH ʹ���γɾ�������
C���ʺ�����ɫ����ṹ���ƣ�Ҳ�������Ի������������Ӧ
D����һ�������£�ɫ����ɷ������۷�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ���ܸ�AB���˷ֱ���������ͬ��������ȵĿ���ͭ��Ϳ��������ڸܸ˲�ʹ�䱣��ƽ�⣬Ȼ��С�ĵ���ˮ���е���ŨCuSO4��Һ��һ��ʱ��������йظܸ˵�ƫ���ж���ȷ����(ʵ������У�����������ĸ����仯)(����)

A. �ܸ�Ϊ������Ե��ʱ����ΪA�˸�B�˵�
B. �ܸ�Ϊ������Ե��ʱ����ΪA�˵�B�˸�
C. ���ܸ�Ϊ����ʱ��A�˵�B�˸�
D. ���ܸ�Ϊ����ʱ��A�˸�B�˵�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����t��Cʱ��AgBr��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��CʱAgCl��Ksp=4��10-10������˵������ȷ����( )
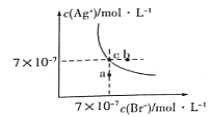
A��ͼ��a���Ӧ����AgBr�IJ�������Һ
B����t ��Cʱ��AgBr��KspΪ 4.9��10-13
C����AgBr������Һ�м���NaBr���壬��ʹ��Һ��c�㵽b��
D����t ��Cʱ��AgCl(s)+Br-(aq)![]() AgBr(s)+C1- (aq)��ƽ�ⳣ��K��816
AgBr(s)+C1- (aq)��ƽ�ⳣ��K��816
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com