
【题目】选择性催化还原是在有催化剂的条件下将NOx转变为N2和H2O,这是目前国外硝酸厂进行尾气治理普遍采用的一种方法,某小组同学拟验证NO能被氨气还原并测算其转化率。
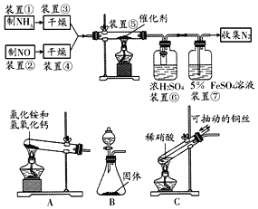
请回答下列问题:
(1)若制取氨气用A装置,则发生反应的化学方程式为_______,若用B装置制取氨气,则分液漏斗和锥形瓶中盛放的药品分别是______、________;
(2)用C装置制取NO时,用可抽动的铜丝,其优点是_______,其反应的离子方程式为________;
(3)装置⑦的作用可能是____________;
(4)若进入装置⑤的NO共2688mL(标况下),氨气过量,最后收集到标况下2016mLN2,则NO的转化率为___。
【答案】2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 浓氨水 碱石灰 反应可以随时关停、操作方便、反复使用、节约药品 3Cu+8H++2 NO3- =3Cu2++2NO↑+4H2O 吸收未反应的NO 90%
CaCl2+2NH3↑+2H2O 浓氨水 碱石灰 反应可以随时关停、操作方便、反复使用、节约药品 3Cu+8H++2 NO3- =3Cu2++2NO↑+4H2O 吸收未反应的NO 90%
【解析】
在加热条件下,实验室通常用氯化铵和氢氧化钙反应制备氨气;若要制备少量氨气,可利用氨气的挥发性和碱石灰的吸水性来制取。结合氨气和NO的性质分析解答。
(1) 在加热条件下,实验室通常用氯化铵和氢氧化钙反应制备氨气,生成氨气、氯化钙和水,发生反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;若制取氨气用不加热装置,则分液漏斗和锥形瓶中盛放的药品分别是浓氨水、碱石灰或生石灰或氢氧化钠;
CaCl2+2NH3↑+2H2O;若制取氨气用不加热装置,则分液漏斗和锥形瓶中盛放的药品分别是浓氨水、碱石灰或生石灰或氢氧化钠;
(2) 制取NO时用可抽动的铜丝,其优点是易于控制反应,操作简便并能节约药品,答案为:反应可以随时关停、操作方便、反复使用、节约药品;铜与稀硝酸发生氧化还原反应生成硝酸铜、一氧化氮和水,其反应的离子方程式为3Cu+8H++2 NO3- =3Cu2++2NO↑+4H2O;
(3) 硫酸亚铁具有还原性,一氧化氮与二价铁发生反应,故装置⑦的作用可能是吸收未反应的NO;
(4) 根据反应6NO+4NH3═5N2+6H2O计算,在一定条件下气体的体积之比等于物质的量之比,
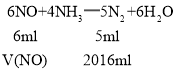
V(NO)=2419.2ml,则NO的转化率为![]() ,答案为90%。
,答案为90%。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】某同学取一定量淀粉进行水解实验,其实验步骤如下所示:
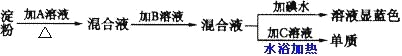
请回答下列问题:
① 所加入的试剂分别是
A_______,B________,C________;
② 加B的原因是_____________________________________________________;
③由此可知淀粉是________(填“部分”、“完全”或“没有”)水解。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置),反应原理为:H3PO4(浓)+NaBr![]() +NaH2PO4+HBr,CH3CH2OH+HBr
+NaH2PO4+HBr,CH3CH2OH+HBr![]() CH3CH2Br+H2O, 有关数据见下表:
CH3CH2Br+H2O, 有关数据见下表:
物质名称 | 乙醇 | 溴乙烷 | 溴 |
状态 | 无色液体 | 无色液体 | 深红棕色液体 |
密度/gcm-3 | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
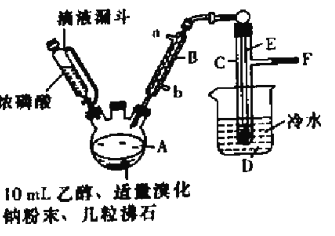
(1)A中加入沸石的作用是______________________.
(2)仪器B的名称为____________,该仪器的进水口为_______(填“a”或“b”)口.
(3)实验中用滴液漏斗代替分液漏斗的优点为_________________
(4)制取氢溴酸时,为什么不能用浓H2SO4代替浓磷酸?_________(用化学方程式表示).
(5)将C中的馏出液转入锥形瓶中,边振荡边逐滴滴入浓H2SO4以除去水等杂质,滴加浓硫酸约1~2mL,使溶液明显分层,再用分液漏斗分去硫酸层,将经硫酸处理后的溴乙烷转入蒸馏瓶,水浴加热蒸馏,收集到35~40℃馏分约10.0g,从乙醇的角度考虑,本实验所得溴乙烷的产率是______(保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1mol H2完全燃烧生成水蒸气放出热量242kJ,且H2中1mol H-H键断裂时吸收热量436kJ,水蒸气中形成1mol H-O键时放出热量463 kJ,则O2中1mol O=O键断裂时吸收的热量为
A.556 kJB.496 kJC.336 kJD.188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烧碱样品含有少量不与酸作用的杂质,为了滴定其纯度,进行以下滴定操作:
A.在天平上准确称取烧碱样品10g,在烧杯中用蒸馏水溶解
B.用移液管(或碱式滴定管)量取25mL烧碱溶液于锥形瓶中滴加几滴酚酞作指示剂
C.在1000mL的容量瓶中配制1000mL烧碱溶液
D.将物质的量浓度为0.5 mol/L的标准硫酸溶液装入酸式滴定管,调整液面记下开始读数为V1mL
E.在锥形瓶下一张白纸,滴定至红色刚好消失为止,记下读数V2mL
回答下列问题:
(1)正确操作步骤的顺序是(填字母): → → → → E。__
(2)滴定前俯视或滴定后仰视 _____ 滴定接近终点时,有少量蒸馏水冲洗锥形瓶内壁 _____(填“偏高”、“偏低”或“无影响”)
(3)操作E中的锥形瓶下垫一张白纸的作用是___________________________。
(4)开始时标准液在滴定管刻度线以上,未予调整 ____(填“偏高”“偏低”或“无影响”)
(5)滴定前滴定管尖嘴有气泡,滴定后尖嘴气泡消失______未用标准液润洗滴定管_____(填“偏高”、“偏低”或“无影响”)
(6)该烧碱样品纯度为: ____________ 。(样品中烧碱的质量/样品的质量×100%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】马日夫盐![]() 用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为
用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为![]() 及少量的FeO、
及少量的FeO、![]() 和
和![]() )为原料制备马日夫盐的主要工艺流程如图:
)为原料制备马日夫盐的主要工艺流程如图:
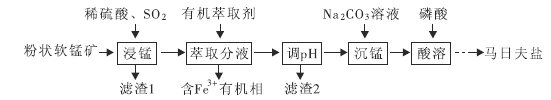
(1)“浸锰”过程中,FeO参与氧化还原反应的离子方程式为_______________。
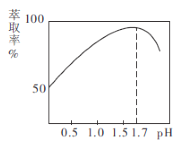
(2)![]() 的萃取率与溶液的pH的关系如图所示,当
的萃取率与溶液的pH的关系如图所示,当![]() 时,
时,![]() 的萃取率急剧下降的原因可能为_______________(用化学用语表示)。
的萃取率急剧下降的原因可能为_______________(用化学用语表示)。
(3)“调pH”的最大范围为________。
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| l. 8 | 3.2 |
| 3.0 | 5.0 |
| 5.8 | 8.8 |
| 7.8 | 9.8 |
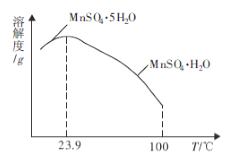
(4)如图为硫酸锰水合物的溶解度曲线,若要用“调pH”所得滤液制备![]() ,需要控制温度在80℃~90℃之间的原因是_____,采用水浴加热,经蒸发浓缩、_____(填操作名称)、用80℃~90℃的蒸馏水洗涤2~3次,放在真空干燥箱中低温干燥获得。
,需要控制温度在80℃~90℃之间的原因是_____,采用水浴加热,经蒸发浓缩、_____(填操作名称)、用80℃~90℃的蒸馏水洗涤2~3次,放在真空干燥箱中低温干燥获得。
(5)写出检验“沉锰”是否已完成的实验操作_________。
(6)常温下,马日夫盐溶液显________性(填“酸”或“碱”),理由是:____________。(写出计算过程并结合必要的文字说明。已知:![]() 的电离常数
的电离常数![]() ,
,![]() ,
,![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,容积不变的容器里,对可逆反应A(g) ![]() 2B(g) +3C(g)的叙述中,能说明反应已达到平衡的是
2B(g) +3C(g)的叙述中,能说明反应已达到平衡的是
A.混合气体的物质的量不再变化B.单位时间消耗a mol A, 同时生成3a molC
C.容器内的气体总质量不再变化D.C生成的速率与B分解的速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 按系统命名法, ![]() 的名称为2,6二甲基5乙基庚烷
的名称为2,6二甲基5乙基庚烷
B. 丙氨酸和甘氨酸脱水,最多可生成4种二肽
C. 化合物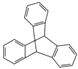 是芳香族化合物
是芳香族化合物
D. 三硝酸甘油酯的分子式为C3H5N3O9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com