
【题目】元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列字母A、D、F、G、Q、M、R、N、T分别代表某种化学元素。请依据这9种元素回答下列问题。
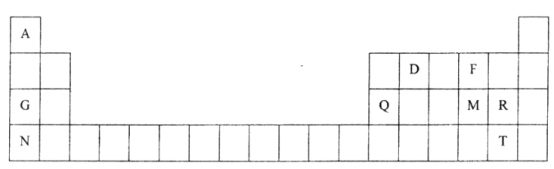
(1)以上9种元素中金属性最强的元素是_______(填元素符号)。
(2)元素的非金属性:M______R(填“>”或“<”)。
(3)R的最高价氧化物对应水化物的化学式是_____________。
(4)F、G两元素形成的淡黄色固体物质的电子式为_____________。
(5)表中M、R、N元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是_____________(用离子符号表示)。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】材料的应用推动了城市发展,很多方面涉及到了化学反应,认真回答下列问题:
(1)我国早在春秋战国就开始生产和使用铁器,写出用赤铁矿为原料炼铁的化学方程式:___________________。
(2)氢氧化钾是我国古代纺织业常用的漂洗洗涤剂,古人将贝壳(主要成分是碳酸钙)灼烧后的固体与草木灰(主要成分是碳酸钾)在水中相互作用,便可得到氢氧化钾。请按要求用化学方程式表示上述反应:分解反应:___________,化合反应:_____________,复分解反应:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能体现乙酸酸性的是( )
A.乙酸滴入碳酸钠溶液中会出现气泡
B.乙酸中滴加几滴石蕊溶液呈红色
C.乙酸和水能以任意比例互溶
D.长时间使用的热水瓶胆可以用乙酸来洗去水垢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,平衡pH随溶液体积变化的曲线如图所示。据图判断正确的是
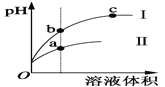
A. Ⅱ为盐酸稀释时pH变化曲线
B. b点溶液的导电性比c点溶液的导电性弱
C. a点KW的值比c点KW的值大
D. 与相同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积,a点比b点大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的说法中正确的是
A.同一主族元素的原子序数的差不可能为10
B.同周期第ⅡA族与第ⅢA族元素的原子序数差值一定是1
C.催化剂一般在金属与非金属的分界线处寻找
D.过渡元素全部是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组在实验室使用软锰矿(主要成分为MnO2)和浓盐酸通过加热制备氧气,并对氯气的性质进行探究。
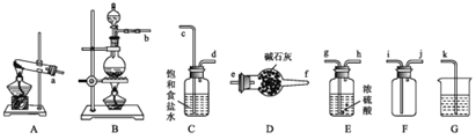
(1)写出实验室制氯气的化学方程式________。欲制取并收集一瓶干燥的氯气,则“制取→收集”的实验装置连接顺序为:____→c→d→_____→i→j→k
(2)装置C中饱和食盐水的作用是______________。
(3)该小组同学对氯气性质进行如下探究:
实验步骤 | 实验结论 |
①将氯气通入到NaCl溶液中,再加入1mL CCl4振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序: 氯、溴、碘 |
②将氯气通入到KBr溶液中,再加入1mL CCl4振荡,静置,观察四氯化碳层颜色 | |
③将氯气通入到KI溶液中,再加入1mL CCl4振荡,静置,观察四氧化碳层颜色 |
该小组的实验设计缺陷是___________,改进的办法是________________。
(4)常温下,高锰酸钾固体和浓盐酸反应也可制得氯气,该反应的离子方程式为______________。
(5)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3-的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的质量之比为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.液氨可用作制冷剂B.SO2使湿润的蓝色石蕊试纸变红
C.常温下可以用铁或铝制容器盛装浓硝酸或浓硫酸D.测定某雨水的pH值小于7.0可判断雨水为酸雨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胆矾是配制波尔多液的主要原料,常用在树木,花卉的保护上。
(1)基态铜原子的电子排布式为___________。
(2)乙烯氨氧化可以得到丙烯腈(CH2=CH-CN),丙烯腈中各元素的电负性由大到小顺序为____________,1mol丙烯腈分子中含有π键数目为_________。
(3)CN-与N2互为等电子体,写出CN-的电子式______________。
(4)通过X射线衍射发现,胆矾中存在SO42-离子,SO42-离子的VSEPR构型名称为___________,CO32-中心原子的杂化形式为________。
(5)硫酸铜灼烧可以生成一种红色晶体,其结构如图所示为体心立方晶胞,则该化合物的化学式是______;若该晶体中距离最近的铜原子与氧原子直接距离为acm,则晶体密度表达式为_____g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下如图,关闭活塞,在左右两室(体积相同)各充入一定量H2和Cl2,且恰好使两容器内气体密度相同,打开活塞,点燃使H2与Cl2充分反应生成氯化氢气体:H2+Cl2=2HCl,恢复到原温度后,下列判断正确的是

A. 开始时左右两室分子数相同
B. 最终容器内无H2存在
C. 反应前后H2室压强相同
D. 最终容器内密度与原来相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com