
| ��ѧʽ | �ܶȻ����� | ��ѧʽ | �ܶȻ����� |
| Ag2S | 6.3��10-50 | AgCl | 1.8��10-10 |
| CuS | 4.3��10-36 | AgBr | 5.4��10-13 |
| FeS | 6.3��10-18 | AgI | 8.3��10-17 |
| A����ȥ��ҵ��ˮ�е�Cu2+����ѡ��Na2S�������� |
| B����AgCl��AgBr��AgI������Һ�������Ϻ��ټ���������ŨAgNO3��Һ����������AgI���� |
| C��Ag2S��CuS��FeS�ܽ���������� |
| D����FeS�����Ũ��CuSO4��Һ�У�����CuS���� |
| Ksp |
| 4.3��10-36 |
| 3 |
| ||
| 3 |
| ||


 ������ϵ�д�
������ϵ�д� �±�Сѧ��Ԫ�Բ���ϵ�д�
�±�Сѧ��Ԫ�Բ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HD��NaOH�����ڻ����� |
| B��̼�ظ֡�����ֺ�Ŀǰ��ͨ��Ӳ�Ҷ����ںϽ� |
| C��Ũ���ᡢŨ���ᡢŨ���ᶼ������������ |
| D����ˮ�����ᡢ��������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
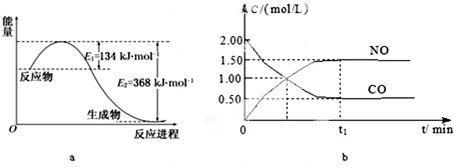
| �� �� | �� | �� | �� |
| ��Ӧ��Ͷ���� | 1mol NO2 1mol CO | 2mol NO 2mol CO2 | 1mol NO2��1mol CO 1mol NO��1mol CO2 |
| ƽ��ʱc��NO��/mol?L-1 | 1.5 | 3 | m |
| �����仯 | �ų�a kJ | ����b kJ | �ų�c kJ |
| CO��NO��ת���� | ��1 | ��2 | ��3 |
| b |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
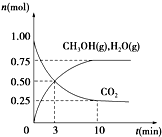 ��1����ѧ����H2��CO2�����״�ȼ�ϣ�Ϊ̽���÷�Ӧԭ������������ʵ�飺ij�¶��£����ݻ�Ϊ2L���ܱ������г���1mol CO2��3.25mol H2����һ�������·�Ӧ�����CO2��CH3OH��g����H2O��g�������ʵ�����n����ʱ��ı仯��ϵ��ͼ��ʾ��
��1����ѧ����H2��CO2�����״�ȼ�ϣ�Ϊ̽���÷�Ӧԭ������������ʵ�飺ij�¶��£����ݻ�Ϊ2L���ܱ������г���1mol CO2��3.25mol H2����һ�������·�Ӧ�����CO2��CH3OH��g����H2O��g�������ʵ�����n����ʱ��ı仯��ϵ��ͼ��ʾ��| ���� ��� | �¶ȣ��棩 | ��ʼ���ʵ�����mol�� | ƽ�����ʵ�����mol�� | |
| CH3OH��g�� | CH3OCH3��g�� | H2O��g�� | ||
| �� | 387 | 0.20 | 0.080 | 0.080 |
| �� | 387 | 0.40 | ||
| �� | 207 | 0.20 | 0.090 | 0.090 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2CH3CH2OH��l��+6O2��g���T4CO2��g��+6H2O��l����H=-1367 kJ/mol���ɼ��Ҵ�ȼ���ȡ�H=-1367 kJ/mol |
| B�����ȷ�Ӧ�ķ�Ӧ�������Ǵ������ȷ�Ӧ�ķ�Ӧ���� |
| C��Ӧ�ø�˹���ɣ��ɼ���ijЩ����ֱ�Ӳ����ķ�Ӧ�ʱ� |
| D��ͬ��ͬѹ�£�H2��g��+Cl2��g���T2HCl��g���ڹ��պ͵�ȼ�����µġ�H��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ij��Һ�еμ�AgNO3��Һ�а�ɫ������˵��ԭ��Һ����Cl- |
| B��ij��Һ���ȵμ����������������ٵμ�BaCl2��Һ�а�ɫ��������ԭ��Һ����SO42- |
| C��ij��ɫ��Һ�����̪��Һ�Ժ�ɫ������Һһ���Ǻ��д�����H+ |
| D��ij��Һ�еμ�ϡ����������ɫ���壬˵��ԭ��Һ����CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
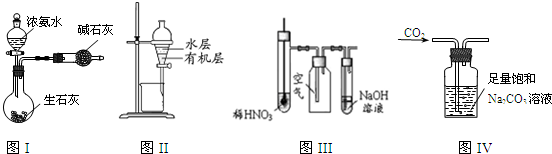
| A��ͼI��ʾװ����ȡ����İ��� |
| B��ͼ����ʾװ��������ȡI2��CCl4��Һ�е�I2 |
| C��ͼ����ʾװ����ϡHNO3���ڹ��ƿ�п��ռ�NO���� |
| D��ͼIV��ʾװ�ÿ����ڳ�ȥCO2�к��е�����HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��pH=1����Һ�У�Na+��K+��MnO4-��CO32- |
| B��0.1 mol/L NH4HCO3��Һ�У�K+��Na+��NO3-��Cl- |
| C��c��Fe3+��=0.1 mol/L����Һ�У�NH4+��Cl-��AlO2-��SO42- |
| D�������£�ˮ�������c��H+��=1��10-13mo1/L����Һ�У�Mg2+��K+��NO3-��Cl- |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com