
| A、某溶液中滴加AgNO3溶液有白色沉淀,说明原溶液中有Cl- |
| B、某溶液中先滴加足量盐酸无现象,再滴加BaCl2溶液有白色沉淀,则原溶液中有SO42- |
| C、某无色溶液滴入酚酞试液显红色,该溶液一定是含有大量的H+ |
| D、某溶液中滴加稀硫酸生成无色气体,说明原溶液中有CO32- |


 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
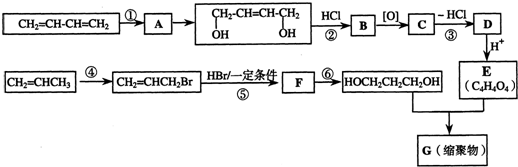
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | 溶度积常数 | 化学式 | 溶度积常数 |
| Ag2S | 6.3×10-50 | AgCl | 1.8×10-10 |
| CuS | 4.3×10-36 | AgBr | 5.4×10-13 |
| FeS | 6.3×10-18 | AgI | 8.3×10-17 |
| A、除去工业废水中的Cu2+可以选用Na2S作沉淀剂 |
| B、将AgCl、AgBr和AgI饱和溶液等体积混合后,再加入足量的浓AgNO3溶液,首先析出AgI沉淀 |
| C、Ag2S、CuS、FeS溶解度依次增大 |
| D、将FeS加入较浓的CuSO4溶液中,会有CuS生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熵变小于零而焓变大于零的反应肯定不能发生 |
| B、热化学方程式中△H的值与反应物的用量有关 |
| C、化学反应中旧键断裂吸收能量,新键形成释放能量,所以化学反应伴随能量变化,但反应前后物质的总能量不变 |
| D、用蒸馏水稀释0.1mol/L的醋酸至0.01mol/L,稀释过程中温度维持25℃不变,溶液中各离子浓度均减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、则此过程中参加反应的铁的质量是14g |
| B、析出铜物质的量是0.25mol |
| C、反应后溶液中溶质物质的量浓度:c(CuSO4)=1.5mol/L |
| D、反应后溶液中溶质物质的量浓度:c(FeSO4)=1.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在标准状况下22.4L H2O中含有氢原子的个数为2NA |
| B、2.7g 铝与足量的盐酸反应时失去的电子数为0.3NA |
| C、1mol/L NaCl溶液中含有钠离子的个数为NA |
| D、常温常压下,11.2 L氧气含有的原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、门捷列夫根据原子量排列的周期表成功预言了类铝(镓)、类硅(锗)等元素的存在 |
| B、铀(U)属于过渡元素,能跟氟形成UF6,据此可推测U原子最外层有6个电子 |
| C、HF、HCl、HBr、HI的还原性依次增强,热稳定性依次减弱,沸点依次升高 |
| D、Na、Mg、Al原子的最外层电子数依次增加,故失去电子的能力越来越强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com