
����Ŀ������������Ҫ��FeTiO3��Fe2O3��SiO2�Ȳ��������ʣ���ȡ��ƷλTiO2��һ����������ͼ��ʾ��

�ش��������⣺
��1���й��ѵ�˵����ȷ����_________������ĸ��ţ���
A��TiOSO4����Ԫ�صĻ��ϼ�Ϊ+4�� |
B��TiO2�мȺ������Ӽ����ֺ��й��ۼ� |
C����Ԫ��λ��Ԫ�����ڱ���IVA�� |
D����ϡ������벷�Χ��800�������£��ý���þ�����Ȼ��ѷ�Ӧ����ȡ�����ѡ� |
��Ӧ�Ļ�ѧ����ʽΪ![]()
��2��Ϊ�˴ӽ�ȡҺ�л�ȡ������FeSO4��7H2O��II��Ӧ��ȡ�IJ�����_________��_________�����ˡ�ϴ�ӡ������μ�����ȡFeSO4��7H2O����Һ�д���Fe2+_________��
��3��III������H2TiO3�����ӷ���ʽ��__________________��
��4����TiO2�뽹̿��ϣ�ͨ��������1173K�·�Ӧ��Ȼ�����ɵ�TiCl4��CO�������ȡTiCl4�� �˷�Ӧ�У��������뻹ԭ�����ʵ���֮����___________��TiCl4����ˮ�⣬���ô������ֿ��Ʊ�������������TiO2��XH2O���÷�Ӧ�Ļ�ѧ����ʽ��__________________��
��5����TiO2����NaF �Ƴ������Σ���ʯīΪ����������������Ĥ�Ķ�����մ�Ϳ��Ϊ����������ͼ��ʾ���װ����ȡ�����ѡ������缫��Ӧʽ��__________________

���𰸡�AD ����Ũ�� ��ȴ�ᾧ ȡ������Һ�����Թ��У�����Һ�м���KSCN��Һ����Һ�����ɫ���ټ���������ˮ����Һ���ɫ��˵��ԭ��Һ�д����������� TiO2++2H2O= H2TiO3��+2H+ 1:1 TiCl4+xH2O=TiO2��XH2O��+4HCl H2-2e-+O2-=H2O
��������
��1��A��TiOSO4�����������Ϊ-2�ۣ�OԪ��Ϊ-2�ۣ�������Ԫ��Ϊ+4�ۣ���ȷ��B��TiO2��ֻ�й��ۼ������Ӽ�������C����Ԫ��λ��Ԫ�����ڱ��ĵ������ڵ�IVB�壬����D��Mg��Ti���ã�Mg��������е�������������Ӧ��������ϡ������벷�Χ��800�������£��ý���þ�����Ȼ��ѷ�Ӧ����ȡ�����ѣ���ȷ����ѡAD��
��2������Һ�л�ȡ����IJ���Ϊ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����Ȳ��裻�����������ӵĴ��ڣ���������Һ�м���KSCN��Һ����Һ�����ɫ��˵���������Ӵ��ڣ��ټ���������ˮ����Һ���ɫ�����ʱ��Һ�д��������ӣ�˵��ԭ��Һ�д����������ӣ�
��3��TiO2+ˮ������H2TiO3�����ȴٽ�ˮ��������У����ɳ��������ӷ���ʽ��TiO2++2H2O= H2TiO3��+2H+;
��4���ڽ�̿���������������ѵķ�Ӧ�У�C�ǻ�ԭ������������������CԪ�صĻ��ϼ۴�0���ߵ�+2�ۣ�ʧȥ2�����ӣ�ClԪ�صĻ��ϼ۴�0���͵�-1�ۣ����彵��2�ۣ��õ�2�����ӣ����ϵ�ʧ�����غ㣬�����������뻹ԭ�������ʵ���֮����1:1��Ti4+ˮ������TiO2��XH2O�������ӣ���ѧ����ʽ��TiCl4+xH2O=TiO2��XH2O��+4HCl��
��5����������������Ӧ������ʧȥ�����������ӽ������ˮ���缫��Ӧʽ��H2-2e-+O2-=H2O��


 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���ѧ���з���һ�������¡��ɺ�������Na��CO2���ε�ء���NaClO4�����л��ܼ���Ϊ���Һ���ƺ���̼���ܵ������ֱ���Ϊ�缫���ϣ���ص��ܷ�ӦΪ��3CO2+4Na![]() 2Na2CO3+C������˵���������
2Na2CO3+C������˵���������

A. �ŵ�ʱ��ClO4�����ƶ�
B. ���ʱ�ͷ�CO2���ŵ�ʱ����CO2
C. �ŵ�ʱ��������ӦΪ��3CO2+4e ��2CO32��+C
D. ���ʱ��������ӦΪ��Na++e��Na
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ�����Ԫ��X��Y��Z�� W��Ԫ�����ڱ��е�λ������ͼ��ʾ�� ������������֮��Ϊ21������˵������ȷ����
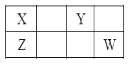
A. ����W���ɺ�ˮ��ԭ�ϻ��
B. Y �ķǽ����Ա� X��ǿ������Y���⻯��һ���� X�ĸ��ȶ�
C. ��ҵ�ϳ����õ��� X�뺬 Z������Ŀ�ʯ�ڸ����·�Ӧ�Ʊ��ߴ� Z
D. X���⻯������� W�ĵ��ʷ�����Ӧ�����Dz����� W ���⻯�����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�д������������������ӣ�![]() ��M�������ʵ���Ũ��֮��Ϊ
��M�������ʵ���Ũ��֮��Ϊ![]() =2��3��1��3��1����M������
=2��3��1��3��1����M������
A.Ba2+B.Na+C.I-D.Mg2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����ͬ�����pH��NaX��NaY��NaZ��������Һ���ֱ��ˮϡ�ͣ���ҺpH�ı仯������ˮ�������ϵ����ͼ��ʾ������˵����ȷ��( )

A.��ͼ��֪�����������Ϊ��HX<HY<HZ
B.�ڵ����ʵ���Ũ�ȵ�NaX��HX�����Һ�д��ڣ�c(H+)-c(OH-)=c(X-)-c(HX)
C.Ũ�Ⱦ�Ϊ0.1mol/L��NaX��NaY��NaZ�Ļ����Һ�У�![]()
D.��pH���NaX��NaY����Һ�д��ڣ�c(HX)+c(X-)=c(HY)+c(Y-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С�鰴����·�ߺϳ�ҩ�ﰱ³���ء�
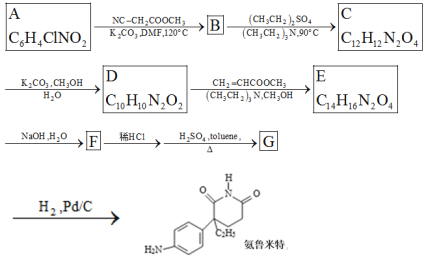
��A��BΪȡ����Ӧ��B�Ļ�ѧʽΪC10H8N2O4��B��C���һ�����Ӧ��
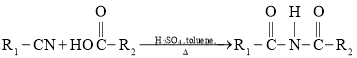
��C��D�ķ�Ӧ����ˮ�⡢��ȥ�Ȼ�(CO2 )������Ӧ��
��
��ش�
(1)������A�Ľṹ��ʽ________��
(2)����˵������ȷ����________��
A��������B�ܷ����ӳɷ�Ӧ B��������C�ܷ�����ȥ��Ӧ C��������G���м�������������������ˮ������CO2 D����³���صķ���ʽ��C13H16N2O2
(3)��ƻ�����Aת��Ϊ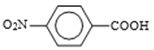 �ĺϳ�·��(������ͼ��ʾ���Լ���ѡ)________��
�ĺϳ�·��(������ͼ��ʾ���Լ���ѡ)________��
(4)д��E��F�Ļ�ѧ����ʽ________��
(5)д��������D���ܵ�ͬ���칹��Ľṹ��ʽ________����ͬʱ���ϣ���1H-NMR�ױ�����������4����ԭ�ӣ�IR����ʾ���б�����������״�ṹ��������-NH2������������ˮ�⣬���ܷ���������Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���ͳ�Ļ��̺��źܶ��ѧ֪ʶ������˵���������( )��
A.��ˮ�������ʣ�ɳ·ѩ��ƽ��δ�漰��ѧ�仯
B.�����ϴ���������ࡷ������(��ͭ)���������������������˺Ͻ�Ӳ�ȷ��������
C.��˾��֮(��)��Ͷ֮�ڵأ�����(��)ָ������˾������������ò���Ϊ![]()
D.�����ݸ�Ŀ������������������н��֮�ң������Ի���֭��ȡ������������������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״���½�4.48 L CO2ͨ��1 L 0.6 mol.L-l NaOH��Һ�У���CO2��NaOH��ȫ��Ӧʱ������˵������ȷ����
A.��Ӧ�����Һ����ȷ���Ƿ��ܼ�������CO2B.��Һ�����ʵ����ʵ���֮��Ϊ1:1
C.��Ӧ�����Һ�ʼ���D.��Һ�в�ֻ��һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£��ں����ܱ������з������·�Ӧ��2A(g)��B(g) ![]() 3C(g)������Ӧ��ʼʱ����2mol A��2mol B����ƽ���A���������Ϊa%��������������ʱ�������������������Ϊ��ʼ���ʣ�ƽ���A�������������a%���ǣ� )
3C(g)������Ӧ��ʼʱ����2mol A��2mol B����ƽ���A���������Ϊa%��������������ʱ�������������������Ϊ��ʼ���ʣ�ƽ���A�������������a%���ǣ� )
A.1mol B��1mol CB.2mol A��3mol B��1mol He��He���μӷ�Ӧ��
C.2mol CD.2mol A��3mol B��3mol C
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com