
【题目】下表为元素周期表中的一部分,列出10种元素在元素周期表中的位置.用化学符号回答下列各问题.
周期 |
|
|
|
|
|
|
| 0 |
2 | ⑥ | ⑦ | ⑧ | |||||
3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
4 | ② | ④ |
(1)10种元素中,化学性质最不活泼的是_________.
(2)①、③、⑤三种元素最高价氧化物对应水化物中,碱性最强的是_________.
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是_________.
(4)元素⑦的简单氢化物的化学式为_____;若该氢化物和元素⑨的单质反应,则化学方程式为_______.
(5)⑤和⑨的最高价氧化物对应水化物的化学式分别为_________和_________.
(6)①和⑤最高价氧化物对应水化物相互反应的离子方程式为__________________.
【答案】![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
根据元素在周期表中的位置关系可知,①、②、③、④、⑤、⑥、⑦、⑧、⑨和⑩分别是Na、K、Mg、Ca、Al、C、O、F、Cl和Ar,同一周期从左到右元素的非金属性依次增强,金属性依次减弱,同一主族中从上到下元素的非金属性依次减弱,金属性依次增强,结合元素周期律及物质的结构与性质分析作答。
(1)0族元素处于稳定状态,化学性质最不活泼,因此10种元素中,化学性质最不活泼的是Ar;
(2)元素的金属性越强,其最高价氧化物对应水化物的碱性越强,则①、③、⑤三种元素最高价氧化物对应水化物中,碱性最强的是NaOH;
(3)电子层数越多,简单离子半径越大,电子层数相同时,核电荷数越小,简单离子半径越大,故②、③、④三种元素形成的离子,离子半径由大到小的顺序是![]() ;
;
(4)元素⑦为O,其氢化物的化学式为H2O;氯气与水反应会生成氯化氢与次氯酸,其化学方程式为:![]() ,故答案为:H2O;
,故答案为:H2O;![]() ;
;
(5)⑤和⑨的最高价分别为+3价和+7价,其氧化物对应水化物的化学式分别为Al(OH)3和HClO4;
(6)①最高价氧化物对应水化物为NaOH,⑤最高价氧化物的水化物为Al(OH)3,两者相互反应的离子方程式为![]() 。
。


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]环丙贝特(H)是一种降血脂药物,可明显降低极低密度和低密度脂蛋白水平,并升高高密度脂蛋白,通过改善胆固醇的分布,可减少CH和LDL在血管壁的沉积,还有溶解纤维蛋白和阻止血小板凝聚作用。如图是合成环丙贝特的一种新方法:
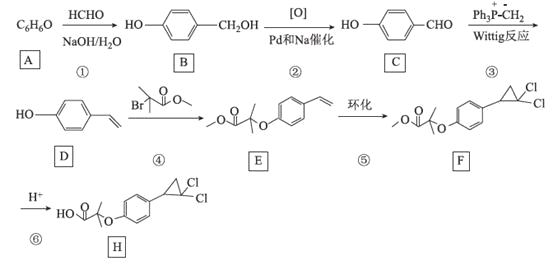
回答下列问题:
(1)C的化学名称为______________________
(2)F中含氧官能团的名称为______________
(3)H的分子式为________________________
(4)反应①的反应类型为___________,反应④的化学方程式为______________________
(5)M为![]() 的同分异构体,能与NaHCO3溶液反应产生气体,则M的结构共有种____(不考虑立体异构);其中1HNMR中有3组峰,且峰面积之比为6:2:1的结构简式为_______
的同分异构体,能与NaHCO3溶液反应产生气体,则M的结构共有种____(不考虑立体异构);其中1HNMR中有3组峰,且峰面积之比为6:2:1的结构简式为_______
(6)利用Wittig反应,设计以环己烷为原料(其他试剂任选),制备![]() 的合成路线:______________________。
的合成路线:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计了如图装置,该装置能制取Cl2,并进行相关性质实验,且可利用装置G储存多余的氯气。
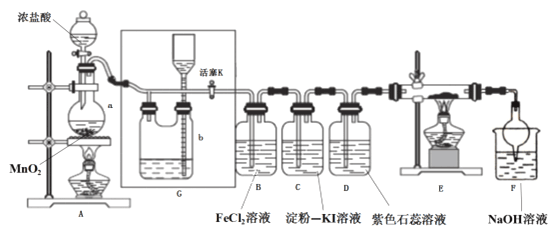
(1)A中发生反应的化学反应方程式为________
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯,回答下列问题:
①在装置C、D中能看到的实验现象分别是 ________ 、________;
②在装置E的硬质玻璃管内盛有碳粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为_________;
③装置F中球形干燥管的作用是__________;
(3)储气瓶b内盛放的试剂是___________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示:“氨气可在纯氧中安静燃烧……”。某校化学兴趣小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验对比。
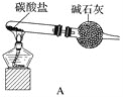
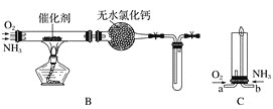
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是____________________;碱石灰的作用是__________________________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式__________________;试管内气体变为红棕色,该反应的化学方程式是_______________________。
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请说明可能的原因________________________。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气生成氮气和水:
①两气体通入的先后顺序是_____________,其理由是______________________。
②氨气燃烧的化学方程式是_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10 mL充满NO2和O2的混合气体的试管,倒置在水槽中,反应停止后试管内剩余2 mL的无色气体,求原混合气体中NO2和O2各多少毫升____________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究光盘金属层含有的Ag(其它金属微量忽略不计)、丢弃电池中的Ag2O等废旧资源的回收利用意义重大。下图为从光盘中提取Ag的工业流程,请回答下列问题。
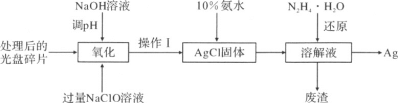
(1)NaClO溶液在受热或酸性条件下易分解,“氧化”阶段需在80℃条件下进行,适宜的加热方式为 _____。
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为______。有人提出以HNO3代替NaClO氧化Ag,从反应产物的角度分析,其缺点是_______。
(3)操作Ⅰ的名称为_______。化学上常用10%的氨水溶解AgCl固体,AgCl与NH3·H2O按1:2反应可生成Cl-和一种阳离子__________的溶液(填阳离子的化学式)。实际反应中,即使氨水过量也不能将AgCl固体全部溶解,可能的原因是_______。
(4)常温时N2H4·H2O(水合肼)在碱性条件下能还原(3)中生成的阳离子,自身转化为无害气体N2,理论上消耗0.1 mol的水合肼可提取到 ______g的单质Ag。
(5)废旧电池中Ag2O能将有毒气体甲醛(HCHO)氧化成CO2,科学家据此原理将上述过程设计为原电池回收电极材料Ag并有效去除毒气甲醛。则此电池的正极反应式为 _____,负极的产物有____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,适合进行现场酒精检测,下列说法不正确的是
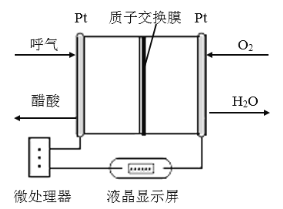
A.电流由O2所在的铂电极经外电路流向另一电极
B.该电池的正极反应式为:O2 + 4e- + 4H+=2H2O
C.该电池的负极反应式为:CH3CH2OH + 3H2O-12e-=2CO2↑ + 12H+
D.微处理器通过检测电流大小而计算出被测气体中酒精的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁是用途最广泛的金属材料。
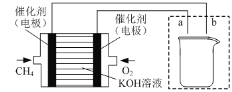
(1)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。写出正极反应式:______。

(2)纯铁作电极插入浓的NaOH溶液电解可制得Na2FeO4,装置如图所示。阳极的电极反应式为______;若消耗11.2g铁,则通过离子交换膜的Na+物质的量为______。

(3)如图所示装置为利用甲烷燃料电池实现在铁质材料上镀锌的一部分,燃料电池的负极反应式为______;在如图所示虚线框内补充完整在铁质材料上镀锌的装置图(注明电极材料和电解质溶液的成分)。_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是一种常见的化工原料,可以通过以下方法合成:
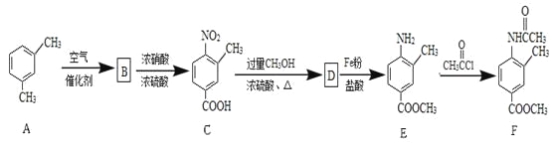
(1)写出化合物C中含氧官能团的名称:_________和___________。
(2)化合物B的结构简式为___________;由D→E的反应类型是___________。
(3)写出C→D反应的化学方程式:___________。
(4)写出同时满足下列条件的E的一种同分异构体的结构简式:___________。
Ⅰ.能发生银镜反应 ; Ⅱ.水解产物之一遇FeCl3溶液显色;
Ⅲ.分子中含有4种不同化学环境的氢。
(5)已知![]() 。请写出以
。请写出以![]() 为原料,制备化合物
为原料,制备化合物![]() 的合成路线流程图(无机试剂可任选)_______________。
的合成路线流程图(无机试剂可任选)_______________。
合成路线流程图示例如下:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com