
【题目】锂—铜空气燃料电池(如图)容量高、成本低,该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法错误的是
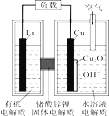
A. 整个反应过程中,氧化剂为O2
B. 放电时,正极的电极反应式为:Cu2O+H2O+2e-=2Cu+2OH-
C. 放电时,当电路中通过0.1 mol电子的电量时,有0.1 mol Li+透过固体电解质向Cu极移动,有标准状况下1.12 L氧气参与反应
D. 通空气时,铜被腐蚀,表面产生Cu2O
【答案】C
【解析】A,根据题意,该电池通过一种复杂的铜腐蚀“现象”产生电力,放电过程中消耗Cu2O,由此可见通入空气Cu腐蚀生成Cu2O,由放电反应推知Cu极电极反应式为Cu2O+2e-+H2O=2Cu+2OH-,Cu2O又被还原成Cu,整个过程中Cu相当于催化剂,氧化剂为O2,A项正确;B,放电时正极的电极反应式为Cu2O+2e-+H2O=2Cu+2OH-,B项正确;C,放电时负极电极反应式为Li-e-=Li+,电路中通过0.1mol电子生成0.1molLi+,Li+透过固体电解质向Cu极移动,反应中消耗O2物质的量为![]() =0.025mol,在标准状况下O2的体积为0.025mol
=0.025mol,在标准状况下O2的体积为0.025mol![]() 22.4L/mol=0.56L,C项错误;D,放电过程中消耗Cu2O,由此可见通入空气Cu腐蚀生成Cu2O,D项正确;答案选C。
22.4L/mol=0.56L,C项错误;D,放电过程中消耗Cu2O,由此可见通入空气Cu腐蚀生成Cu2O,D项正确;答案选C。


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】在实验室进行下列实验, 括号内的实验用品都能用到的是
A. 苯的溴代(苯、溴水、试管)B. 蛋白质的盐析(试管、醋酸铅溶液、鸡蛋白溶液)
C. 钠的焰色反应(铂丝、氯化钠溶液、稀盐酸)D. 肥皂的制取(烧杯、玻璃棒、甘油)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。
(1)科学家提出由CO2制取C的太阳能工艺如图所示。

①若“重整系统”发生的反应中n(FeO)/n(CO2)=6,则FexOy的化学式为____________。
②“热分解系统”中每分解1mol FexOy,转移电子的物质的量为________。
(2)工业上用CO2和H2反应合成二甲醚。已知:CO2(g)+ 3H2(g)═CH3OH(g)+ H2O(g) △H1=-53.7kJ/mol,CH3OCH3(g)+H2O(g) ═ 2CH3OH(g) △H2=+23.4kJ/mol,则2CO2(g)+ 6H2(g)![]() CH3OCH3(g)+3H2O(g) △H3=______kJ/mol。
CH3OCH3(g)+3H2O(g) △H3=______kJ/mol。
①一定条件下,上述合成甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是_____(填代号)。
a.逆反应速率先增大后减小 b.H2的转化率增大
c.反应物的体积百分含量减小 d.容器中的nCO2/nH2值变小
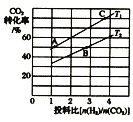
②在某压强下,合成甲醚的反应在不同温度、不同投料比时,CO2的转化率如图所示。T1温度下,将6 mol CO2和12molH2充入2L的密闭容器中,5 min后反应达到平衡状态,则0~5min内的平均反应速率v(CH3OCH3) =___;KA、KB、KC三者之间的大小关系为_____。
(3)常温下,用氨水吸收CO2可得到NH4HCO3溶液,在NH4HCO3溶液中:c (NH4+)_____c(HCO3-)(填“>”、“<”或“=”);反应NH4++HCO3-+H2O![]() NH3·H2O+H2CO3的平衡常数K=__________________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7mol·L-1,K2=4×10-11mol·L-1)
NH3·H2O+H2CO3的平衡常数K=__________________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7mol·L-1,K2=4×10-11mol·L-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断开1molH-H键吸收的能量为436KJ,形成1molH-N键放出的能量为391KJ,根据化学方程式N2+3H2![]() 2NH3,反应完1molN2放出的能量为924KJ,则断开1molN≡N键吸收的能量是
2NH3,反应完1molN2放出的能量为924KJ,则断开1molN≡N键吸收的能量是
A.431KJ B.649KJ C.869KJ D.945.6KJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度中,将1 molA 和2mol B放入容积为5L 的某密闭容器中发生反应:A(s) +2B(g)![]() C(g)+2D(g)。5min后达到平衡,测得容器内B的浓度减少了0.2mol/L,则下列叙述不正确的是
C(g)+2D(g)。5min后达到平衡,测得容器内B的浓度减少了0.2mol/L,则下列叙述不正确的是
A. 在5min 内该反应用C 的浓度变化表示的反应速率为0.02mol/(L·min)
B. 平衡时B 的转化率为50%
C. 平衡时B 的体积分数约为33.3%
D. 初始时的压强与平衡时的压强比为4 :5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图:
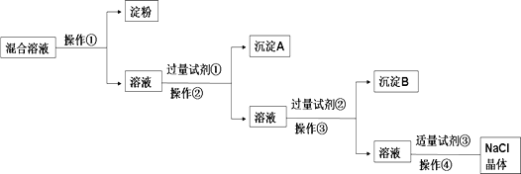
(1)写出上述实验过程中所用试剂:试剂①____;试剂③____。
(2)判断试剂①已过量的方法是:_____。
(3)操作①是利用半透膜进行分离提纯,操作①的实验结果:淀粉___(填“能”或“不能”)透过半透膜。
(4)操作④的名称是____,其中玻璃棒的作用是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】比较填空(填“>”、“<”或“=”)
(1)Ⅰ.比较等体积等浓度的溶液①盐酸 ②醋酸 与足量锌粒反应产生氢气的体积,① ②
Ⅱ.比较2H2(g)+O2(g)![]() 2H2O(g) ΔH 1 2H2(g)+O2(g)
2H2O(g) ΔH 1 2H2(g)+O2(g)![]() 2H2O(l) ΔH2的反应热 ΔH1 ΔH2
2H2O(l) ΔH2的反应热 ΔH1 ΔH2
Ⅲ.比较常温下两溶液水的电离程度,①pH=4盐酸 ②pH =10氨水溶液① ②
Ⅳ.同温度下溶液①使甲基橙呈现红色,溶液②使石蕊呈现紫色,比较两者pH① ②
(2)Ⅴ.已知某可逆反应aA(g) + bB(g) ![]() cC(g) + dD(g)。反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如右图,则a + b c + d
cC(g) + dD(g)。反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如右图,则a + b c + d

Ⅵ.比较①0.1mol/L醋酸与②0.01mol/L醋酸的导电能力,① ②
Ⅶ.1mol/L氨水与0.1mol/L氨水的c(OH-)之比 10
Ⅷ.体积相同的恒容密闭容器,在A中充入SO2和O2各1g,在B中充入SO2和O2各2g,相同条件下发生反应2SO2+O2![]() 2SO3 平衡时 SO2的转化率A B
2SO3 平衡时 SO2的转化率A B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2+ B2= 2AB的能量变化如图所示,则下列说法正确的是( )

A. 该反应是吸热反应
B. 断裂1 mol A—A键和1 mol B—B键能放出x kJ的能量
C. 断裂2 mol A—B键需要吸收y kJ的能量
D. 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若配制90mL0.1mol/L的FeCl3溶液,需要用到的仪器有托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管,还需要的仪器是( )
A.100mL圆底烧瓶B.100mL量筒
C.100mL容量瓶D.100mL烧杯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com