
【题目】下图是与乙醇有关的两个实验,
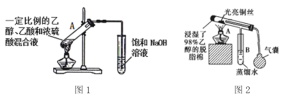
(1)图1试管A中的反应方程式为______________________________。请指出图1中两处明显的错误①________________________________;②_________________________________。
(2)点燃图2中酒精灯,反复挤压气囊,向图2装置中鼓入空气,铜丝反复出现由红变黑又由黑变红的现象,请写出相应的化学反应方程式____________________、____________________在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是________(填“吸热”或“放热”)反应。
(3)图2反应进行一段时间后,若试管B中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有__________(填名称)。要除去该物质,可先在混合液中加入_____(填写字母),
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过________________(填实验操作名称)即可除去。
【答案】CH3COOH+HOCH2CH3![]() CH3COOCH2CH3+H2O 导管末端伸入液面以下,易造成倒吸 饱和NaOH溶液碱性太强,易造成乙酸乙酯水解而降低产率 2Cu+O2
CH3COOCH2CH3+H2O 导管末端伸入液面以下,易造成倒吸 饱和NaOH溶液碱性太强,易造成乙酸乙酯水解而降低产率 2Cu+O2![]() 2CuO CH3CH2OH+CuO
2CuO CH3CH2OH+CuO![]() CH3CHO+Cu+H2O 放热 乙酸 c 蒸馏
CH3CHO+Cu+H2O 放热 乙酸 c 蒸馏
【解析】
图1为乙酸乙酯的制备实验,乙醇、乙酸和浓硫酸的混合液共热,反应生成乙酸乙酯,试管中盛放饱和碳酸钠溶液,可降低乙酸乙酯的溶解度,同时反应挥发出的乙酸,溶解乙醇,便于溶液分层,为防止倒吸,导管不能插入液面以下;图2为乙醇的催化氧化实验,加热条件下,铜先和氧气反应生成氧化铜,挥发的乙醇在加热条件被氧化铜氧化成乙醛,铜丝反复出现由红变黑又由黑变红的现象。
(1)乙酸和乙醇的酯化反应方程式为CH3COOH+HOCH2CH3![]() CH3COOCH2CH3+H2O;根据分析图示错误为:导管末端伸入液面以下,易造成倒吸;乙酸乙酯在碱性环境下发生水解,所以饱和NaOH溶液碱性太强,易造成乙酸乙酯水解而降低产率;
CH3COOCH2CH3+H2O;根据分析图示错误为:导管末端伸入液面以下,易造成倒吸;乙酸乙酯在碱性环境下发生水解,所以饱和NaOH溶液碱性太强,易造成乙酸乙酯水解而降低产率;
(2)铜丝反复出现由红变黑又由黑变红的现象,说明铜先和氧气反应生成氧化铜,挥发的乙醇在加热条件被氧化铜氧化成乙醛,氧化铜被还原为铜,反应的方程式为2Cu+O2![]() 2CuO、CH3CH2OH+CuO
2CuO、CH3CH2OH+CuO![]() CH3CHO+Cu+H2O;熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是放热反应;
CH3CHO+Cu+H2O;熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是放热反应;
(3)若试管B中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体显酸性,根据各物质的性质可以应是乙醛被氧化生成的乙酸;乙酸可以和碳酸氢钠溶液反应生成盐,增大与乙醇、乙醛的熔沸点差异,所以之后再进行蒸馏分离即可。


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A.1molNa2O2固体中含离子总数是3NA
B.0.1molMg 2+含有的核外电子数为0.2NA
C.常温下,1 L pH=13 的Ba(OH )2溶液中所含 OH-数目为 0.2NA
D.6.4 g Cu与足量硫充分反应,转移电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烷的催化裂解可按下列两种方式进行:C4H10→C2H6+C2H4; C4H10→CH4+C3H6;某化学兴趣小组的同学为探究丁烷裂解气中CH4和C2H6的比例关系,设计如图所示实验:
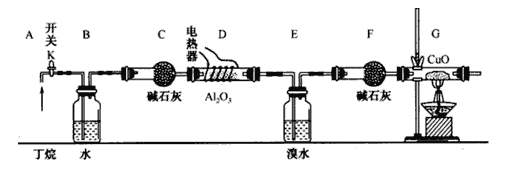
注:CuO能将烃氧化成CO2和H2O;A12O3是丁烷裂解的催化剂,G后面装置已省略。如图连接好装置后(部分夹持装置已略去),需进行的实验操作有:
①给D、G装置加热:②检査整套装置的气密性;③排尽装置中的空气。
(1)这三步操作的先后顺序依次是____________。
(2)简要说明检验空气排尽的方法:_______________________________________________。
(3)B装置所起的作用是__________________________________________。
(4)假设丁烷完全裂解,流经各装置中的气体能完全反应。当(E和F)装置的总质量比反应前增加了 1.82g, G装置中固体质量减少了 4.l6g,则丁烷的裂解产物中n(CH4)∶n(C2H6)=_____________。
(5)若对E装置中的混合物再按以下流程实验:

①分离操作I、Ⅱ的名称是I_____________、 II_______________;
②Na2SO3溶液的作用是(用离子方程式表示)__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两种有机物Q(![]() )与P(
)与P(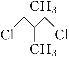 ),下列有关它们的说法中正
),下列有关它们的说法中正
确的是( )
A.二者的核磁共振氢谱中均只出现两种峰且峰面积之比为3∶1
B.二者在NaOH醇溶液中均可发生消去反应
C.一定条件下,二者在NaOH溶液中均可发生取代反应
D.Q的一氯代物只有1种、P的一溴代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的有
①0.1mol丙烯酸中含有双键的数目为0.1NA
②12g金刚石中,碳碳共价键数为4NA
③常温下,21g C3H6和C4H8的混合物中含有的碳原子数为1.5NA
④2g ![]() 中含有的质子数、中子数、电子数均为NA
中含有的质子数、中子数、电子数均为NA
⑤常温常压下,S2和S6的混合物共6.4g,其中所含硫原子数一定为0.2NA
⑥10mL 18mol/L的浓硫酸与足量的镁反应时转移的电子数为0.18NA
A. ①⑥B. ④⑤⑥C. ③④⑤D. ①②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】手持技术的氧电化学传感器可用于测定 O2含量,右图为某种氧电化学传感器的 原理示意图。已知在测定O2含量过程 中,电解质溶液的质量保持不变。一定时 间内,若通过传感器的待测气体为aL(标 准状况),某电极增重了b g。下列说法正确的是
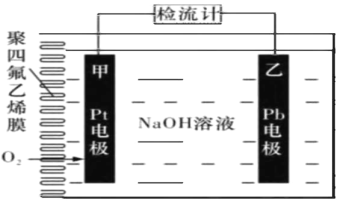
A.Pt电极为负极
B.反应过程中转移OH-的物质的量为0.125bmol
C.Pb电极上发生的电极反应为Pb-2e- +2OH- = Pb(OH)2
D.待测气体屮氧气的体积分数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对工业废水和生活污水进行处理是防止水体污染的主要措施.
![]() 水的净化和软化的区别是 ______
水的净化和软化的区别是 ______
![]() 在实验室中过滤操作需要用到的玻璃仪器有 ______ .
在实验室中过滤操作需要用到的玻璃仪器有 ______ .
![]() 下列试剂能够用来对自来水进行杀菌消毒,且不会造成二次污染的是 ______
下列试剂能够用来对自来水进行杀菌消毒,且不会造成二次污染的是 ______ ![]() 填字母
填字母![]() .
.
![]() 福尔马林
福尔马林![]() 漂白粉
漂白粉![]() 臭氧
臭氧![]() 氯气
氯气
![]() 是一种新型水处理剂,工业上可用
是一种新型水处理剂,工业上可用![]() 制备
制备![]() 其工艺流程如图:
其工艺流程如图:
![]()
![]() 工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加入绿矾.请解释这一做法的原因 ______
工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加入绿矾.请解释这一做法的原因 ______ ![]() 用必要的离子方程式和文字描述
用必要的离子方程式和文字描述![]() .
.
![]() 假设每步反应均是完全的,若制取3molNa2FeO4,需要NaClO固体 ______
假设每步反应均是完全的,若制取3molNa2FeO4,需要NaClO固体 ______ ![]()
![]() 写出第一步在酸性环境下加入H2O2的离子反应方程式 ______ .
写出第一步在酸性环境下加入H2O2的离子反应方程式 ______ .
![]() 石灰纯碱法是常用的硬水软化方法,已知
石灰纯碱法是常用的硬水软化方法,已知![]() 时
时![]() ,现将等体积的
,现将等体积的![]() 溶液与
溶液与![]() 溶液混合
溶液混合![]() 假设溶液体积具有加和性
假设溶液体积具有加和性![]() ,若
,若![]() 溶液的浓度为
溶液的浓度为![]() ,则生成沉淀所需Ca(OH)2溶液的最小浓度为 ______ .
,则生成沉淀所需Ca(OH)2溶液的最小浓度为 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是氢氧燃料电池构造示意图。下列说法不正确的是( )
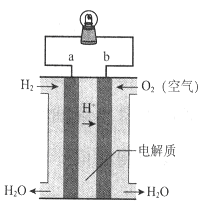
A. a极是负极
B. 电流由b通过灯泡流向a
C. 该电池总反应是2H2+ O2=2H2O
D. b极的电极反应为:O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有室温下四种溶液,①pH=11的氨水;②pH=11的NaOH溶液;③pH=3的醋酸;④pH=3的硫酸,下列有关说法不正确的是
A.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B.分别加水稀释10倍,四种溶液的pH①>②>④>③
C.①、④两溶液混合后,若溶液呈中性,则所得溶液中2c(NH4+)=c(SO42-)
D.V1L④与V2L②溶液混合后,若混合后溶液pH=4,则V1:V2=11:9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com