
【题目】已知乙酸和乙醇在浓硫酸催化下会发生下列反应:

CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
CH3CH2OH+CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
CH3CH2OH![]() CH2===CH2↑+H2O
CH2===CH2↑+H2O
沸点:乙醇78.5 ℃、乙酸117.9 ℃、乙酸乙酯77.1 ℃
某同学为了在实验室制备乙酸乙酯,设计了如下图所示的装置(部分类持仪器省略)。
实验步骤:
①在干燥的100 mL三颈烧瓶中加入8 mL 95%的乙醇,在冷水冷却下,边摇边慢慢加入8 mL浓硫酸,加入碎瓷片;在滴液漏斗中加入8 mL 95%的乙醇和8 mL乙酸,摇匀。按图组装仪器。滴液漏斗的末端和温度计的水银球必须浸到液面以下距瓶底0.5 cm~1 cm处。
②用电热套加热烧瓶,当温度计读数上升到110 ℃时,从滴液漏斗中滴加乙醇和乙酸混合液(速度为每分钟30滴为宜),并维持适宜的反应温度。滴加完毕,继续加热数分钟,直到反应液温度升到130 ℃,不再有馏出液为止。
③洗涤粗产物。
请回答下列问题:
(1)碎瓷片的作用是_____________________________________________。
冷凝管的作用是________________________________,水要从______(填“A”或“B”)口进入。馏出液的成分有_______________________________。
(2)整个实验过程要严格控制温度在________℃左右,否则会________________。
(3)洗涤粗产物的方法是:向粗产物中慢慢加入________溶液,然后用分液法分离。下列有关分液操作的叙述正确的是________(填字母序号)。
a.应选用球形分液漏斗进行分液,使用前要检查是否漏水
b.将混合液倒入分液漏斗,塞紧玻璃塞,上下振荡
c.混合液摇匀后,立即将分液漏斗放在铁圈上静置,分层
d.打开分液漏斗的玻璃塞,再打开旋塞,使下层液体从分液漏斗下端放出,待下层液体完全流出后关闭旋塞,把上层液体从分液漏斗上口倒出
(4)为了得到更纯的产物,需向(3)中得到的酯中加入无水硫酸镁进行干燥,然后通过________法分离。
下列区分乙酸乙酯精品和粗品的方法,不合理的是______________。
a.用溴水检验 b.用金属钠检验
c.测定沸点 d.用新制Cu(OH)2悬浊液检验
(5)本实验如何创造条件使酯化反应尽量向生成物方向进行?(至少提出两点)
①________________________________________________________;
②________________________________________________________。
【答案】 防止液体暴沸 冷凝收集乙酸乙酯 A 乙酸乙酯、乙酸、乙醇 120 发生副反应,使制得的乙酸乙酯不纯(或含有乙醚) 饱和碳酸钠 d 蒸馏 ad 加入过量的乙醇 将乙酸乙酯从反应液中不断蒸出,使平衡向乙酸乙酯产生的方向移动
【解析】(1)酯化反应需要加热,为了防止液体沸腾时剧烈跳动,需要加热碎瓷片以防止暴沸;冷凝管常用于蒸馏液体或在有机制备中起冷凝或回流作用,本实验中冷凝收集挥发出的乙酸乙酯;为了使冷凝效果更佳,应采用逆流方式进水,故水从A口进入B口流出;反应温度为120℃,所以馏出液的成分有:乙酸乙酯、乙酸、乙醇。
(2)由已知,酯化反应在120℃条件下发生,温度超过140℃会有副反应发生,使制得的乙酸乙酯不纯,所以要控制温度在120℃左右。
(3)粗产品中含有乙酸乙酯、乙酸、乙醇,加入饱和碳酸钠一方面可以吸收乙醇,中和乙酸,另一方面可以降低乙酸乙酯的溶解度,有利于分层析出;乙酸乙酯不溶于水溶液,所以分离方法为分液,打开分液漏斗的玻璃塞,使内外空气相通,再打开旋塞,使下层液体从分液漏斗下端放出,待下层液体完全流出后关闭旋塞,把上层液体从分液漏斗上口倒出,故d是正确的分液操作。
(4)分离酯中可溶性的有机物,可利用乙酸乙酯沸点为77.1 ℃用蒸馏法分离;乙酸乙酯精品和粗品的不同为:粗品中含有乙醇、乙酸等杂质,都能与金属钠反应,精品为纯净物有固定熔沸点,溴水和新制Cu(OH)2悬浊液与乙醇、乙酸都不反应,故无法区分乙酸乙酯精品和粗品,选ad。
(5)制备乙酸乙酯的反应为可逆反应,增大反应物浓度或减小生成物浓度平衡正向移动,所以加入过量的乙醇可使酯化反应向生成物方向进行,将乙酸乙酯从反应液中不断蒸出,也可使平衡向乙酸乙酯产生的方向移动。


科目:高中化学 来源: 题型:
【题目】下列关于苯的说法中正确的是( )
A. 苯分子中的所有化学键都完全相同
B. 苯分子中含有碳碳双键,能使酸性高锰酸钾溶液褪色
C. 苯是一种密度比水小,不溶于水的有特殊气味的无色液体
D. 在催化剂存在下,苯能与溴水发生取代反应,生成溴苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了避免NO、NO2、N2O4对大气的污染,常采用NaOH溶液进行吸收处理(反应方程式:2NO2+2NaOH===NaNO3+NaNO2+H2O;NO2+NO+2NaOH===2NaNO2+H2O)。现有由a mol NO、b mol NO2、c mol N2O4组成的混合气体恰好被V L NaOH溶液吸收(无气体剩余),则此NaOH溶液的物质的量浓度为
A. ![]() mol·L-1 B.
mol·L-1 B. ![]() mol·L-1
mol·L-1
C. ![]() mol·L-1 D.
mol·L-1 D. ![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4常用作氧化剂、防腐剂、消毒剂、漂白剂和水处理剂等。
(1)在K2MnO4溶液中通入CO2可制得高锰酸钾,副产物是黑色沉淀M。该反应中氧化剂与还原剂的质量之比为__________________。由锂离子有机高聚物、锂及M构成原电池,电池反应为Li+M=LiM(s),消耗8.7gM时转移0.1mol电子。则该电池正极的电极反应为___________________________________。
(2)实验室用KMnO4制备O2和Cl2。取0.4mol KMnO4固体加热一段时间后,收集到
amolO2,在反应后的残留固体中加入足量浓盐酸,加热又收集到bmolCl2。设锰元素全部
转化成Mn2+存在于溶液中,当a+b=0.8mol时,在标准状况下生成Cl2的体积为______L;
(3)电解K2MnO4溶液加以制备KMnO4。工业上,通常以软锰矿(主要成分是MnO2)与KOH的混合物在铁坩埚(熔融池)中混合均匀,小火加热至熔融,即可得到绿色的K2MnO4 ,化学方程式为_______________________________。用镍片作阳极(镍不参与反应),铁板为阴极,电解K2MnO4溶液可制备KMnO4。上述过程用流程图表示如下:

则D的化学式为___________;阳极的电极反应式为_____________________;阳离子迁移方向是___________________。
(4)高锰酸钾在酸性介质中还原产物为Mn2+,废液中c(Mn2+)浓度较大时会污染水体。实验室可以用过二硫酸铵[(NH4)2S2O8]溶液检验废水中Mn2+,实验现象是溶液变紫红色(还原产物为SO42-)。过二硫酸可以看成是H2O2的衍生物,过二硫酸铵中含有过氧键(-O-O-)。写出检验Mn2+的离子方程式_________________________________。如果将这个反应设计成盐桥原电池,盐桥中溶液最好选用______________。(选填:饱和KCl溶液、饱和K2SO4溶液或饱和NH4Cl溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

(I)该硫酸的物质的量浓度是________。
(II)某化学兴趣小组进行硫酸性质的实验探究时,需要240mL1.84mol/L的稀硫酸。可供选抒的仪器由:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙 请冋答下列问题:
(1) 上述仪器中,再配置稀硫酸时用不到的有________ (填代号)
(2) 经计算,需:浓硫酸的体积为_____________。现有:
①10mL ②50mL ③100mL三种规格的量筒,你选用的量筒是______ (填代号)
将上述硫酸迸行稀释的实验操作有:___________________。
(3)在配制稀硫酸过程中,其他操作都准确,能引起误差偏高的有:_________ (填代号)
①洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
②容量瓶用1moll/L稀硫酸润洗
③转移前,容量瓶中含存少量蒸馏水
④量.取浓硫酸时俯视读刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅单质及其化合物的说法不正确的是( )
A. 水玻璃是一种矿物胶,既不易燃烧也不易腐蚀
B. 水泥、玻璃、石英都是硅酸盐制品
C. 氮化硅(Si3N4)是一种重要的结构陶瓷材料
D. 向Na2SiO3溶液中逐滴加入稀盐酸制备硅酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用固体NaOH配制0.5 mol/L的NaOH溶液500 mL,①烧杯②100 ml量筒③容量瓶④药匙⑤玻璃棒⑥托盘天平⑦烧瓶
(1)配制时,必须使用的仪器有_____________(填代号),还缺少的仪器是__________________。
(2)在配制的转移过程中某学生进行如图操作,请指出其中的错误:______________、____________。
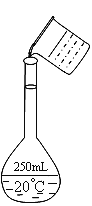
(3)配制时,一般可分为以下几个步骤①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却。其正确的操作顺序为_________________。
(4)下列操作会使配制的溶液浓度偏低的是___________(填字母)
A.没有将洗涤液转移到容量瓶 B.转移过程中有少量溶液溅出
C.容量瓶洗净后未干燥 D.定容时俯视刻度线
E.固体NaOH中含有少量Na2O杂质
(5)在容量瓶使用方法中,下列操作不正确的是(填序号) ___________
A.使用容量瓶前检査它是否漏水
B.容量瓶用蒸馏水洗净后,再用碱液润洗
C.将氢氧化钠固体直接放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是 ( )

A. 该硫酸的物质的量浓度为9.2mol/L
B. 1molCu与足量该硫酸反应产生2g氢气
C. 配制200mL4.6mol/L的稀硫酸需取该硫酸50mL
D. 该硫酸与等质量的水混合后所得溶液的浓度大于9.2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
(1)金刚石晶体中含有共价键形成的C原子环,其中最小的C环上有_______个C原子。
(2)CsCl晶体中每个Cs+周围有_________个Cl-,每个Cs+周围与它最近且距离相等的Cs+共有________个。
(3)白磷分子中的键角为__________,分子的空间结构为__________,每个P原子与___个P原子结合成共价键。若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合_______个氧原子, 若每个P原子上的孤对电子再与氧原子配位,就可以得到磷的另一种氧化物_______________(填分子式)。

(4)二氧化硅是一种________晶体,每个硅原子周围有_________个氧原子。
(5)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答。这个基本结构单元由_____个硼原子组成,共含有________个B-B键。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com