
【题目】工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2·4H2O],煅烧可获得钛酸钡粉体。

(1)“酸浸”应选择_________(填标号);为提高酸浸率,可采取的措施_________(至少答两点)
a. 硫酸 b. 盐酸 c. 硝酸
(2)实验室要完成操作1需要的玻璃仪器有_________。
(3)加入H2C2O4溶液时,发生的反应为______+______TiCl4+_____H2C2O4+ _____H2O= BaTiO(C2O4)2·4H2O↓ + _________;可循环使用的物质X是(写名称)_________。
(4)请简述检验草酸氧钛钡晶体是否洗涤干净的方法_________。
(5)高温煅烧草酸氧钛钡晶体得到BaTiO3的同时,生成的气体产物有CO、和_________。
(6)测定钛酸钡粉体中BaTiO3的质量分数。
已知:Ba2++CrO42-=BaCrO4↓ 2CrO42-+2H+=Cr2O72-+H2O
现取a g煅烧后的BaTiO3粉末酸溶得到100.0 mL含Ba2+的溶液,取25.00 mL于锥形瓶,加入x mL 浓度为C1 mol/L的Na2CrO4溶液(Na2CrO4过量)充分反应后,用浓度为C2 mol/L标准盐酸滴定至CrO42-被完全反应,消耗盐酸体积为y mL。(钛元素不干扰测定过程)已知BaTiO3的摩尔质量为M g/mol,试写出粉体中BaTiO3质量分数的表达式。_________
【答案】b 适当加热、搅拌、将固体粉碎、适当提高酸的浓度 漏斗、玻璃棒、烧杯 1BaCl2 1 2 5 6HCl 盐酸 取最后一次洗涤流出液于试管,加入少量硝酸酸化的AgNO3溶液,若试管中无白色浑浊出现,则证明已经洗涤干净 CO2、H2O ![]()
【解析】
由制备流程可知,碳酸钡与盐酸反应生成氯化钡,然后氯化钡与四氯化钛、草酸反应生成BaTiO(C2O4)24H2O,过滤、洗涤、干燥、煅烧得到BaTiO3。
(1)碳酸钡与盐酸反应生成氯化钡、水、二氧化碳,根据物质的存在状态及影响速率的因素分析采取的措施;
(2)分离难溶性固体与液体混合物的操作是过滤,使用的玻璃仪器有烧杯、漏斗、玻璃棒;
(3)向BaCl2、TiCl4混合溶液中加入H2C2O4溶液生成草酸氧钛钡晶体,同时生成HCl可循环使用;
(4)草酸氧钛钡晶体是从含HCl的溶液中过滤出来的,可用硝酸银检验沉淀是否洗涤干净;
(5)根据元素守恒,结合物质组成及元素的化合价分析判断生成物;
(6)根据给出的方程式,计算出25.00 mL溶液中含有的Ba2+的物质的量,然后根据物质总体积与实验时的体积关系及样品质量,得到其质量分数表达式。
(1)根据流程图可知使用的酸为盐酸,序号为b;为加快反应速率,采取的措施可以是将固体粉碎、搅拌、升高反应温度、增大酸的浓度等措施;
(2)操作1是过滤,过滤时使用的玻璃仪器有漏斗、玻璃棒、烧杯;
(3)根据流程图可知:向BaCl2、TiCl4混合溶液中加入H2C2O4溶液生成草酸氧钛钡晶体,反应的化学方程式为:BaCl2+TiCl4+2H2C2O4+5H2O=BaTiO(C2O4)24H2O↓+6HCl,反应产生的HCl可循环使用,用来再溶解BaCO3;
(4)根据(3)方程式可知:草酸氧钛钡晶体是从含HCl的溶液中过滤出来的,若该晶体洗涤干净,则洗涤溶液中无Cl-,加入AgNO3溶液,不会产生白色沉淀。因此草酸氧钛钡晶体可用硝酸银检验沉淀是否洗涤干净;
(5)BaTiO(C2O4)24H2O煅烧,发生分解反应,生成高温下的气体产物有CO、CO2、H2O(g);
(6)根据题意可知在25.00mL溶液中含有Ba2+的物质的量是n(Ba2+)=(xC1 –yC2)×10-3mol,则a g样品得到的100.0 mL含Ba2+的物质的量是n(Ba2+)(总)=(xC1 –yC2)×10-3![]() mol=4(xC1 –yC2)×10-3mol;BaTiO3的摩尔质量为M g/mol,则含有的BaTiO3的质量为m(BaTiO3)= 4(xC1 –yC2)×10-3mol×Mg/mol= 4M(xC1 –yC2)×10-3g,样品质量为ag,故粉体中BaTiO3质量分数的表达式为:
mol=4(xC1 –yC2)×10-3mol;BaTiO3的摩尔质量为M g/mol,则含有的BaTiO3的质量为m(BaTiO3)= 4(xC1 –yC2)×10-3mol×Mg/mol= 4M(xC1 –yC2)×10-3g,样品质量为ag,故粉体中BaTiO3质量分数的表达式为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】常温下,取一定量的PbI2固体配成饱和溶液,t时刻改变某一条件,离子浓度变化如图所示。下列有关说法正确的是

A. 常温下,Ksp(PbS)=8×10-28,向PbI2的悬浊液中加入Na2S溶液,反应PbI2(s)+S2-(aq)![]() PbS(s)+2I-(aq)的化学平衡常数为5×1018
PbS(s)+2I-(aq)的化学平衡常数为5×1018
B. 常温下,PbI2的Ksp为2×10-6
C. 温度不变,t时刻改变的条件可能是向溶液中加入了KI固体,PbI2的Ksp增大
D. 温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,平衡向左移动,Pb2+的浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨为放热反应,下列说法正确的是
A.断开H-H键放出能量B.形成N-H键吸收能量
C.反应物的总能量大于生成物的总能量D.反应物的总能量小于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某体积固定的密闭容器中加入0.3 mol A、0.1 mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:

(1)密闭容器的体积是_____L;
(2)若t1=15时,则t0~t1 s内以C物质浓度变化表示的反应速率v(C)=_______;
(3)写出反应的化学方程式:________________________;
(4)t1 s时,A的转化率为__________,此时v(A)正______v(B)逆(选填“>”、“<”或“=”);
(5)B的起始的物质的量是_____;
(6)平衡时体系内的压强为初始状态的___________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学---选修3:物质结构与性质)
(1)![]() 中
中![]() 原子的杂化轨道类型为____________,
原子的杂化轨道类型为____________,![]() 分子空间构型为________________。
分子空间构型为________________。
(2)已知:硼酸的电离方程式为![]() ,试依据上述反应写出
,试依据上述反应写出![]() 的结构式____________________。
的结构式____________________。
(3)钛铁矿经过![]() 等多种物质处理后会生成
等多种物质处理后会生成![]() 等中间产物。
等中间产物。
①![]() 晶体中存在_________________(填字母代号)。
晶体中存在_________________(填字母代号)。
A. 离子键 B. ![]() 键 C.
键 C. ![]() 键 D.氢键
键 D.氢键
②![]() 为粘稠状、难挥发性的强酸,而
为粘稠状、难挥发性的强酸,而![]() 是易挥发性的强酸,其原因是____________________。
是易挥发性的强酸,其原因是____________________。
(4)![]() 是离子晶体,其晶格能可通过下图的
是离子晶体,其晶格能可通过下图的![]() 循环计算得到。
循环计算得到。
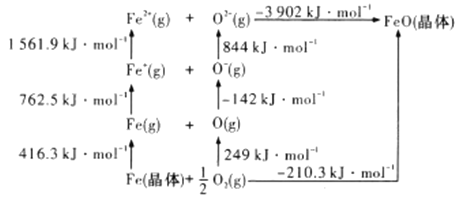
可知,![]() 原子的第一电子亲和能为___________
原子的第一电子亲和能为___________![]() ,
,![]() 晶格能为______________
晶格能为______________![]() 。
。
(5)![]() 可用于制造高温发热元件,其在高温时具有立方晶型,晶胞如图所示。
可用于制造高温发热元件,其在高温时具有立方晶型,晶胞如图所示。

已知晶胞参数为![]() ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为![]() ,则
,则![]() 原子与
原子与![]() 原子之间的最短距离为_______
原子之间的最短距离为_______![]() ;
;![]() 的密度为_______________________
的密度为_______________________![]() (列式表示)。
(列式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,纯水的电离度为α1,pH=3的醋酸中水的电离度为α2,pH=11的氢氧化钠溶液中水的电离度为α3。若将上述醋酸溶液和氢氧化钠溶液等体积混合,所得溶液中水的电离度为α4,则下列关系正确的是
A. α1<α3<α2<α4 B. α3<α2<α1<α4 C. α2=α3<α1<α4 D. α2=α3<α4<α1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知二元弱碱B(OH)2在水中存在如下电离平衡:B(OH)2 ![]() B(OH)++OH-,Kb1=10-3.75;B(OH)+
B(OH)++OH-,Kb1=10-3.75;B(OH)+![]() B2++OH-,Kb2=10-7.62。常温下,用0.1 mol/L盐酸滴定25 mL 0.1 mol/L的B(OH)2溶液,得到如图所示的滴定曲线。下列说法不正确的是
B2++OH-,Kb2=10-7.62。常温下,用0.1 mol/L盐酸滴定25 mL 0.1 mol/L的B(OH)2溶液,得到如图所示的滴定曲线。下列说法不正确的是

A. a点所得的溶液中:c[B(OH)2]= c[B(OH)+]
B. b点所得的溶液中:c[B(OH)2] +c(OH-)=c(B2+)+c(H+)
C. c点所得的溶液中:c(Cl-)<3c[B(OH)+]
D. d点所得的溶液中:c(B2+)>c[B(OH)+]>c[B(OH)2]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com