
肼(N2H4)广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用的氧化剂。请回答下列问题:
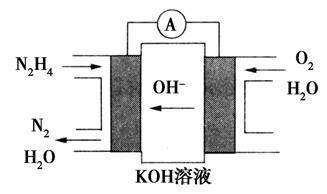
(1)肼燃料电池原理构造如图所示,负极上的电极反应式为____。
(2)火箭常用N2O4作氧化剂,肼作燃料,已知:
①N2(g)+2O2(g)===2NO2(g)
ΔH=-67.7 kJ/mol
②N2H4(g)+O2(g)===N2(g)+2H2O(g)
ΔH=-534.0 kJ/mol
③2NO2(g)===N2O4(g) ΔH=-52.7 kJ/mol
试写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:____________________________。
(3)在高锰酸钾催化下,用尿素[CO(NH2)2]和次氯酸钠-氢氧化钠溶液反应获得肼,该反应的离子方程式为_________________。
解析:本题考查了燃料电池和热化学方程式等知识,意在考查考生对相关知识的理解与应用能力。(1)由题给装置图可知,负极发生反应的物质为N2H4,负极反应式为N2H4-4e-+4OH-===N2↑+4H2O。(2)根据盖斯定律,由②×2-(①+③)得,2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-947.6 kJ/mol。(3)分析题给信息知,反应的粒子为CO(NH2)2、ClO-、OH-,生成的粒子为N2H4、CO 、Cl-、H2O,则CO(NH2)2+ClO-+2OH-
、Cl-、H2O,则CO(NH2)2+ClO-+2OH-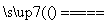 N2H4+CO
N2H4+CO +Cl-+H2O。
+Cl-+H2O。
答案:(1)N2H4-4e-+4OH-===N2↑+4H2O(3分)
(2)2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-947.6 kJ/mol(3分)
(3)CO(NH2)2+ClO-+2OH-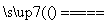 N2H4+CO
N2H4+CO +Cl-+H2O(2分)
+Cl-+H2O(2分)


科目:高中化学 来源: 题型:
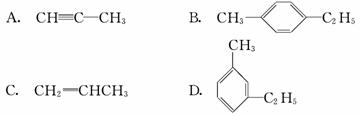
有机物中碳原子和氢原子个数比为3∶4,不能与溴水反应却能使KMnO4酸性溶液褪色。其蒸气密度是相同状况下甲烷密度的7.5倍。在铁存在时与溴反应,能生成两种一溴代物。该有机物可能是( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与有机物结构、性质相关的叙述中,正确的是( )
A.乙醇与金属钠反应比水与金属钠反应更剧烈
B.乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色
C.蛋白质、淀粉、纤维素、蔗糖都属于有机高分子化合物
D.乙酸、甲酸甲酯和羟基乙醛( )互为同分异构体
)互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
用CH4催化还原NOx可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)
ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)
ΔH=-1160 kJ·mol-1
下列说法不正确的是( )
A.由反应①可推知:CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l) ΔH=-Q,Q>574 kJ·mol-1
B.等物质的量的甲烷分别参加反应①、②,反应转移的电子数不同
C.若用标准状况下4.48 L CH4还原NO2至N2则放出的热量为173.4 kJ
D.若用标准状况下4.48 L CH4还原NO2至N2,则整个过程中转移的电子总物质的量为1.6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2(g)+ O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1,C(s)+
O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1,C(s)+ O2(g)===CO(g) ΔH2=-110.5 kJ·mol-1。由此可知焦炭与水蒸气反应的热化学方程式为:C(s)+H2O(g)===CO(g)+H2(g) ΔH3,则ΔH3为( )
O2(g)===CO(g) ΔH2=-110.5 kJ·mol-1。由此可知焦炭与水蒸气反应的热化学方程式为:C(s)+H2O(g)===CO(g)+H2(g) ΔH3,则ΔH3为( )
A.+131.3 kJ·mol-1 B.-131.3 kJ·mol-1
C.+352.3 kJ·mol-1 D.-352.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
将2 mol A与2 mol B混合于2 L的密闭容器中,发生如下反应:2A(g)+3B(g)2C(g)+zD(g),若2分钟后达到平衡,A的转化率为50%,测得v(D)=0.25 mol/(L·min),则下列推断正确的是( )
A.v(C)=0.2 mol/(L·min)
B.z=3
C.B的转化率为25%
D.C的体积分数约为28.6%
查看答案和解析>>
科目:高中化学 来源: 题型:
温度为T时,向V L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)C(s)+xD(g) ΔH>0,容器中A、B、D的物质的量浓度随时间的变化如图所示。下列说法正确的是( )
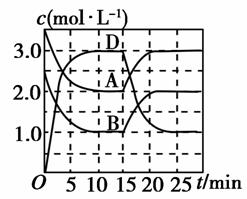
A.反应在前10 min的平均反应速率v(B)=0.1 mol·L-1·min-1
B.该反应的平衡常数表达式K=
C.若平衡时保持温度不变,压缩容器体积平衡向逆反应方向移动
D.反应至15 min时,改变的条件是降低温度
查看答案和解析>>
科目:高中化学 来源: 题型:
氮的氧化物(用NOx表示)是大气污染物,必须进行处理。
(1)汽车尾气主要含有CO2、CO、SO2、NOx等物质,这种尾气逐渐成为城市空气污染的主要来源之一。
①汽车尾气中的CO来自于____________________,NO来自于_____________________。汽车尾气对环境的危害主要有________________________(至少填两种)。
②汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。反应的化学方程式可表示为__________________________。
(2)用氨可将氮氧化物转化为无毒气体。已知:4NH3+6NO 5N2+6H2O,8NH3+6NO2
5N2+6H2O,8NH3+6NO2 7N2+12H2O。同温同压下,3.5 L NH3恰好将3.0 L NO和NO2的混合气体完全转化为N2,则原混合气体中NO和NO2的体积之比是________。
7N2+12H2O。同温同压下,3.5 L NH3恰好将3.0 L NO和NO2的混合气体完全转化为N2,则原混合气体中NO和NO2的体积之比是________。
(3)工业尾气中氮的氧化物常采用碱液吸收法处理,若NO与NO2按物质的量之比1∶1被足量NaOH溶液完全吸收后得到一种钠盐,该钠盐的化学式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
亚硝酸钠(NaNO2)在纤维纺织品的染色和漂白、照相、生产橡胶、制药等领域有广泛应用,也常用于鱼类、肉类等食品的染色和防腐。但因其有毒,所以在食品行业用量有严格限制。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:①NO+NO2+2OH-===2NO +H2O
+H2O
②气体液化的温度:NO2为21 ℃,NO为-152 ℃

(1)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接)为A、C、________、________、________。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是________________________________________________________________________。
(3)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是_______________________________
________________________________________________________________________。
②装置E的作用是_______________________________________________________。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为________________
________________________________________________________
________________。如果没有装置C,对实验结论造成的影响是__________________
______________________________________________________。
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com