
【题目】有关下列各装置图的叙述,不正确的是( )

A. 装置①可用于吸收实验中多余的Cl2
B. 装置②可用于收集H2、NH3、Cl2、HCl、NO等
C. 装置③中X为CCl4,可用于吸收氨气或氯化氢
D. 装置④可用于收集氨气,并吸收多余的氨气
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气发生反应的装置。回答下列问题:
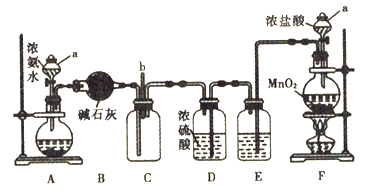
(1)仪器a的名称为______________。装置A的圆底烧瓶中盛放的固体物质可选用_______(填序号)
a.氯化钠 b.氢氧化钠 c.碳酸钙
(2)装置B、D的作用均为_____________________。从装置C的b处逸出的尾气中含有少量Cl2,为防止其污染环境,可将尾气通过盛有_____________溶液的洗气瓶。
(3)装置F的圆底烧瓶中发生反应的离子方程式为____________________________。装置E的作用是除去Cl2中的HCl,洗气瓶中盛 放的试剂为_________________________。
(4)反应过程中,装置C的集气瓶中有大量白烟产生,另一种产物为N2。该反应的化学方程式为___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。
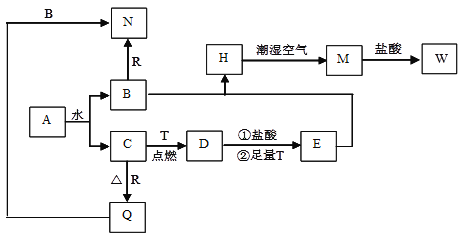
(1)写出下列物质的化学式A_______;D__________;N________。
(2)按要求写下列反应方程式:检验w中阳离子的离子方程式__________________________。
H在潮湿空气中变成M的化学方程式_________________________________。
D与盐酸反应的离子方程式_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、D是由常见的短周期非金属元素形成的单质,常温下A是淡黄色粉末,B、D是气体,F、G、H的焰色反应均为黄色,水溶液均显碱性,E有漂白性。它们之间的转化关系如图所示(部分产物及反应条件已略去),回答下列问题:
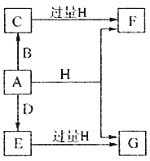
(1)A所含元素在周期表中的位置为______________,C的电子式为_______________。
(2)A与H在加热条件下反应的化学方程式为__________________。
(3)将A溶于沸腾的G溶液中可以制得化合物I,I在酸性溶液中不稳定,易生成等物质的量的A和E,I在酸性条件下生成A和E的离子方程式为____________________。I是中强还原剂,在纺织、造纸工业中作为脱氯剂,向I溶液中通入氯气可发生反应,参加反应的I和氯气的物质的量比为1:4,该反应的离子方程式为__________________。
(4)向含有0.4molF、0.1molG的混合溶液中加入过量盐酸,完全反应后收集到aL气体C(标准状况),取反应后澄清溶液,加入过量FeCl3溶液,得到沉淀3.2g,则a=____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请用下列10种物质的序号填空:
①O2 ②H2 ③NH4NO3 ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2
其中既有离子键又有非极性键的是________;既有离子键又有极性键的是________。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为_________;若XY2为共价化合物时,其结构式为______。
(3)氯化铝的物理性质非常特殊,如:氯化铝的熔点为190℃,但在180℃就开始升华。据此判断,氯化铝是________(填“共价化合物”或“离子化合物”),可以证明你的判断正确的实验依据____________________。
(4)现有a~g7种短周期元素,它们在周期表中的位置如图所示,请据此回答下列问题:
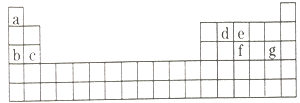
①元素的原子间反应最容易形成离子键的是________________。
A.c和f B.b和g C.d和g D.b和e
②写出a~g7种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按如图进行反应。下列说法中正确的是

A. A、B、C中三种元素的任意两种元素形成的化合物所属物质类别可能是氧化物
B. A、B、C中三种元素的任意两种元素形成的化合物所属物质类别一定不是碱
C. 如果E溶液是一种强酸,则E溶液为硫酸
D. A、B、C中有一种金属且为B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纤维素被称为“第七营养素”.食物中的纤维素虽然不能被消化,但能刺激肠道蠕动和分泌消化液,有助于食物的消化和废物的排泄.在化学分类中,纤维素属于( )
A.蛋白质
B.脂肪
C.多糖
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com