
����Ŀ��A��B��D���ɳ����Ķ����ڷǽ���Ԫ���γɵĵ��ʣ�������A�ǵ���ɫ��ĩ��B��D�����壬F��G��H����ɫ��Ӧ��Ϊ��ɫ��ˮ��Һ���Լ��ԣ�E��Ư���ԡ�����֮���ת����ϵ��ͼ��ʾ�����ֲ��P��Ӧ��������ȥ�����ش��������⣺
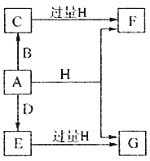
��1��A����Ԫ�������ڱ��е�λ��Ϊ______________��C�ĵ���ʽΪ_______________��
��2��A��H�ڼ��������·�Ӧ�Ļ�ѧ����ʽΪ__________________��
��3����A���ڷ��ڵ�G��Һ�п����Ƶû�����I��I��������Һ�в��ȶ��������ɵ����ʵ�����A��E��I����������������A��E�����ӷ���ʽΪ____________________��I����ǿ��ԭ�����ڷ�֯����ֽ��ҵ����Ϊ���ȼ�����I��Һ��ͨ�������ɷ�����Ӧ���μӷ�Ӧ��I�����������ʵ�����Ϊ1:4���÷�Ӧ�����ӷ���ʽΪ__________________��
��4������0.4molF��0.1molG�Ļ����Һ�м���������ᣬ��ȫ��Ӧ���ռ���aL����C����״������ȡ��Ӧ�������Һ���������FeCl3��Һ���õ�����3.2g����a=____________________��
���𰸡� �������� ����A�� ![]() 3S + 6NaOH
3S + 6NaOH ![]() 2Na2S + Na2SO3 + 3H2O 2H+ + S2O32-
2Na2S + Na2SO3 + 3H2O 2H+ + S2O32- ![]() S��+ SO2��+H2O 4Cl2 +S2O32-+ 5H2O
S��+ SO2��+H2O 4Cl2 +S2O32-+ 5H2O![]() 8Cl- + 2SO42- + 10H+ 2.24
8Cl- + 2SO42- + 10H+ 2.24
��������������A�ǵ���ɫ��ĩ����Ϊ���ʣ���A����B��D�����壬A��D����E��E��Ư���ԣ�˵��EΪSO2��D��O2����B��H2��CΪH2S��F��G��H����ɫ��Ӧ��Ϊ��ɫ��F��G��H�о�������Ԫ�أ�ˮ��Һ���Լ��ԣ�SO2��H2S������H��Ӧ��HΪNaOH����FΪNa2S��GΪNa2SO3����1��A�����ʣ�λ�ڵ������ڢ�AԪ�أ�CΪH2S�����ڹ��ۻ���������ʽΪ![]() ����2���������ȵ�����������Һ�����绯��Ӧ���������ƺ��������ƣ�����Ӧ����ʽΪ��3S + 6NaOH
����2���������ȵ�����������Һ�����绯��Ӧ���������ƺ��������ƣ�����Ӧ����ʽΪ��3S + 6NaOH ![]() 2Na2S + Na2SO3 + 3H2O����3��S�ͷ���Na2SO3�õ�������Na2S2O3��Na2S2O3����������������S��SO2�������ӷ�Ӧ����ʽΪ��2H+ + S2O32-
2Na2S + Na2SO3 + 3H2O����3��S�ͷ���Na2SO3�õ�������Na2S2O3��Na2S2O3����������������S��SO2�������ӷ�Ӧ����ʽΪ��2H+ + S2O32- ![]() S��+ SO2��+H2O����������ǿ�����ԣ��ܰ�S2O32��������SO42������������ԭ��Cl����Na2SO3�����������ʵ���֮��Ϊ1��4�������ߵ�ϵ��Ϊ1��4��S2O32����4Cl2��2SO42����8Cl�������ݻ�ѧ��Ӧ����ʽԭ�Ӹ����غ㣬��Ӧǰ��5��O����ȱ��5molH2O������������Ӧ��10H���������ӷ�Ӧ����ʽΪ4Cl2��S2O32����5H2O=8Cl����2SO42����10H������4����Ӧ�������Һ���������FeCl3��Һ���õ�����3.2g�����ݷ�Ӧ2Fe3����S2��=2Fe2����S�����÷�Ӧ�����ĵ�Na2SΪ0.1mol��Na2S��Na2SO3�Ļ����Һ�м���������ᣬ������Ӧ��2S2����SO32����6H��=3S����3H2O������Na2SO3 0.1mol��ʣ���Na2S 0.1mol�����ᷴӦ�ų�H2S���ų�H2S�����ʵ���Ϊ0.1mol����״���µ����Ϊ2.24L��
S��+ SO2��+H2O����������ǿ�����ԣ��ܰ�S2O32��������SO42������������ԭ��Cl����Na2SO3�����������ʵ���֮��Ϊ1��4�������ߵ�ϵ��Ϊ1��4��S2O32����4Cl2��2SO42����8Cl�������ݻ�ѧ��Ӧ����ʽԭ�Ӹ����غ㣬��Ӧǰ��5��O����ȱ��5molH2O������������Ӧ��10H���������ӷ�Ӧ����ʽΪ4Cl2��S2O32����5H2O=8Cl����2SO42����10H������4����Ӧ�������Һ���������FeCl3��Һ���õ�����3.2g�����ݷ�Ӧ2Fe3����S2��=2Fe2����S�����÷�Ӧ�����ĵ�Na2SΪ0.1mol��Na2S��Na2SO3�Ļ����Һ�м���������ᣬ������Ӧ��2S2����SO32����6H��=3S����3H2O������Na2SO3 0.1mol��ʣ���Na2S 0.1mol�����ᷴӦ�ų�H2S���ų�H2S�����ʵ���Ϊ0.1mol����״���µ����Ϊ2.24L��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ַ�ɢϵ�ķ�ɢ�����Ӽ�������Ĥ��Ҳ������ֽ���÷�ɢϵΪ��������
A. ��ҺB. ����C. ����ҺD. ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ���������ʵĵ���ƽ�ⳣ�������ʾ��
��ѧʽ | CH3COOH | H2C2O4 | H2S |
����ƽ�ⳣ�� | 1.8��10��5 | Ka1=5.4��10��2 | Ka1=1.3��10��7 |
��ش��������⣺
��1��H2S��һ�����볣������ʽΪKa1=
��2��CH3COOH��H2C2O4��H2S��������ǿ������˳��
��3��H2C2O4��������KOH��Һ��Ӧ�Ļ�ѧ����ʽ��
��4��NaHS��Һ��NaHC2O4��Һ��Ӧ�����ӷ���ʽ��
��5��H+Ũ����ͬ�������������ҺA�����ᣩ��B��CH3COOH���ֱ���п�۷�Ӧ����������һ����Һ�д���п���ų�������������ͬ��������˵����ȷ��������д��ţ��� �ٷ�Ӧ����Ҫ��ʱ��B��A
�ڿ�ʼ��Ӧʱ������A��B
�۲μӷ�Ӧ��п�����ʵ���A=B
�ܷ�Ӧ���̵�ƽ������B��A
��B����пʣ�࣮
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����a��ʾ���ȷ�ӦX��g��+Y��g��Z��g��+M��g��+N��s�����й�����X��ת������ʱ��仯�Ĺ�ϵ����Ҫ�ı���ʼ������ʹ��Ӧ���̰�b���߽��У��ɲ�ȡ�Ĵ�ʩ�ǣ� �� 
A.��ѹ
B.�Ӵ�X��Ͷ����
C.�����¶�
D.�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У�����������KMnO4��Һ��Ӧ����������ˮ��Ӧ����
������ �ڱ� �۱�ϩ ���ڶ��ױ�
A. �٢�B. ��C. �ڢ�D. ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ҫ����к��ȵIJⶨ��
��1��ʵ�����ϱ��д�С�����ձ�����ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ����β����������0.5molL��1���ᡢ0.55molL��1NaOH��Һ��ʵ����ȱ�ٵIJ�����Ʒ���� ��
��2��ʵ�����ܷ��û���ͭ˿��������滷�β��������������ܡ�������ԭ���� ��
��3�����Ǽ�¼��ʵ���������£�
ʵ����Ʒ | ��Һ�¶� | �к��� | ||
t1 | t2 | ��H | ||
�� | 50 mL0.55 molL��1NaOH��Һ | 20�� | 23.3�� | |
50 mL0.5 molL��1HCl��Һ | ||||
�� | 50 mL0.55 molL��1NaOH��Һ | 20�� | 23.5�� | |
50 mL0.5 molL��1HCl��Һ | ||||
��֪��Q=cm��t2��t1������Ӧ����Һ�ı�����cΪ4.18J����1g��1 �� �����ʵ��ܶȾ�Ϊ1gcm��3 ��
�ټ�������ϱ���H=������2λС������
�ڸ���ʵ����д��NaOH��Һ��HCl��Һ��Ӧ���Ȼ�ѧ����ʽ�� ��
��4������KOH����NaOH���Բⶨ�������С����ޡ���Ӱ�죻���ô������HCl��ʵ�飬�Բⶨ�����С����ޡ���Ӱ�죮
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ�ᾧţ�ȵ��ط��ӽṹʾ��ͼ����֪�ȵ��غ���A��B������������A������21�������ᣬB������30�������ᣬ������������ͨ��������������������������SH�ѵ����������Ӷ��ɣ����ӣ���A����Ҳ�γ�1������������ȵ��ط����к��е��ļ�����51����������ˮ�����γ��ȵ��غ���Է���������ԭ�����ٵ���ֵ���ǣ� ��
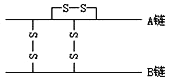
A. 49 882 B. 49 888 C. 50 882 D. 50 888
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2A��g��+B��g��=3C��g��+4D��g����Ӧ�У���ʾ�÷�Ӧ�������������ǣ� ��
A.v��A��=0.9 mol/��Ls��
B.v��B��=0.5 mol/��Ls��
C.v��C��=1.4 mol/��Ls��
D.v��D��=1.8 mol/��Ls��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ3H2+N2 ![]() 2NH3���ܱ������н��У����й��ڸ÷�Ӧ��˵��������ǣ� ��
2NH3���ܱ������н��У����й��ڸ÷�Ӧ��˵��������ǣ� ��
A.�����¶��ܼӿ췴Ӧ����
B.ʹ��ǡ���Ĵ����ܼӿ췴Ӧ����
C.����N2��Ũ���ܼӿ췴Ӧ����
D.ƽ��ʱ����ֺ���֮��һ������3��1��2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com