
【题目】下列有关物质用途的叙述错误的是
A.SO2可用于杀菌消毒,是一种食品添加剂
B.液氨常用作制冷剂,是因为氨气液化时要吸收大量的热
C.硅单质具有良好的半导体性能,可制成计算机的芯片
D.硫酸铵、碳酸氢铵等铵盐是农业上常用的化肥
科目:高中化学 来源: 题型:
【题目】香豆素类化合物具有芳香气味,是生药中的一类重要的活性成分,主要分布在伞形科、豆科、菊科、芸香科、茄科、瑞香科、兰科等植物中。化合物X是一种香豆素衍生物,可以用作香料,其合成路线如下:
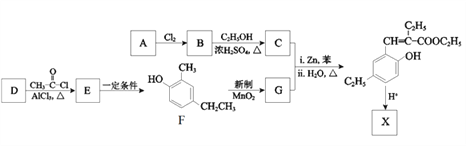
已知: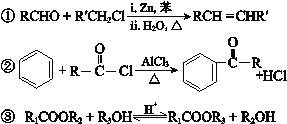
(1)已知A的分子式为C4H8O2。A所含官能团的名称是______________。
(2)B生成C反应的化学方程式是______________________________________________。
(3)G的结构简式是__________________________。
(4)D的分子式是C7H8O,与F互为同系物。则D的结构简式是___________________。
(5)E可以经多步反应合成F,请写出一条可能的合成路线_________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
(6)X的分子式是C13H14O2,X与足量NaOH溶液共热的化学方程式是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A由Al2O3、Fe3O4、Al、Cu中的某几种粉末混合而成,设计成分分析方案如下,下列分析不正确的是( )
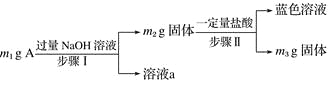
A. 当m1>m2时,溶液a中阴离子只有1种
B. 生成蓝色溶液的离子方程式涉Cu+2Fe3+===Cu2++2Fe2+
C. 要确定混合物中是否含Al,可取A加入适量稀HCl
D. 当m2-m3=2.96 g,Fe3O4的质量至少为2.32 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的现象描述与离子方程式都正确的是
A. 锌片插入硝酸银溶液中,有银析出: ![]()
B. 氢氧化钡溶液与稀硫酸反应,有白色沉淀生成: ![]()
C. 氢氧化铜加到盐酸中, 无明显现象: ![]()
D. 碳酸钡中加入稀盐酸,固体溶解,生成无色无味气体: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的某有机物A完全燃烧后,生成0.03mol二氧化碳和0.04mol水,其蒸汽的密度是同温同压条件下氢气密度的30倍。
(1)A的分子式为____________________。
(2)根据其分子组成,A的类别可能为__________或__________(填物质类别)。
(3)A可与金属钠发生置换反应,其H-NMR(氢核磁共振)谱图显示有三组吸收峰,请写出A在铜催化下被氧化的化学方程式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增加的短周期主族元素。W存在4原子核18电子的氢化物分子,X的最外层电子数是电子层数的![]() ,Z与W同主族,X、Y、Z的最外层电子数之和为9。下列说法正确的是
,Z与W同主族,X、Y、Z的最外层电子数之和为9。下列说法正确的是
A. 简单离子半径:W>X>Y>Z
B. 简单氢化物的沸点:Z>W
C. X2W、YZ均为离子化合物
D. W、X、Z三种元素组成的化合物水溶液显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了能观察到丁达尔效应,一中鼹鼠科学社的同学在实验室制备Fe(OH)3胶体。
(1)胶体与其他分散系的本质区别是:__。
(2)制备时,将_逐滴滴加至_中,待液体呈_后,停止加热;反应方程式为__。
(3)有一种橘红色的硫化锑(Sb2S3)胶体,装入U型管,插入电极后通直流电,发现阳极附近橘红色加深,这叫__现象,证明Sb2S3胶粒带__电荷。
(4)如何设计实验验证制得的氢氧化铁是胶体:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒容密闭容器中,发生反应:CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH。其平衡常数(K)和温度(T)的关系如下表:
CO(g)+H2O(g) ΔH。其平衡常数(K)和温度(T)的关系如下表:
T℃ | 700 | 800 | 850 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
试回答下列问题:
(1)上述反应为____(填“放热”或“吸热”)反应,升高温度,平衡向______ (填“正反应”或“逆反应”) 方向移动。
(2)某温度下,在体积为2L的恒容密闭容器中通入2molCO2(g)和4molH2(B)发生上述应,5min时反应达到平衡,测得CO2(g)的转化率是75%。
①v(H2O)=______mol·L-1·min-l。
②该温度下反应的平衡常数K=______.
(3)生产水煤气的过程如下:
①C(s)+CO2(g) ![]() 2CO(g)ΔH1
2CO(g)ΔH1
②CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH2
CO2(g)+H2(g) ΔH2
③反应:CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH=________ (用含ΔH1、ΔH2的代数式表示)。
CO(g)+H2O(g) ΔH=________ (用含ΔH1、ΔH2的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com