
【题目】已知铅蓄电池放电时的原电池反应:PbO2+Pb+2H2SO4===2PbSO4+2H2O。关于铅蓄电池的下列说法中正确的是( )
A. 放电时的正极反应式是Pb+SO42--2e-===PbSO4
B. 放电时电池的负极材料是铅板
C. 充电时,电池中硫酸的浓度不断变小
D. 充电时,铅板发生氧化反应
科目:高中化学 来源: 题型:
【题目】化合物H是合成药物盐酸沙格雷酯的重要中间体,其合成路线如图:
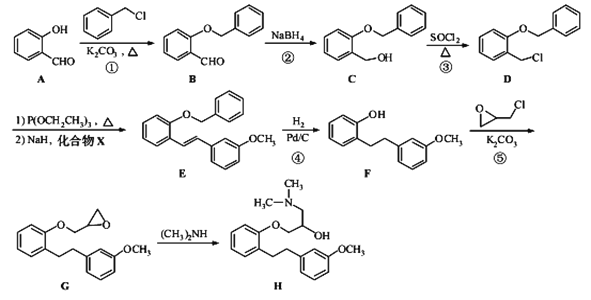
(1)化合物A中的含氧官能团为___和___(填官能团名称)。
(2)反应⑤的反应类型是___,反应方程式___。
(3)B的分子式___,1molB与足量的银氨溶液反应,最多能产生___gAg。
(4)检验D中卤原子种类,所需的试剂有___。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式:___。
a.分子中含有两个苯环;
b.分子中有7种不同化学环境的氢;
c.不能与FeCl3溶液发生显色反应,但水解产物之一能发生此反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】花椒毒素(Ⅰ)是白芷等中草药的药效成分,也可用多酚A为原料制备,合成路线如下:

回答下列问题:
(1)①的反应类型为_____________________;B分子中最多有_________个原子共平面。
(2)C中含氧官能团的名称为______________________;③的“条件a”为____________________。
(3)④为加成反应,化学方程式为__________________________________。
(4)⑤的化学方程式为__________________________________。
(5)芳香化合物J是D的同分异构体,符合下列条件的J的结构共有_________种,其中核磁共振氢谱为五组峰的J的结构简式为_________________。(只写一种即可)。
①苯环上只有3个取代基;②可与NaHCO3反应放出CO2;③1mol J可中和3mol NaOH。
(6)参照题图信息,写出以 为原料制备
为原料制备 的合成路线(无机试剂任选) :______________
的合成路线(无机试剂任选) :______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是( )

A. Mg 电极是该电池的正极
B. H2O2在石墨电极上发生氧化反应
C. 石墨电极附近溶液的pH 增大
D. 溶液中Cl-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 有相同容积的定容密封容器甲和乙,甲中加入
有相同容积的定容密封容器甲和乙,甲中加入![]() 和
和![]() 各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
A.甲、乙提高相同温度 B. 甲中加入0.1mol He,乙不改变
C.甲降低温度,乙不变 D. 甲增加0.1mol ![]() ,乙增加0.1mol I2
,乙增加0.1mol I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在体积为10L的密闭容器中,3molX和1molY进行反应:2X(g)+Y(g)![]() Z(g),经2min达到平衡,生成0.6mol Z,下列说法正确的是( )
Z(g),经2min达到平衡,生成0.6mol Z,下列说法正确的是( )
A.以X浓度变化表示的反应速率为0.01 mol/(L·s)
B.将容器体积变为20L,Z的平衡浓度为原来的![]()
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、M、N为短周期元素且原子序数依次增大,X与M、W与N分别同主族,且元素X、Y、Z、W分属两个短周期,它们四者原子序数之和为22,最外层电子数之和为16,在化合物Y2X6、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构,请回答下列问题:
(1)Y元素在周期表中的位置是____________,X、Y、Z、W、M的原子半径由大到小的顺序为:__________________________(用元素符号表示)。
(2)写出Y2X6的电子式_____;Z2X4结构式______;X2W2所含化学键的类型______。
(3)用电子式描述M2N所形成化合物的形成过程_________________________。
(4)均含X、W、M、N四种元素的两种化合物相互反应有刺激性气味气体放出,反应的离子方程式为__________________。
(5)火箭发动机曾经利用Z2X4作燃料X2W2作助燃剂,产物环保无污染,写出二者反应的方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能(KJ/mol) | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15399 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
①某同学根据上述信息,推断B的核外电子排布如下图所示,该同学所画的电子排布图违背 ,B元素位于周期表五个区域中的 区。
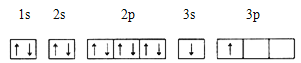
②ACl2分子中A的杂化类型为 ,ACl2的空间构型为 。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①以体心立方堆积形成的金属铁中,其原子的配位数为 。
②写出一种与CN-互为等电子体的单质的电子式 。
③六氰合亚铁离子[Fe(CN)6]4-中不存在 。
A.共价键
B.非极性键
C.配位键
D.σ键
E.π键
(3)一种Al-Fe合金的立体晶胞如右图所示。请据此回答下列问题:
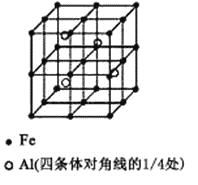
①确定该合金的化学式 。
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为 cm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com