
| A、Na2CO3═2Na++CO32- |
| B、NaHCO3═Na++HCO3- |
| C、H2SO4═2H++SO42- |
| D、KClO3═K++Cl-+3O2- |


科目:高中化学 来源: 题型:
| A、200 mL 0.25 mol/L NaCl溶液 |
| B、200 mL 1 mol/L NaCl溶液 |
| C、100 mL 0.5 mol/L NaOH溶液 |
| D、100 mL 2 mol/L NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无沉淀生成 |
| B、得到的沉淀是BaSO4和BaSO3组成的混合物 |
| C、得到的沉淀是纯净物 |
| D、肯定没有BaSO3生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化碳的摩尔质量是44g |
| B、摩尔既是微粒数目的单位,也是物质的量的单位 |
| C、阿伏加德罗常数的符号为NA,其近似值为6.02×1023 mol-1 |
| D、1 mol H2O的质量为18 g?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚丙烯的链节是-CH2-CH2-CH2- | |||
B、向苯酚溶液中滴加Na2CO3溶液: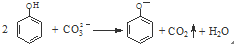 | |||
C、CH3COOH+CH3CH218OH
| |||
| D、苯的同系物能使酸性高锰酸钾溶液褪色,说明烃基对苯环的性质产生了较大的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ | |
| 甲 | 常温常压下气体的质量 | 气体分子数 | 固体体积 | 溶液中溶质质量分数 |
| 乙 | 气体相对分子质量 | 阿伏加德罗常数 | 固体密度 | 溶液的体积 |
| A、①② | B、③④ | C、②③ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
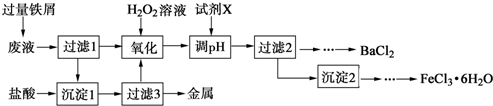
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com