
【题目】石油气“芳构化”是由石油气生产高辛烷值汽油的一种有效生产工艺。测得反应2C4H10![]() C8H10(g)+5H2在不同温度下的平衡常数变化如下:
C8H10(g)+5H2在不同温度下的平衡常数变化如下:
温度(℃) | 400 | 450 | 500 |
平衡常数K | a | 6a | 40a |
(1)该反应的正反应是________(填“吸热”或“放热”)反应。
(2)向2 L密闭定容容器中充入2 mol C4H10,反应10 s后测得H2浓度为1 mol·L-1,此10 s内,以C8H10表示的平均速率为____________________。
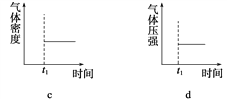
(3)能表示该反应在恒温恒容密闭容器中t1时刻后已经达平衡状态的图示是__________。

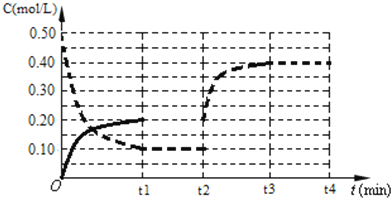
(4)下图表示某温度时将一定量的C4H10(含少量H2)充入容器中反应期间物质浓度随时间的变化(容器容积可变),实线代表C8H10,虚线代表C4H10。请用实线补充画出t1~t4间C8H10的浓度变化曲线。_____________
【答案】 吸热 0.02 b d 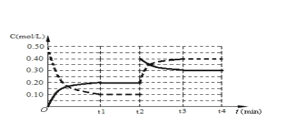
【解析】(1)图表数据,平衡常数随温度升高增大,平衡正向进行,正反应是吸热反应;(2)向2L密闭定容容器中充入2mol C4H10,反应10s后测得H2浓度为1mol/L,2C4H10 ![]() C8H10(g)+5H2,反应过程中生成C8H10的物质的量浓度为
C8H10(g)+5H2,反应过程中生成C8H10的物质的量浓度为![]() ×1mol/L=0.2mol/L,此10s内,以C8H10表示的平均速率=
×1mol/L=0.2mol/L,此10s内,以C8H10表示的平均速率=![]() =0.02mol/(Ls);(3)2C4H10
=0.02mol/(Ls);(3)2C4H10![]() C8H10(g)+5H2,反应是气体体积增大的吸热反应,依据平衡移动原理分析图象;a、反应前后都是气体,气体质量在反应过程中和平衡状态都始终不变,不能说明反应达到平衡状态,选项a不符合;b、反应前后气体质量不变,物质的量增大,平均摩尔质量不变说明反应达到平衡状态,选项b符合;c、气体质量不变,体积不变,密度在反应过程中和平衡状态都不变,选项c不符合;d、反应前后气体物质的量变化,压强之比等于气体物质的量之比,物质的量不变压强不变,说明反应达到平衡,选项d符合;答案选b、d;(4)分析图象可知,刚开始因为达到平衡状态,所以浓度不变,后面体积缩小为原来的
C8H10(g)+5H2,反应是气体体积增大的吸热反应,依据平衡移动原理分析图象;a、反应前后都是气体,气体质量在反应过程中和平衡状态都始终不变,不能说明反应达到平衡状态,选项a不符合;b、反应前后气体质量不变,物质的量增大,平均摩尔质量不变说明反应达到平衡状态,选项b符合;c、气体质量不变,体积不变,密度在反应过程中和平衡状态都不变,选项c不符合;d、反应前后气体物质的量变化,压强之比等于气体物质的量之比,物质的量不变压强不变,说明反应达到平衡,选项d符合;答案选b、d;(4)分析图象可知,刚开始因为达到平衡状态,所以浓度不变,后面体积缩小为原来的![]() (根据虚线的浓度变化可知),所以实线浓度也变为两倍,浓度变化为0.40mol/L,随反应进行后面又慢慢减小,直至继续平衡,据此画出的图象为:
(根据虚线的浓度变化可知),所以实线浓度也变为两倍,浓度变化为0.40mol/L,随反应进行后面又慢慢减小,直至继续平衡,据此画出的图象为: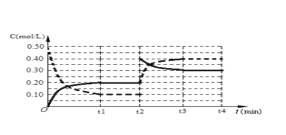


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值.下列说法正确的是( )
A. 高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
B. 室温下,1 L pH=13的NaOH溶液中,由水电离的OH﹣离子数目为0.1NA
C. 氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA
D. 5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验的反应原理用离子方程式表示正确的是( )
A. 室温下,测的氯化铵溶液pH<7,证明一水合氨的是弱碱:NH4++2H2O=NH3·H2O+H3O+
B. 用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O=2AlO2-+3H2↑
C. 用碳酸氢钠溶液检验水杨酸中的羧基:
 +2HCO3-→
+2HCO3-→ +2H2O+2CO2↑
+2H2O+2CO2↑
D. 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有8种物质:①乙烷②乙烯③乙炔④苯⑤甲苯⑥四氯化碳⑦聚丙烯⑧环己烯。其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是( )
A.①②③⑤B.①⑥⑦⑧C.①④⑥⑦D.②③⑤⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁:另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡.则原混合溶液中钾离子的物质的量浓度为( )
A.(4b﹣2a)/V molL﹣1
B.(b﹣2a)/V molL﹣1
C.(2b﹣2a)/V molL﹣1
D.(b﹣a)/V molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,不能观察到明显的变化的是 ( )
A. 把氯气通入FeCl2溶液中 B. 把一段打磨过的镁带放入少量冷水中
C. 把溴水滴加到KI淀粉溶液中 D. 把绿豆大的钾投入水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通过反应“SiO2+2C![]() Si+2CO↑”制取单质硅,下列说法正确的是
Si+2CO↑”制取单质硅,下列说法正确的是
A. 自然界中硅元素均以SiO2形式存在
B. 高纯度晶体Si可用于制造光导纤维
C. 该反应条件下C的还原性比Si强
D. 标准状况下生成4.48 L CO时转移电子数为0.4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定放置已久的小苏打样品中纯碱的质量分数.
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算.实验中加热至恒重的目的是 .
(2)方案二:按如图装置进行实验.并回答以下问题: 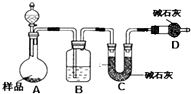
①分液漏斗中应该装(填“盐酸”或“稀硫酸盐”),D装置的作用是 .
②实验中除称量样品质量外,还需称装置反应前后质量的变化(用装置的字母代号);
③根据此实验得到的数据,测定结果有较大误差,因为实验装置还存在一个明显缺陷,该缺陷是 .
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液,过滤洗涤,干燥沉淀,称量固体质量,计算:
①实验中判断沉淀已完全的方法是 .
②若加入试剂改为氢氧化钡,已知称得样品9.5g,干燥的沉淀质量为19.7g,则样品中碳酸钠的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA.下列说法正确的是( )
A. 1L0.1molL﹣1NH4Cl溶液中,NH4+的数量为0.1NA
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1NA
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com