
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
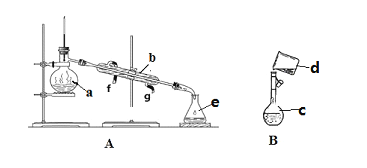
(1)写出下列仪器的名称:a.____________,b.___________,c.__________。
(2)若利用装置分离酒精和水的混合物,还缺少的仪器是______,冷凝水由___口流出(填f或g)。
(3)现需配制0.1mol/LNaOH溶液450mL,装置B是某同学转移溶液的示意图。
①图中的错误是_____________________________。
②根据计算得知,所需NaOH的质量为____________________。
【答案】蒸馏烧瓶 冷凝管 容量瓶 酒精灯 f 移液时未用玻璃棒引流 2g
【解析】
(1)蒸馏装置中的主要仪器有蒸馏烧瓶、冷凝管、温度计、牛角管、锥形瓶,酒精灯,精确配制溶液需容量瓶和玻璃棒,根据实验的需求进行判断;
(2)根据蒸馏的原理和操作步骤寻找装置中的缺少的仪器;冷凝管下口是进水口,上口是出水口;
(3)根据配制一定物质的量浓度的溶液的方法和操作来寻找装置中的错误;根据容量瓶的容积确定配制溶液的多少;
(1)根据装置的特征,装置a为蒸馏烧瓶;b为冷凝管;c为容量瓶;答案为:蒸馏烧瓶;冷凝管;容量瓶;
(2)蒸馏装置还缺少主要加热的装置,酒精灯;为保证水充满冷凝管,充分起到冷凝的作用,冷凝管下口是进水口,上口是出水口,所以冷凝管的进水口是f,故答案为:酒精灯; f;
(3)配制一定物质的量浓度的溶液是必须用玻璃棒引流,防止液体外溅,容量瓶只有一个刻度线,只能用来配制所标容量规格的溶液,现需配制450mL只能选用500ml容量瓶,需配制0.1mol/LNaOH溶液500mL,m(NaOH)=0.1mol/L×0.5L×40g/mol=2g;答案为:移液时未用玻璃棒引流;2g;


科目:高中化学 来源: 题型:
【题目】将等物质的量的金属Na、Mg、Al分别与100mL2mol/L盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法不正确的是( )

A. x=2.24
B. 反应时,Na、Mg、Al均过量
C. 钠的物质的量为0.2 mol
D. 曲线b为Mg与盐酸反应的图像
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.萃取操作可在普通漏斗中完成
B.浓烧碱液沾到皮肤上应立即用稀盐酸冲洗
C.闻未知液体或气体的气味时,应该将试剂瓶口距离口鼻远一些,用手轻轻扇动
D.用容量瓶配制好一定浓度的某溶液后,将溶液保存在容量瓶中并贴上标签
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化苄(C6H5CH2Cl)为无色液体,是一种重要的有机化工原料。现在实验室模拟工业上用甲苯与干燥氯气在光照条件下加热反应合成氯化苄、分离出氯化苄并检验样品的纯度,其装置(夹持装置略去)如图所示:
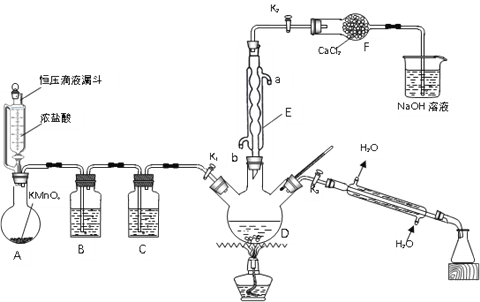
回答下列问题:
(1)仪器E的名称是______;其作用是______;其进水口为______(填“a”或“b”)。
(2)装置B中的溶液为______;装置F的作用是______。
(3)用恒压滴液漏斗代替分液漏斗的优点是______。
(4)装置A中反应的离子方程式为______。
(5)反应结束后,关闭K1和K2,打开K3,加热三颈烧瓶,分馏出氯化苄,应选择温度范围为______℃。
物质 | 溶解性 | 熔点(℃) | 沸点(℃) |
甲苯 | 极微溶于水,能与乙醇、乙醚等混溶 | -94.9 | 110 |
氯化苄 | 微溶于水,易溶于苯、甲苯等有机溶剂 | -39 | 178.8 |
二氯化苄 | 不溶于水,溶于乙醇、乙醚 | -16 | 205 |
三氯化苄 | 不溶于水,溶于乙醇、乙醚和苯 | -7 | 220 |
(6)检测氯化苄样品的纯度:
①称取13.00g样品于烧杯中,加入50.00mL 4 molL-1 NaOH水溶液,水浴加热1小时,冷却后加入35.00mL 40% HNO3,再将全部溶液转移到容量瓶中配成100mL溶液。取20.00mL溶液于试管中,加入足量的AgNO3溶液,充分振荡,过滤、洗涤、干燥,称量固体质量为2.87g,则该样品的纯度为______%(结果保留小数点后1位)。
②实际测量结果可能偏高,原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌是一种重要的过渡金属,锌及其化合物有着广泛的应用。
(1)指出锌在周期表中的位置:第________周期,第________族,________区。
(2)Zn形成金属晶体,其金属原子堆积属于下列______模式。
A.简单立方 B.钾型 C.镁型 D.铜型
(3)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式________;葡萄糖分子中碳原子的杂化方式为________。
(4)Zn2+能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子属于________(填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,NH3位于正四面体的顶点,试在右下图中表示[Zn(NH3)4]2+中Zn2+与NH3之间的化学键______。
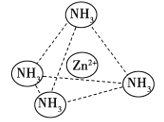
(5)下图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为______________________。该化合物晶体的熔点比干冰高得多,原因是____________________。

(6)与锌同周期,最外层有3个未成对电子的元素名称是________,该元素最高价氧化物对应水化物的酸性比溴的最高价氧化物对应水化物的酸性________(填“强”或“弱”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种常见的金属单质,A的焰色为黄色;B为红色固体,锈蚀时变为绿色;C在空气中加热熔化但不滴落;D在氧气中燃烧,火星四射,生成黑色固体。
根据以上信息回答下列问题:
(1)写出对应化学式:A________,B________,C________,D________。
(2)写出下列化学方程式:
①A在空气中燃烧_______________________________________;
②B与AgNO3 溶液:_________________________________;
③C与氢氧化钠溶液:___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列填空:
(1)要使 NH3 与 CH4 含相同数目的 H 原子,则 NH3 和 CH4 的物质的量之比为_______。
(2)19g 某二价金属氯化物(ACl2)中含有 0.4mol Cl, ACl2 的化学式是_____。
(3)在标准状况下,V L H2 中含有 N 个氢分子,则阿伏加德罗常数为_____mol-1。
(4)实验室某盐酸试剂的密度为 1.19g/mL,质量分数为 36.5%,则该盐酸的物质的量浓度为_____mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以Ni的氧化物作催化剂,将丙烯氨氧化制得丙烯腈(CH2=CHCN),然后以H3PO4-K3PO4等作为电解质溶液,电解丙烯腈制已二腈。已知总反应的化学方程式为:4CH2=CHCN+2H2O![]() O2↑+2NC(CH2)4CN。
O2↑+2NC(CH2)4CN。
(1)基态Ni原子价层电子的轨道表达式为_______;在上述总反应的化学方程式中所涉及到的各元素中,电负性由小到大的顺序为_______。
(2)PO43-的空间构型是_______,CH2=CHCN中碳原子的杂化方式为_______ 。
(3)NC(CH2)4CN分子中σ键与π键数目之比为_______。
(4)已知K3PO4是离子晶体,写出其主要物理性质_____(写出2条即可)。
(5)反应中核心元素碳有金刚石、石墨等多种同素异形体。设石墨晶体中碳碳键的键长为am,金刚石晶体中碳碳键的键长为bm,则a____b(填“>”、“=”或“<”),原因________。
(6)金刚石的晶胞结构如下图1所示,已知ZnS晶胞与金刚石晶胞微粒排列方式相同,若图中a为Zn2+,则S2-处于ZnS晶胞中的位置为_________。

(7)石墨烯中部分碳原子被氧化后,转化为氧化石墨烯(如图2所示)
①石墨烯转化为氧化石墨烯时,1号C与相邻C原子间键能的变化是___(填“变大”、“变小”“不变”)。
②石墨烯具有很大的比表面积,可用于制超级电容器。若石墨烯中碳碳键的键长为am,12g单层石墨烯的单面理论面积约为_______m3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如下图所示装置可以完成一系列实验(图中夹持装置已略去)

请回答下列问题:
Ⅰ. 若气体a是Cl2,装置A、B、C中的试剂依次为: FeCl2溶液、淀粉KI溶液、石蕊溶液。
(1)A溶液由浅绿色变为棕黄色,反应的离子方程式为_________________________________。
(2)B瓶中的淀粉KI溶液变为蓝色,反应的离子方程式为______________________________。
(3)C瓶中的现象为_______________________________________________________________。
(4)D装置中试剂为_______________________________________________________________。
II.若气体a是SO2,装置A、B、C中的试剂依次为:品红溶液、酸性高锰酸钾溶液、氢硫酸(硫化氢的水溶液)。
(1)A瓶中品红和B瓶中酸性高锰酸钾溶液均褪色,其中体现了SO2漂白性的是 _____(填写序号A或B)。
(2)C瓶中产生淡黄色沉淀, 反应的化学方程式_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com