
【题目】(1)根据反应8NH3+3Cl2![]() 6NH4Cl+N2,回答下列问题:
6NH4Cl+N2,回答下列问题:
①该反应中氧化剂是______________,氧化产物是___________________。
②该反应中被氧化的物质与被还原的物质物质的量之比为________________。
(2)某一反应体系中存在下列6种物质:NO、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O。已知存在下列转化关系:HNO3→NO,请完成下列各题:
①该反应的氧化剂是__________,还原剂是___________。
②该反应中1 mol氧化剂____________(填“得到”或“失去”)____________mol电子。
③当有0.1 mol HNO3被还原,此时生成标准状况下NO的体积是__________L。
④请把各物质填在下面空格处,需配平:
□______+□______=□______+□______+□______+□
【答案】Cl2 N2 2∶3HNO3FeSO4得到32.244HNO3+3FeSO4![]() Fe(NO3)3+Fe2(SO4)3+NO↑+2H2O
Fe(NO3)3+Fe2(SO4)3+NO↑+2H2O
【解析】
(1)①在氧化还原反应8NH3+3Cl2![]() 6NH4Cl+N2中,氮元素化合价升高,被氧化,NH3作还原剂,N2是氧化产物;氯元素化合价降低,被还原,作氧化剂,NH4Cl是还原产物;故该反应的氧化剂是Cl2,还原剂是NH3;②若有8 mol NH3参与反应,则2 mol NH3被氧化,3 mol Cl2被还原,因此该反应中被氧化的物质与被还原的物质物质的量之比为2∶3;
6NH4Cl+N2中,氮元素化合价升高,被氧化,NH3作还原剂,N2是氧化产物;氯元素化合价降低,被还原,作氧化剂,NH4Cl是还原产物;故该反应的氧化剂是Cl2,还原剂是NH3;②若有8 mol NH3参与反应,则2 mol NH3被氧化,3 mol Cl2被还原,因此该反应中被氧化的物质与被还原的物质物质的量之比为2∶3;
(2)①由于反应中存在转化关系:HNO3→NO,因此氮元素化合价降低,被还原,HNO3为氧化剂,NO为还原产物;因此铁元素一定是化合价升高,被氧化,FeSO4是还原剂,Fe(NO3)3和Fe2(SO4)3是氧化产物;故该反应的氧化剂是HNO3,还原剂是FeSO4;②1 mol氧化剂得到3 mol e;③当有0.1 mol HNO3被还原,根据原子守恒可知,生成NO的物质的量为0.1 mol,标准状况下的体积为![]() ;④根据得失电子守恒,并结合原子守恒,可以配平化学方程式:4HNO3+3FeSO4
;④根据得失电子守恒,并结合原子守恒,可以配平化学方程式:4HNO3+3FeSO4![]() Fe(NO3)3+Fe2(SO4)3+NO↑+2H2O 。
Fe(NO3)3+Fe2(SO4)3+NO↑+2H2O 。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质中,固定容器中,无论以何比例混合,其密度都不变的是
A. CH4 和 C2H4 B. C3H6和 CO2
C. C2H6和 C2H4 D. CO和C2H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维尔纳配合物M是一种橙黄色单斜晶体,该晶体以浓氨水、双氧水、CoCl2·6H2O、NH4Cl为原料在加热条件下通过活性炭的催化来合成。为探究该晶体的组成,设计了如下实验:
步骤一,氮的测定:准确称取一定量橙黄色晶体,加入适量水溶解,注入下图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品中的氨全部蒸出,用500.00mL7.0mol/L的盐酸溶液吸收,吸收结束后量取吸收液25.00mL,用2.00mol/L的NaOH溶液滴定过量的盐酸,终点消耗NaOH溶液12.50mL。
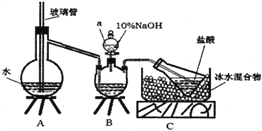
步骤二,氯的测定:准确称取橙黄色晶体wg,配成溶液后用AgNO3标准溶液滴定,以K2CrO4溶液为指示剂,至出现淡红色沉淀不再消失为终点(Ag2CrO4为砖红色沉淀)。
(1)上述装置A中,玻璃管的作用是________;装置B中仪器a的名称为_________。
(2)装置A、B三脚架处应放置一个酒精灯作为热源,酒精灯应放置在____(填“A”或“B”)处。
(3)步骤一所称取的样品中含氮的质量为_________g。
(4)有同学提出装置C中所用盐酸的浓度过大易挥发,会造成测得氮的含量结果将_______(填“偏高”、“偏低”或“无影响”);冰水混合物的作用是___________。
(5)测定氯的过程中,使用棕色滴定管的原因是_________;出现浅红色沉淀时,若溶液中c(CrO42-)=0.0025mol/L,通过计算说明该实验可以使用K2CrO4溶液为指示剂的原因______(呈现计算过程)。已知:Ksp(Ag2CrO4)=1.0×10-12Ksp(AgCl)=1.8×10-10
(6)经上述实验测定,配合物M中钴、氮、氯的物质的量之比为1:6:3,其中氮元素以氨的形式存在。制备M的化学方程式为_____________________,其中双氧水的作用是__________;制备M的过程中温度不能过高的原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于漂白粉的叙述正确的是( )
A.漂白粉的有效成分是Ca(ClO)2和CaCl2
B.漂白粉在空气中久置后会变质失效
C.漂白粉的有效成分Ca(ClO)2不稳定,易分解
D.在使用漂白粉时要加盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两个体积相同的容器,一个盛有NO,另外一个盛有N2和O2,在标准状况下两容器内的气体一定具有相同的( )
①原子总数;②质子总数;③分子总数;④质量
A.①②B.②④C.②③D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某HNO3和Fe(NO3)3的混合溶液中逐渐加入铁粉,产生无色气体,该气体遇空气变红棕色,溶液中Fe2+浓度和加入Fe粉的物质的量之间的关系如下图所示,则原稀溶液中HNO3和Fe(NO3)3的物质的量浓度之比为( )

A. 4∶1 B. 3∶1 C. 2∶1 D. 1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁有许多重要的化合物,除中学化学常见的三种氧化物和两种氢氧化物外,还有许多盐。FeSO4·7H2O是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子Cr2O![]() )进行处理。
)进行处理。
(1)绿矾除用铁粉与硫酸反应生成外,工业上还可用空气、水、黄铁矿(主要成分为FeS2)来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:
________________________________________________________________________。
(2)试配平:________Fe2++________Cr2O![]() +________===________Fe3++________Cr3++________H2O
+________===________Fe3++________Cr3++________H2O
(3)若该废水经处理后Cr3+的含量为1×10-2 mol·m-3,理论上83.4 kg绿矾可以处理该废水________吨(已知废水的密度为1 g·cm-3)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种生活中常用的食品添加剂,但使用时必须严格控制其用量。某兴趣小组将下图装置连接起来制备NaNO2(装置可重复使用,A中加热装置已略去)。

兴趣小组查阅资料可知:
①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+;
③在酸性条件下NaNO2能把I-氧化为I2,NO2-被还原为NO;Na2S2O3与I2的反应为2Na2S2O3+I2=Na2S4O6+2NaI
(1)连接装置的顺序为________。
(2)装置A三颈烧瓶中发生反应的化学方程式为______________;为保证制得的亚硝酸纯度,装置B中盛放的试剂可能是_________(填序号)。
A.P2O5 B.碱石灰 C.无水CaCl2 D.生石灰
(3)C装置的目的是_____________;E装置的作用是_____________。
(4)利用NaNO2的氧化性来测定其纯度的步骤是:准确称取mgNaNO2样品放人锥形瓶中,加适量水溶解,再加过量clmol·L-lKI溶液VlmL和几滴淀粉溶液,然后滴加稀硫酸,用c2mol·L-1Na2S2O3溶液滴定消耗V2mL。
①滴定终点的判断方法是____________;②NaNO2的质量分数__________%(写出表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一硝酸盐晶体,其化学式为M(NO3)xnH2O,相对分子质量为242g/mol, 取1.21g该晶体溶于水,配成100mL溶液,将此溶液倒入下图所示装置中,用石墨作电极进行电解,当有0.01mol电子通过电极时,溶液中的金属阳离子全部析出。在A极得到金属0.32g.下列说法正确的是( )

A. 金属M的摩尔质量为64 B. x=4
C. n=3 D. C极发生还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com