
�ȼҵ�IJ���NaOH�벻ͬ���ʷ�Ӧ�������ɲ�ͬ���Ρ���֪������,Ũ�Ⱦ�Ϊ0.1 mol��L-1��4��������Һ��pH���±�:
| ���� | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
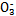 )>c(S
)>c(S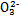 )>c(OH-)
)>c(OH-)  ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ij�¶��£���һ�����0.1 mol/L�İ�ˮ����εμ�0.1mol/L�����ᣬ��Һ��pH��pOH[ע��pOH��-lgc��OH����]�ı仯��ϵ��ͼ��ʾ��������˵���д������
| A��M����ʾ��Һ��c( NH4��)��c��Cl���� |
| B��Q����ʾ��Һ�ĵ�������ǿ��M�� |
| C��Q�����������������ڰ�ˮ����� |
| D��M���N����ʾ��Һ��ˮ�ĵ���̶���ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������Һ����Ũ�ȹ�ϵһ����ȷ����
| A����pH=5��H2SO4��Һϡ��1��103��,c(H+):c(SO42-)=2:1 |
B������������Ƶ�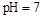 �Ļ����Һ��:c(CH3COO-)+c(CH3COOH)<c(Na+) �Ļ����Һ��:c(CH3COO-)+c(CH3COOH)<c(Na+) |
C��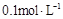 ���������Һ��:c(NH4+)+c(H+)��c(SO42-)+c(OH-) ���������Һ��:c(NH4+)+c(H+)��c(SO42-)+c(OH-) |
| D��������pH=4��NaHC2O4��Һ��:c(H2C2O4)<c(C2O42��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ɷ��Ǹ��л�ѧѧϰ���õķ���֮һ��ij��ѧ�о���ѧϰС����ѧϰ�ˡ���ѧ��Ӧԭ���������������µĹ����ܽ������ȷ����
�ٳ����£�pH��3�Ĵ�����Һ��pH��11��NaOH��Һ�������ϣ�����c (Na+) + c(H+)��c(OH��) + c(CH3COO��)
�ڶ��ѽ�����ѧƽ���ij���淴Ӧ�����ı�����ʹ��ѧƽ��������Ӧ�����ƶ�ʱ��������İٷֺ���һ������
�۳����£�AgCl��ͬ���ʵ���Ũ�ȵ�CaCl2��NaCl��Һ�е��ܽ����ͬ
�ܳ����£���֪�������ƽ�ⳣ��ΪKa�������ˮ��ƽ�ⳣ��ΪKh��ˮ�����ӻ�ΪKw��
����Ka��Kh��Kw
�ݵ�⾫��ͭʱ���������Һ��ͭ����Ũ�Ȳ��� ��
| A���٢� | B���٢ڢ� | C���٢ڢܢ� | D���٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����£���c1mo1/L�Ĵ�����Һ�еμ�ͬ�����c2 mo1/L������������Һ��������Һ��pH=7����
| A�����ǡ���к� | B��c1=c2 |
| C�����˷�̪��Һ��dz��ɫ | D��������Һc(Na+)=c(CH3COOһ) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��H2O+CH3COO- CH3COOH+OH-��ƽ���У�Ҫʹƽ�������ƶ���Ӧ��ȡ�Ĵ�ʩ��
CH3COOH+OH-��ƽ���У�Ҫʹƽ�������ƶ���Ӧ��ȡ�Ĵ�ʩ��
| A������NaOH���� | B����������� | C������ѹǿ | D�������¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����£���0.1 mol��L-1����������Һ��0.06 mol��L-1������Һ�������ϣ��û����Һ��pH����
| A��1.7 | B��2.0 | C��12.0 | D��12.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
25 ��ʱ��0.1 mol Na2CO3�����������õ�һ�����Ϊ1 L����Һ����Һ�в�������pH�Ĺ�ϵ��ͼ��ʾ�������й���Һ������Ũ�ȹ�ϵ��������ȷ���� (����)��
| A��W����ʾ����Һ�У�c(Na��)��c(H��)��2c(CO32��)��c(OH��)��c(Cl��) |
| B��pH��4����Һ�У�c(H2CO3)��c(HCO3��)��c(CO32��)<0.1 mol��L��1 |
| C��pH��8����Һ�У�c(H��)��c(H2CO3)��c(HCO3��)��c(OH��)��c(Cl��) |
| D��pH��11����Һ�У�c(Na��)>c(Cl��)>c(CO32��)>c(HCO3��)>c(H2CO3) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������pH��6�������pH��6��NH4Cl��Һ��������ˮ�������c(H��)�ֱ�Ϊx mol/L��y mol/L����x��y�Ĺ�ϵ��( )
| A��x��y | B��x >y | C��x��10��2y | D��x��102y |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com