
【题目】金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下密闭容器中用H2还原WO3可得到金属钨,其总反应为: WO3(s)+3H2(g) ![]() W (s) +3H2O (g) 请回答下列问题:
W (s) +3H2O (g) 请回答下列问题:
(1)上述反应的化学平衡常数表达式为。
(2)某温度下反应达到平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为;随着温度的升高,H2与水蒸气的体积比减小,则该反应为反应(填“吸热”或“放热”)。
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
温度 | 25 ℃~550 ℃~600 ℃~700 ℃ |
主要成分 | WO3 W2O5 WO2 W |
第一阶段反应的化学方程式为 ;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为 。
(4)已知:温度过高时,WO2(s)转变为WO2(g):
WO2(s)+2H2(g) ![]() W(s)+2H2O (g) H=+66.0 kJmol1
W(s)+2H2O (g) H=+66.0 kJmol1
WO2(g)+2H2(g) ![]() W(s)+2H2O (g) H=-137.9 kJmol1
W(s)+2H2O (g) H=-137.9 kJmol1
则WO2(s) ![]() WO2(g)的 H=。
WO2(g)的 H=。
(5)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W(s)+ 2 I2 (g) ![]() WI4 (g)。下列说法正确的有。
WI4 (g)。下列说法正确的有。
a.灯管内的I2可循环使用
b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
【答案】
(1)K= ![]()
(2)60%;吸热
(3)2WO3+H2 ![]() W2O5+H2O;1:1:4
W2O5+H2O;1:1:4
(4)△H=+203.9 kJmol1
(5)a、b
【解析】(1)WO3(s)+3H2(g) ![]() W(s)+3H2O(g)的平衡常数k=
W(s)+3H2O(g)的平衡常数k= ![]() ;
;
(2)由反应方程式知,消耗的H2与生成的水的物质的量相等,故H2的平衡转化率为 ![]() ×100%=60%,升高温度,H2与水蒸气的体积比减小,说明升温时平衡向右移动,故正反应为吸热反应;
×100%=60%,升高温度,H2与水蒸气的体积比减小,说明升温时平衡向右移动,故正反应为吸热反应;
(3)由表中主要成分与温度关系可知,第一阶段反应为WO3与H2反应是W2O5 , 同时还生成H2O,反应方程式为:2WO3+H2 ![]() W2O5+H2O,580℃时,温度介于550℃~600℃,固体为W2O5、WO2的混合物;假定有2molWO3 , 由2WO3+H2
W2O5+H2O,580℃时,温度介于550℃~600℃,固体为W2O5、WO2的混合物;假定有2molWO3 , 由2WO3+H2 ![]() W2O5+H2O、W2O5+H2
W2O5+H2O、W2O5+H2 ![]() 2WO2+H2O、WO2+2H2
2WO2+H2O、WO2+2H2 ![]() W+2H2O可知,三个阶段消耗的氢气的物质的量之比为1mol:1mol:2mol×2=1:1:4;
W+2H2O可知,三个阶段消耗的氢气的物质的量之比为1mol:1mol:2mol×2=1:1:4;
(4)已知:①WO2 (s)+2H2 (g) ![]() W (s)+2H2O (g);△H=+66.0kJmol-1②WO2 (g)+2H2
W (s)+2H2O (g);△H=+66.0kJmol-1②WO2 (g)+2H2 ![]() W (s)+2H2O (g);△H=-137.9kJmol-1
W (s)+2H2O (g);△H=-137.9kJmol-1
①-②得则WO2 (s) ![]() WO2 (g),故△H=66.0kJmol-1-(-137.9kJmol-1)=+203.9 kJmol-1;
WO2 (g),故△H=66.0kJmol-1-(-137.9kJmol-1)=+203.9 kJmol-1;
(5)由所给化学方程式知,挥发的W与I2结合形成气态WI4 , 由于气体运动的结果,WI4会与还没有挥发的W接触,在高温下WI4分解生成的W及I2 , 生成W附着在还没有挥发的W上,灯管内的I2可循环使用,故a、b对;灯管壁温度较低,WI4不会分解,故c错;升高温度,也能加快W与I2的反应速率,故d错;
故答案为:(1)![]() ;(2)60%,吸热;(3)2WO3+H2
;(2)60%,吸热;(3)2WO3+H2 ![]() W2O5+H2O,1:1:4;(4)+203.9 kJmol-1;(5)a、b
W2O5+H2O,1:1:4;(4)+203.9 kJmol-1;(5)a、b
(1)根据平衡常数的表达式进行书写即可;
(2)平衡转化率等于参与反应的量除以起始加入的量;结合温度对平衡移动的影响因素分析;
(3)写出反应过程的化学方程式,结合化学方程式进行计算;
(4)结合盖斯定律进行反应热;
(5)在不同的温度下, 反应进行的方向不同,结合具体发生的反应,进行分析即可。


科目:高中化学 来源: 题型:
【题目】有机化合物的结构可用键线式表示,如CH2═CHCH2Br可表示为 ![]() .则关于有机物
.则关于有机物 ![]() 的说法正确的有( )
的说法正确的有( )
A.与苯互为同分异构体
B.其二氯代物有3种 (不考虑立体异构)
C.分子中所有的碳原子在同一平面上
D.属于烯烃,是乙烯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与应用具有相对应关系的是
A.苯酚显弱酸性,可用于杀菌消毒
B.氢氧化铝受热易分解,可用于中和胃酸
C.KOH溶液呈碱性,可用于油脂的皂化
D.C2H4能使酸性高锰酸钾褪色,可用于果实的催熟
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分元素在元素周期表中位置,根据下列要求回答问题:
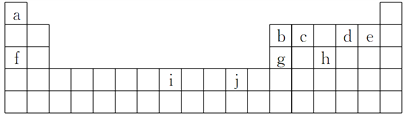
(1)下列关于Ca、97Bk(锫)、![]() Uus和
Uus和![]() Uus的说法中不正确的是____(填字母,下同)。
Uus的说法中不正确的是____(填字母,下同)。
A.117号元素的相对原子质量为293.5
B.![]() Uus和
Uus和![]() Uus互为同位素
Uus互为同位素
C. Ca、97Bk表示两种原子、两种元素
D.上述元素都位于长周期中
(2)根据元素周期表结构推知,117号元素在周期表中的位置是________。
A.第七周期第ⅣA族
B.第七周期第ⅦA族
C.第六周期第ⅣA族
D.第六周期第ⅦA族
(3)117号元素Uus属于________(填“金属元素”或“非金属元素”),它的气态氢化物稳定性比砹的气态氢化物稳定性________(填“强”或“弱”);它的最高价氧化物的化学式为________________。
(4)下列关于上述元素及其化合物的判断正确的是________(填字母)。
A.53I、55Cs和55Cs放射性元素变成其他元素,发生了化学变化
B.he3分子和ha3分子结构相同
C.j元素与d元素组成化合物的颜色相同
D.加碘食盐中“碘”不是碘53I
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、KHPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO3,则下列说法正确的是
A.H3PO2属于二元酸B.H3PO2属于三元酸
C.NaH2PO2属于酸式盐D.NaH2PO2属于正盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲测定烟雾中的SO2含量,可做下列实验:取100 L该烟雾(标准状况),通过盛放100 mL过氧化氢(H2O2)水溶液的吸收瓶,使它们充分反应,生成硫酸。在吸收后的水溶液中加入BaCl2溶液,生成白色沉淀,经测定其质量为11.65 g,则该烟雾中SO2的体积分数是( )
A. 1.12% B. 2.24%
C. 3.36% D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上测量SO2、N2、O2混合气体中SO2含量的装置如右图。反应管中装有碘的淀粉溶液。SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2 +2H2O==H2SO4+2HI
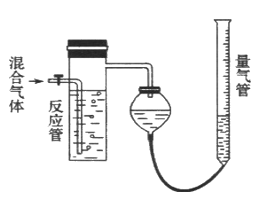
(1)混合气体进入反应管后,量气管内增加的水的体积等于__________的体积(填分子式)。
(2)反应管内的溶液蓝色消失后,没有及时停止通气,则测得的SO2含量_____(填“偏高”、“偏低”或“不受影响”)。
(3)反应管内的碘的淀粉溶液也可以用_______________代替(填写物质名称)。
(4)若碘溶液体积为V![]() mL,浓度为cmol·L
mL,浓度为cmol·L![]() 。N2与O2的体积为V
。N2与O2的体积为V![]() mL(已折算为标准状况下的体积)。用c、V
mL(已折算为标准状况下的体积)。用c、V![]() 、V
、V![]() 表示SO2的体积百分含量为:_________________。
表示SO2的体积百分含量为:_________________。
(5)将上述装置改为简易实验装置,除导管外,还需选的仪器为________(选下列仪器编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com