
【题目】依据氧化还原反应:2Ag++Cu=Cu2++2Ag,设计的原电池如图所示。
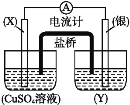
请回答下列问题:
(1)电极X的材料是___;电极X是原电池的___极;
(2)银电极发生的电极反应为___;
(3)今有2H2+O2![]() 2H2O反应构成燃料电池,则正极通的应是___;负极的电极反应式为___。
2H2O反应构成燃料电池,则正极通的应是___;负极的电极反应式为___。
【答案】Cu 负 Ag++e-=Ag O2 H2+2OH--2e-=2H2O
【解析】
根据总反应:2Ag++Cu=Cu2++2Ag,Cu元素的化合价由0价升至+2价,Cu作负极,发生氧化反应;Ag元素的化合价由+1价降至0价,Ag作正极,Ag+发生还原反应,据此分析解答。
(1)根据上述分析可知,Cu发生氧化反应,根据原电池中负极发生失电子的氧化反应,Cu应为原电池的负极,故答案为:Cu;负;
(2)银电极为电池的正极,正极上反应为Ag+得电子被还原成Ag,发生的电极反应为Ag++e-=Ag,故答案为:Ag++e-=Ag;
(3)由反应2H2+O2![]() 2H2O可知,电解质溶液为KOH,H化合价升高,H2在负极失去电子,电极反应式为H2+2OH--2e-=2H2O,O化合价降低,O2在正极得到电子,电极反应式为O2+4e-+2H2O===4OH-,故答案为:O2;H2+2OH--2e-=2H2O。
2H2O可知,电解质溶液为KOH,H化合价升高,H2在负极失去电子,电极反应式为H2+2OH--2e-=2H2O,O化合价降低,O2在正极得到电子,电极反应式为O2+4e-+2H2O===4OH-,故答案为:O2;H2+2OH--2e-=2H2O。


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】某常见微粒X的结构模型可表示为 (
(![]() 代表电子),下列有关X的说法正确的是( )
代表电子),下列有关X的说法正确的是( )
A.微粒X的组成元素不可能是第三周期元素
B.X的组成元素一定是氖元素
C.若X的组成元素原子的核电荷数为8,则X是![]()
D.若X的核内质子数比电子数多,则X最多有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.甘油醛(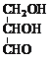 )和葡萄糖均属于单糖,互为同系物
)和葡萄糖均属于单糖,互为同系物
B.2,3,5,5四甲基3,3二乙基己烷的键线式为![]()
C.高聚物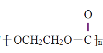 和
和![]() 均是缩聚产物,它们有共同的单体
均是缩聚产物,它们有共同的单体
D.将总物质的量为1 mol的水杨酸、1,2二氯乙烷和CH3NHCOOCH3的混合物与NaOH溶液充分反应,最多可以消耗2 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:①高锰酸钾 ②镁 ③氧气 ④氢氧化钠 ⑤硫酸 ⑥甲烷 ⑦![]() 胶体 ⑧硫酸铜
胶体 ⑧硫酸铜
(1)以上物质属于电解质的是_________,属于非电解质的是_______。(填序号)
(2)属于有机物的是__________。(填序号)
(3)鉴别胶体和溶液最简单有效的物理方法是_____;分离胶体和溶液常用的物理方法是_____。
(4)从上述物质中选出一种或两种为反应物,按下列反应类型各写一个反应化学方程式:
①化合反应:______;
②分解反应:______;
③置换反应:______;
④复分解反应:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.分子式 C8H10 的苯的同系物共有 3 种结构
B.![]() 与
与![]() 互为同系物
互为同系物
C.三联苯(![]() )的一氯代物有 4 种
)的一氯代物有 4 种
D.立方烷(![]() )经硝化可得到六硝基立方烷,其可能的结构有 3 种
)经硝化可得到六硝基立方烷,其可能的结构有 3 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写热化学方程式:
(1)25℃、101kPa条件下充分燃烧一定量的C2H2气体放出热量为1300kJ,经测定,将生成的CO2通入足量澄清石灰水中产生100g白色沉淀,写出表示C2H2气体充分燃烧的热化学方程式:___;
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有关微粒结构的表示或说法不正确的是( )
A.氮分子的电子式为::N:::N:
B.氨分子的空间构型为三角锥型,属于极性分子
C.白磷属于分子晶体,空间构型为正四面体,键角60°,是非极性分子
D.NH4+离子中的四个N—H键虽然形成方式不同,但键能、键长、键角都相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组探究稀HNO3、浓HNO3与铜的反应。
装置(尾气处理装置略) | 现象 |
| Ⅰ中开始无明显现象,渐有小气泡生成,越来越剧烈,液面上方出现浅红棕色气体,溶液呈蓝色。 |
Ⅱ中反应剧烈,迅速生成大量红棕色气体,溶液呈绿色。 |
(1)试管Ⅰ中Cu与稀HNO3反应的化学方程式是________。
(2)Ⅱ中反应的速率比Ⅰ中的快,原因是________。
(3)针对Ⅱ中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;

假设2:溶解了生成的NO2。
探究如下:取Ⅱ中绿色溶液,分为两等份。
①取一份于如图所示装置中,_______(填“操作”和“现象”),证实Ⅱ中溶解了NO2。
②向另一份溶液加入_____(填化学试剂),溶液变为蓝色。证实假设1不成立,假设2成立。
(4)对于稀HNO3与铜生成NO、浓HNO3与铜生成NO2的原因,提出两种解释:
解释1.HNO3浓度越稀,溶液中NO3-的数目越少,被还原时,每个NO3-从还原剂处获得较多电子的机会_____(填“增多”或“减少”),因此被还原为更低价态。
解释2.推测下列平衡导致了产物的不同,并通过如下实验证实了推测的合理性。
3NO2+H2O=2HNO3+NO

①B中盛放的试剂是________。
②C中盛放Cu(NO3)2和_________。
③该小组证实推测的合理性所依据的实验现象是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学在实验室研究Al与CuCl2溶液的反应.
实验操作 | 实验现象 |
|
|
(1)现象![]() 中的红色物质是 ______ .
中的红色物质是 ______ .
(2)经检验现象![]() 中的无色气体为氢气.
中的无色气体为氢气.
①甲认为Al与H+反应产生了氢气,用离子方程式表示溶液中存在大量H+的原因 ______.
②氢气从红色物质表面逸出的原因是 ______ .
(3)探究白色沉淀的化学成分.
查阅资料:Cu+可与浓氨水反应生成Cu(NH3)2+(无色),该无色物质在空气中易被氧化变为蓝色.
乙认为白色沉淀可能是CuCl,并通过实验证明其猜测正确,实验步骤如下:
a.取白色沉淀,充分洗涤;
b.向其中加入浓氨水,沉淀溶解得到无色溶液,将无色溶液分为两份;
c.取其中一份无色溶液![]()
d.将另一份无色溶液放置于空气中,一段时间后,溶液变为蓝色.
①步骤c的实验方案是 ______.
②用化学平衡移动原理解释CuCl溶于浓氨水的原因 ______.
(4)探究CuCl产生的原因.
①丙猜测可能是Cu与CuCl2溶液反应生成了CuCl,因为Cu具有 ______性.
②取Cu粉与1mol/LCuCl2溶液混合,无白色沉淀产生,丙再次分析Al与CuCl2溶液反应的实验现象,改进实验方案,证明了Cu与CuCl2溶液反应生成了CuCl,改进之处是 ______ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com