
【题目】金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为: WO3(s) + 3H2(g)![]() W (s) + 3H2O (g),请回答下列问题:
W (s) + 3H2O (g),请回答下列问题:
(1)在一定温度下进行上述反应,若反应容器的容积为0.5 L,2min后达到平衡,测得固体的质量减少了4.80 g,则H2的平均反应速率______;该反应的平衡常数表达式K=_____。
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为__________;随温度的升高,H2与水蒸气的体积比减小,则该反应为______(填“吸热”或“放热”) 反应。
(3)一定温度下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是________。
A.混合气体的总压强保持不变 B.v正(H20)= v正(H2)
C.混合气体的密度保持不变 D.混合气体的平均式量保持不变
(4)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2(g)![]() WI4(g)。下列说法正确的有__________。
WI4(g)。下列说法正确的有__________。
A.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.灯管内的I2可循环使用
【答案】0.3 mol/(L·min) ![]() 60% 吸热 C BD
60% 吸热 C BD
【解析】
(1)由氢气的消耗量与增重质量列关系式计算;反应的化学平衡常数K=![]() ;
;
(2)设氢气的起始体积为a,变化体积为x,由题意建立三段式计算;随温度的升高,H2与水蒸气的体积比减小,说明平衡向正反应方向进行;
(3)化学反应达到化学平衡,正逆反应速率相等,各物质的浓度保持不变;
(4)由所给化学方程式知,挥发的W与I2结合形成气态WI4,由于气体运动的结果,WI4会与还没有挥发的W接触,在高温下WI4分解生成的W及I2,生成W附着在还没有挥发的W上,灯管内的I2可循环使用。
(1)设反应消耗氢气的物质的量为x,由方程式可知WO3(s) + 3H2(g)![]() W (s) + 3H2O (g),氢气的消耗量与增重质量的关系为3mol:48g=xmol:4.8g,解得x=0.3,则H2的平均反应速率为
W (s) + 3H2O (g),氢气的消耗量与增重质量的关系为3mol:48g=xmol:4.8g,解得x=0.3,则H2的平均反应速率为![]() = 0.3 (mol/(L·min)),由化学方程式可知反应的化学平衡常数K=
= 0.3 (mol/(L·min)),由化学方程式可知反应的化学平衡常数K=![]() ,故答案为:0.3 (mol/(L·min));
,故答案为:0.3 (mol/(L·min));![]() ;
;
(2)设氢气的起始体积为a,变化体积为x,由题意建立如下三段式:
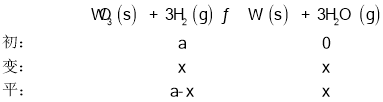
由H2与水蒸气的体积比为2:3可得(a-x):x=2:3,解得x=![]() ,则H2的平衡转化率为
,则H2的平衡转化率为![]() ×100%=60%;随温度的升高,H2与水蒸气的体积比减小,说明平衡向正反应方向进行,该反应为吸热反应,故答案为:60%;吸热;
×100%=60%;随温度的升高,H2与水蒸气的体积比减小,说明平衡向正反应方向进行,该反应为吸热反应,故答案为:60%;吸热;
(3)A、前后气体系数相等,“混合气体的总压强保持不变”不能作为平衡标志,故错误;
B、同向的,不是标志,故错误;
C、因不都是气体,虽体积不变,“混合气体的密度保持不变”只在平衡时,可做标志,故正确;
D、M=m/n, m和n始终不变,不是标志,故错误;
C正确,故答案为:C;
(4)A、温度升高,,WI4的分解速率加快,W和I2的化合速率加快,故错误;
B、高温下,WI4分解生成的W及I2,生成W附着在还没有挥发的W上,故正确;
C、灯管壁温度较低,WI4不会分解,寿命会降低,故错误;
D、由所给化学方程式知,挥发的W与I2结合形成气态WI4,由于气体运动的结果,WI4会与还没有挥发的W接触,在高温下WI4分解生成的W及I2,生成W附着在还没有挥发的W上,灯管内的I2可循环使用,故正确;
BD正确,故答案为:BD。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
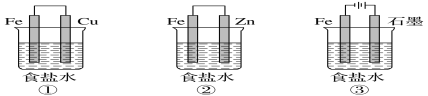
为防止金属Fe被腐蚀,可以采用上述________(填装置序号)装置原理进行防护;装置③中总反应的离子方程式为_________。
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为__________。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
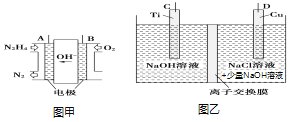
①上述装置中D电极应连接肼燃料电池的________极(填“A”或“B”)。
②该电解池的阳极反应式为_______。
③当反应生成14.4 g Cu2O时,至少需要肼________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求回答下列问题:
(1)25 ℃时,向纯水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为_____________,由水电离出的c(OH-)=________mol·L-1。
(2)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式 | 电离常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25 ℃时,有等pH的a.NaCN溶液、b.Na2CO3溶液和c.CH3COONa溶液,三溶液的浓度由大到小的顺序为___________________________。(用a b c表示)
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为_________。
(3)室温时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
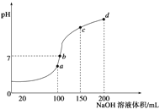
试分析图中a、b、c、d四个点,水的电离程度最大的是________;在b点,溶液中各离子浓度由大到小的排列顺序是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A是制取溴苯的实验装置,B,C是改进后的装置,请仔细分析,对比三个装置,回答以下问题:
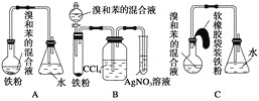
(1)写出三个装置中所共同发生的两个反应的化学方程式:_____;_____。写出B中盛有AgNO3溶液的试管中所发生反应的化学方程式:_____。
(2)装置A和C均采用了长玻璃导管,其作用是_____。
(3)按装置B,C装好仪器及药品后要使反应开始,应对装置B进行的操作是_____;应对装置C进行的操作是____。
(4)装置B,C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作。A装置中这一问题在实验中造成的后果是_____。
(5)B中采用了洗气瓶吸收装置,其作用是____,反应后洗气瓶中可能出现的现象是_____。
(6)B装置也存在两个明显的缺点,使实验的效果不好或不能正常进行。这两个缺点是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有一定量NaOH溶液中,逐渐通入一定量 CO2,充分反应后,将溶液在一定条件下进行蒸干,得到晶体物质。其质量m 与通入气体体积V(CO2)的关系如图。如下说法正确的是
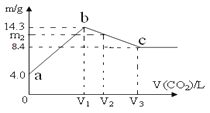
A.晶体物质:a点是NaOH;b点是Na2CO3;c点是NaHCO3
B.a→b 和 b→c 两段过程得到的晶体,含有相同的晶体物质
C.整个过程中的溶液,一定存在恒等式:c(Na+)+c(H+)=c(OH-)+c(CO32-)+c(HCO3-)
D.若通入V2=1.344 L (标况) 气体,则m2=13.12 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式为
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH2=-393.5kJ·mol-1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH3=-285.8kJ·mol-1
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的ΔH为( )
A.-488.3kJ·mol-1
B.-191kJ·mol-1
C.-476.8kJ·mol-1
D.-1549.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:-CHO+(C6H5)3P=CH-R -CH=CH-R + (C6H5)3P=O,R代表原子或原子团,W是一种有机合成中间体,结构简式为:HOOC-CH=CH-CH=CH-COOH,其合成方法如下:
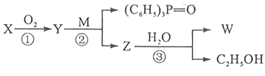
其中,![]() 分别代表一种有机物,合成过程中其他产物和反应条件已略去。
分别代表一种有机物,合成过程中其他产物和反应条件已略去。
X与W在一定条件下反应可以生成酯N,N的相对分子质量为168。
请回答下列问题:
(1)W能发生反应的类型有__________。(填写字母编号)
A.取代反应 | B.水解反应 | C.氧化反应 | D.加成反应 |
(2)写出X与 W在一定条件下反应生成N的化学方程式:___________________。
(3)写出含有3个碳原子且不含甲基的X的同系物的结构简式_________________
(4)写出第②步反应的化学方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各对物质中,互为同系物的是( )
A.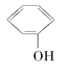 与
与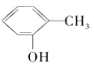
B.HCOOCH3与CH3CH2COOH
C.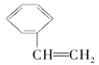 与CH3-CH=CH2
与CH3-CH=CH2
D.C6H5OH与C6H5CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①25 ℃时,NaHCO3溶液呈碱性,原因是_________水解引起的(填“Na+”或 “HCO3-”);
②常温下,0.0100 mol/L盐酸的pH=__________
③用0.0100 mol/L盐酸滴定未知浓度的NaOH溶液,酚酞作指示剂,滴定终点时, 溶液的颜色由红色变为__________(填“蓝色”或“无色”),且半分钟内保持不变。
(2)在某密闭容器中进行可逆反应:FeO(s)+CO(g)![]() Fe(s)+CO2(g) ΔH>0平衡常数表达式为K=c(CO2)/c(CO)。
Fe(s)+CO2(g) ΔH>0平衡常数表达式为K=c(CO2)/c(CO)。
①反应达到平衡后,向容器中通入CO,化学平衡向____方向移动(填“正反应”或“逆反应”);
②若升高温度,平衡常数K__________(填“增大”、“减小”或“不变”);
③查阅资料得知1 100℃时K=0.263。某时刻测得容器中c(CO2)=0.025 mol/L,c(CO)=0.10 mol/L,此时刻反应__________平衡状态(填“达到”或“未达到”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com