
��һ���¶��£�������X������Y��0.16mol����10L�����ܱ������У�������Ӧ
X(g)��Y(g)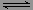 2Z(g) ��H��0��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ����������
2Z(g) ��H��0��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ����������
����
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ����
A�����¶��´˷�Ӧ��ƽ�ⳣ��K��1.44
B�������������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰ��(��)����(��)
C����Ӧǰ2min��ƽ��������(Z)��2.0��10��3mol��L��1��min-1
D�������������䣬�ٳ���0.2mol Z��ƽ��ʱX�������������
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������������(����)
A��SO2ʹ��ˮ��ɫ����ϩʹKMnO4��Һ��ɫ��ԭ����ͬ
B���Ʊ���������ʱ�����ȵ�NaOH��Һ�ռ������Գ�ȥ���е�����
C���ñ���ʳ��ˮ���ˮ����ʯ��Ӧ�����Լ�����Ȳ�IJ�������
D����AgNO3��Һ���Լ���KCl��KI
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ������ҪO��1 mol��L NaOH��Һ450 mL��0��5mol��l������Һ480 mL��������������Һ����������ش��������⣺
(1)��ͼ��ʾ��������������Һ��Ҫ���� (���ֺ�)������������Һ�����õ��IJ��������� (����������)��
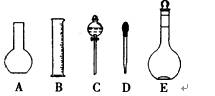
(2)���в����У�������ƿ���߱��Ĺ����� ��
A������һ�����ȷŨ�ȵı���Һ
B��������Һ
C����������Ũ�Ⱥ�����ı���Һ
D��ϡ��ijһŨ�ȵ���Һ
E����ȡһ�������Һ��
(3)���ݼ�����������ƽ��ȡNaOH������Ϊ g����ʵ����������������ȷ��������ʱ���ӿ̶��ߣ���������ҺŨ�� (����ڡ������ڡ���С�ڡ�)O��1 mol��l����NaOH��Һ��ת��������ƿʱ������������������Ҫ��β����� ��(4)���ݼ����֪��������������Ϊ98�����ܶ�Ϊl.84 g��cm3��Ũ��������Ϊ ml�����ʵ������10 mL��15 mL��20 mL��Ͳ��Ӧѡ�� mL����Ͳ��á����ƹ������������ձ��н�Ũ�������ϡ�ͣ�ϡ��ʱ����������
(5)���в�����ʹ���Ƶ�NaOH��ҺŨ��ƫ�� ���ǡ�
A������ֽ����NaOH
B��ѡ�õ�����ƿ������������ˮ
C������ҡ�Ⱥ�Һ���½����ּ�ˮ���̶���
D���������ƹ����У�����ƿ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪H2(g)��Br2(l)��2HBr(g) ��H����72kJ��mol��1������1mol Һ���Br2(g)��Ҫ����
������Ϊ30kJ����������������±���

�����aΪ
A��404 B��260 C��230 D��200
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪���и��鷴Ӧ�ķ�Ӧ�P�¶ȣ���Ӧ��ʼʱ���ų�H2�����������ǣ�����
�����ʾ�Ϊ��Ӧ�
| ��� | ��������С����״��ͬ�ķ�ĩ�����ʵ��� | ���Ũ�ȼ���� | ��Ӧ�¶�/�� |
| A | Mg 0.1 mol | 3 mol/L������10 mL | 60 |
| B | Mg 0.1 mol | 3 mol/L������10 mL | 30 |
| C | Fe 0.1 mol | 3 mol/L������10 mL | 60 |
| D | Mg 0.1 mol | 3 mol/L������10 mL | 60 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ҵ�Ͽ�����ú���������CO��H2���ϳɶ����ѣ�CH3OCH3��ͬʱ��
�ɶ�����̼����������Ӧ���£�
�� 2H2 (g)��CO(g)  CH3OH (g) ��H�� ��90.8 kJ��mol-1
CH3OH (g) ��H�� ��90.8 kJ��mol-1
�� 2CH3OH(g)  CH3OCH3(g)��H2O(g) ��H�� ��23.5 kJ��mol-1
CH3OCH3(g)��H2O(g) ��H�� ��23.5 kJ��mol-1
�� CO(g)��H2O(g)  CO2 (g)��H2(g) ��H�� ��41.3 kJ��mol-1
CO2 (g)��H2(g) ��H�� ��41.3 kJ��mol-1
��1���ܺϳɷ�Ӧ���Ȼ�ѧ����ʽΪ ��
��2��һ�������µ��ܱ������У������ܷ�Ӧ�ﵽƽ��ʱ��Ҫ���CO��ת���ʣ���
�Բ�ȡ�Ĵ�ʩ��_____������ĸ���ţ���
A�����¸�ѹ B��������� C������CO2��Ũ��
D������CO��Ũ�� E�������������
��3����Ӧ��2CH3OH(g) CH3OCH3(g)��H2O(g)�����ֲ�ͬ�����½��У���Ӧ����
CH3OCH3(g)��H2O(g)�����ֲ�ͬ�����½��У���Ӧ����
Ϊ��ͬ�ĺ����ܱ�������CH3OCH3��H2O��ʼŨ��Ϊ0����CH3OH(g)��Ũ��
��mol/L���淴Ӧʱ�䣨min���ı仯������±���
| ʵ�� ��� | �¶� Ũ�� ʱ�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800�� | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800�� | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800�� | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820�� | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
�����������ݣ����������գ�
��ʵ��1����Ӧ��10��20����ʱ������CH3OH(g)��ʾ��ƽ������Ϊ ��
��ʵ��2��CH3OH(g)�ij�ʼŨ��c2�� mol/L����Ӧ��20���Ӿʹﵽƽ�⣬
���Ʋ�ʵ��2�л������������� ��
����ʵ��3�ķ�Ӧ����Ϊv3��ʵ��1�ķ�Ӧ����Ϊv1����v3 v1�����������������c3�� mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���в��������ֻ�����Ӧ���ͣ�������������ԭ��Ӧ���ǣ� ����
|
C��Cu2(OH)2CO3==2CuO+ H2O+CO2�� D��4Fe(OH)2+O2+2H2O=4Fe(OH)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�밴Ҫ����գ�
�� ����ʵ��������ʵ����ʵ��������ȷ����______________������ţ�
�� ��ϡHNO3��ϴ����������Ӧʵ����Թܣ�
�� ����Ũ�����Ũ����Ļ����ʱ����Ũ�����������������뵽Ũ�����У������Ͻ��裻
�� �ü�ʽ�ζ�����ȡ20.00mL 0.1000mol/L ��KMnO4��Һ��
�� ��������ƽ��ȡ10.50g�����NaCl���壻
�� ������������Һմ��Ƥ���ϣ������þƾ���ϴ��
�� ������������Fe(CrO2)2��Na2CO3�������
�� ����ڵ�NaOHϡ��Һ�еμ�FeCl3������Һ�����Ʊ�Fe(OH)3���壻
�� ����Al2(SO4)3��Һʱ������������ϡ���ᡣ
�� Ϊ��ȷ���Ҵ����ӵĽṹ��ʽ��CH3��O��CH3����CH3CH2OH��ʵ����������ͼ��ʾ��ʵ��װ�ã��ⶨ�Ҵ����Ʒ�Ӧ����H��0��������������������ݴ˼����Ҵ���������������Ʒ�Ӧ����ԭ�ӵ���Ŀ���Իش��������⣺
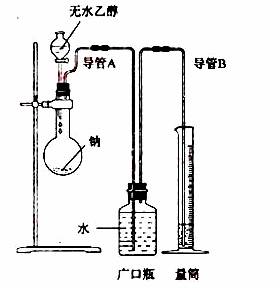
�� ָ��ʵ��װ���еĴ���_________________________��
�� ��ʵ�����ú�������ˮ���Ҵ�������ͬ��������ˮ�Ҵ�����ͬ�����£���õ����������__________(�ƫ����ƫС�����䡱)��
�� ��ָ����ʹ��ʵ�鰲ȫ��˳�����еĹؼ�ʵ�鲽�裨����ָ�������ؼ����裩____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��һ����ȡ������������Ϊԭ�Ͻ����ض���Ӧ��װ�ã�
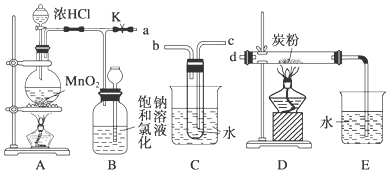
������������ܽ�ȣ����³�ѹ�£�1�����ˮ���ܽ�CO2��Cl2��HCl�ֱ�Ϊ1��2��500�����
��1��A����������װ�ã����еĻ�ѧ��Ӧ����ʽΪ���� ������������������
��2��Ҫ��Cװ�ý���B��D֮�䣬��ȷ�Ľӷ���a��______��______����d
��3��ʵ�鿪ʼʱ���ȵ�ȼA���ľƾ��ƣ�������K����Cl2��������װ�ã��ٵ�ȼD���ƾ��ƣ�������Eװ�á�Cl2ͨ��Cƿ���ٽ���D��Dװ�õ�Ӳ�ʲ�������ʢ��̿�ۣ�����������ԭ��Ӧ�������ΪCO2��HCl���塣��д��D�з�Ӧ�Ļ�ѧ����ʽ������������������ ������������������������װ��C���������������������������������������� ��������������������������Ϊ��ʹCװ�÷��Ӹ��õ����ã������ձ��м���Ũ���ᣬ����Ũ����������������� ���������� ����
��4����A��B��C��D��Eװ������һ����Ҫ�Ľ���˵����Ҫ�Ľ�������____________________________________________________________________��
��5��D����Ӧ��Ϻر�����K����ȥ�ƾ��ƣ����������ȵ����ã�A������Cl2��������ʱB������������������________________________ ����������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com