
【题目】下列物质不可能是乙烯加成产物的是
A. CH3CH3B. CH3CHCl2C. CH3CH2OHD. CH3CH2Br
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的NaOH溶液时,能造成所配溶液浓度偏低的原因是( )
A.定容时俯视液面
B.未洗涤烧杯和玻璃棒
C.容量瓶未干燥
D.转移溶液前溶液未冷却至室温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】止咳酮(F)具有止咳、祛痰作用.其生产合成路线如下:已知:CH3COOH3COOC3H3+CH3Cl ![]()
![]() +HCl
+HCl 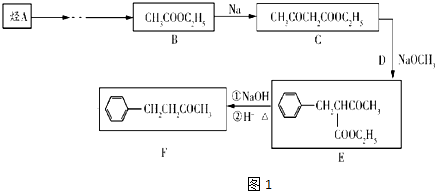
(1)E中含有的官能团名称为
(2)已知D为氯化烃,写出C+D→E的化学方程式 , 其反应类型为
(3)1molH2加成后生成有机物M,满足下列条件的M的同分异构体有种.①苯的二元取代物
②1molBr2的浓溴水完全发生反应,写出满足上述条件且取代基无支链的一种结构 .
(4)利用题给相关信息,以葡萄糖为原料,合成目标高分子化合物的流程图如图2.请将空白处过程补充完整.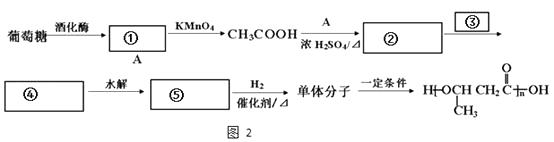
①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物燃料电池是以有机物为燃料,直接或简介利用酶作为催化剂的一类特殊的燃料电池,其能量转化效率高,是一种真正意义上的绿色电池.其工作原理如图所示.下列有关说法正确的是( ) 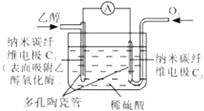
A.O2在C2电极上得电子,被氧化
B.电子由C2极经外电路流向C1极
C.每转移6mole﹣1 , 理论上生成22.4LCO2
D.C1极的电极反应式为:C2H5OH+3H2O﹣12e﹣1=2CO2+12H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道科研人员应用计算机模拟出结构类似C60的物质N60 。已知:①. N60分子中每个氮原子均以N—N键结合三个N原子而形成8电子稳定结构;②.N—N键的键能为167 kJ/mol,N≡N键的键能为942kJ/mol。试回答下列问题:
(1)N60组成的晶体为_______ 晶体,其熔、沸点比N2的 _______(高或低),其原因是__________ 。
(2)1mol N60 分解成N2时吸收或释放的热量为________________kJ。
(3)常温常压下,向50 mL 0.4mol/L的NaOH溶液中加入过量的稀H2SO4,测得放热 a kJ.写出上述反应的热化学方程式:____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一无色未知溶液中检验出有Ba2+、Ag+ , 同时又测得其酸性很强.某学生还要鉴定此溶液中是否大量存在①Cu2+ ②Al3+ ③Cl﹣ ④NO ![]() ⑤NH4+ ⑥CO
⑤NH4+ ⑥CO ![]() ⑦S2﹣ ⑧Mg2+ ⑨Fe3+ , 而事实上有部分离子不用鉴定就能加以否定,你认为不必鉴定的是( )
⑦S2﹣ ⑧Mg2+ ⑨Fe3+ , 而事实上有部分离子不用鉴定就能加以否定,你认为不必鉴定的是( )
A.③⑤⑥⑦⑨
B.①③⑥⑦⑨
C.③④⑦⑧⑨
D.①②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向10mL 0.1molL﹣1CH3COONa溶液中,不断通入HCl后,CH3COO﹣与CH3COOH浓度的变化趋势如图所示(不考虑溶液体积变化),下列说法不正确的是( ) 
A.M点溶液中水的电离程度比原溶液小
B.在M点时,c(H+)﹣c(OH﹣)=(100a﹣5.0×10﹣2) mol/L
C.随着HCl的通入, ![]() 值不断减小
值不断减小
D.当n(HCl)=1.0×10﹣3mol时,溶液中c(Na+)>c(Cl﹣)>c(CHCOO﹣)>c(H+)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】共聚法可改进有机高分子化合物的性质,高分子聚合物P的合成路线如下: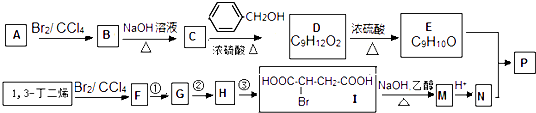
(1)B的名称为 , E中所含官能团的名称为 .
(2)F可以使溴水褪色,其中②的反应试剂是 , ③的反应类型是 .
(3)下列说法正确的是(填字母序号).a.C可与水任意比例混合
b.A与1,3一丁二烯互为同系物
c.由I生成M,1mol最多消耗3mol NaOH
d.N不存在顺反异构体
(4)写出E与N按照物质的量之比为1:1发坐共聚生成P的化学反应方程式: , 高聚物P的亲水性比由E形成的聚合物(填“强”或“弱”).
(5)D的同系物K比D分子少一个碳原子,K有多种同分异构体,符合下列条件的K的同分异构体有种,写出其中核磁共振氢谱为1:2:2:2:3的一种同分异构体的结构简式: . a.苯环上有两种等效氢
b.能与氢氧化钠溶液反应
c.一定条件下1mol该有机物与足量金属钠充分反应,生成1mol H2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度为2.00mol/L的盐酸溶液1L,欲使其浓度变为4.00mol/L,下列方法可行的是( )
A.蒸发掉0.5L水
B.标况下通入44.8L HCl气体
C.将溶液加热蒸发浓缩至0.5L
D.加入10mol/L盐酸0.6L,再将溶液稀释至2L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com