
【题目】铬是重要的战略物质之一,由于具有质硬,耐磨,耐高温,抗腐蚀性等特性,所以在工业上应用比较广泛,在冶金工业上主要用铬铁矿(Cr2O3 、FeO、SiO2 、Al2O3 等,其它杂质不参加反应)生产铬和铁等金属。流程如下:
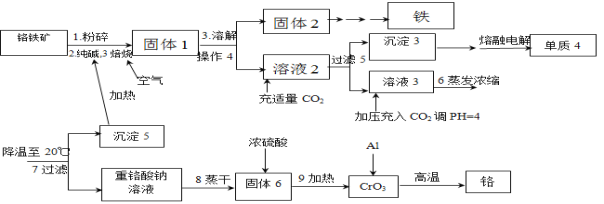
已知:2Cr2O3+3O2+4Na2CO3![]() 4Na2CrO4+4CO2;部分物质的溶解度(单位g)
4Na2CrO4+4CO2;部分物质的溶解度(单位g)
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | |
Na2CO3 | 7.0 | 13 | 29 | 40 | 49 | 46 | 44 |
NaHCO3 | 6.9 | 8.5 | 9.6 | 11.1 | 12.7 | 14.4 | 16.9 |
Na2Cr2O7 | 161 | 170 | 183 | 198 | 218 | 240 | 265 |
(1)粉碎的目的
(2)写出焙烧时含铝物质发生的化学反应方程式_______________________________;
(3)操作4是_______________________,沉淀3含有的物质有_____________________;
(4)写出生成沉淀5的离子方程式_____________________________________________;
(5)整个流程可以循环使用的物质有___________________________;
(6)最后一步制备金属铬的化学方程式______________________________。
【答案】增大接触面积,加快反应速率Al2O3+Na2CO3![]() 4NaAlO2+CO2↑过滤Al(OH)3 、H2SiO32Na++2CrO42―+2CO2+H2O=Cr2O72―+2NaHCO3↓Na2CO3、CO2、Al)或NaHCO3、AlCrO3+2Al
4NaAlO2+CO2↑过滤Al(OH)3 、H2SiO32Na++2CrO42―+2CO2+H2O=Cr2O72―+2NaHCO3↓Na2CO3、CO2、Al)或NaHCO3、AlCrO3+2Al![]() Cr+2Al2O3
Cr+2Al2O3
【解析】
(1)铬铁矿粉碎的目的:增大接触面积,加快反应速率;正确答案:增大接触面积,加快反应速率。
(2)铬铁矿中的氧化铝与碳酸钠焙烧时发生反应生成偏铝酸钠和二氧化碳,化学反应方程式:Al2O3+Na2CO3![]() 4NaAlO2+CO2↑;正确答案:Al2O3+Na2CO3
4NaAlO2+CO2↑;正确答案:Al2O3+Na2CO3![]() 4NaAlO2+CO2↑。
4NaAlO2+CO2↑。
(3)从流程看出该操作过程是把固体和液体分开,操作4是过滤;溶液2中含有硅酸钠、偏铝酸钠,铬酸钠,通入适量的二氧化碳后,生成H2SiO3、Al(OH)3 两种沉淀,所以沉淀3含有的物质有H2SiO3、Al(OH)3;正确答案:过滤,H2SiO3、Al(OH)3。
(4)溶液3为铬酸钠溶液,通入二氧化碳并调pH=4后,生成碳酸氢钠固体和重铬酸钠,离子方程式:2Na++2CrO42―+2CO2+H2O=Cr2O72―+2NaHCO3↓ ;正确答案: 2Na++2CrO42―+2CO2+H2O=Cr2O72―+2NaHCO3↓。
(5)从流程图看出,整个流程可以循环使用的物质有Na2CO3、CO2、Al或NaHCO3、Al;正确答案:Na2CO3、CO2、Al或NaHCO3、Al。
(6)氧化铬在高温下被金属铝还原为铬,化学方程式:CrO3+2Al![]() Cr+2Al2O3;正确答案:CrO3+2Al
Cr+2Al2O3;正确答案:CrO3+2Al![]() Cr+2Al2O3。
Cr+2Al2O3。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】从植物中分离出的活性化合物zeylastral的结构简式如图所示,下列说法错误的是( )
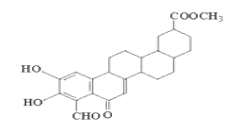
A. 1mol zeylastral最多与5molH2发生反应
B. 能与FeCl3溶液、银氨溶液发生反应
C. 化合物 zeylastral可以发生水解反应
D. 1mol zeylastral可与2molBr2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:

(1)该浓盐酸的物质的量浓度为_______________mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.1 mol/L稀盐酸。
①该学生需要量取_____________ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填 “偏高”或“偏低”或“无影响”)。
a、用量筒量取浓盐酸时俯视观察凹液面。(____________)
b、用量筒量取浓盐酸后,洗涤量筒2-3次,洗涤液也转移到容量瓶。(_________)
(4)现将100mL 0.5mol/L的盐酸与200mL 0.1mol/LCuCl2溶液混合,体积变化忽略不计,所得溶液中Cl-的物质的量浓度是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液可能含有Na+、NH4+、Fe2+、CO32、SO42、Cl中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是( )

A. 向原溶液中加K3Fe(CN)6溶液,无明显现象
B. 原溶液中c(Cl-)≥0.1mol˙L-1
C. 用洁净的铂丝蘸取原溶液,在酒精灯上灼烧,火焰呈黄色
D. 将湿润的红色石蕊试纸靠近实验产生的气体,试纸变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知CaO+SO2 = CaSO3 ,2CaSO3 + O2 = 2CaSO4 。为了真正减轻煤燃烧产生的污染,你认为下列措施可取的是( )
A.尽量用大块状的燃煤B.通入过量的空气
C.煤粉中掺进适量的生石灰D.高烟囱降低污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在实验室进行了一次有趣的反应过程:物质A经一系列的反应又回到了A。请回答下列问题。
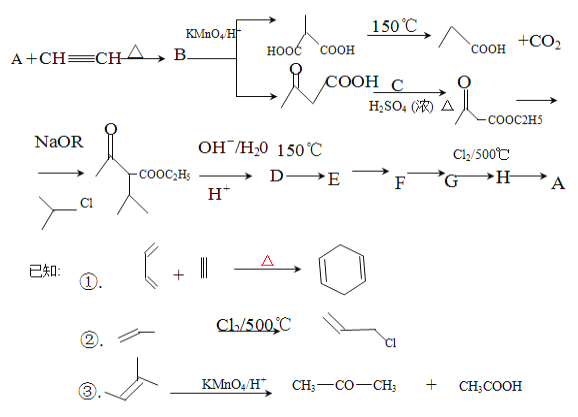
(1)下列说法正确的是_______。
A.A存在顺反异构 B.B能够发生加聚反应 C.C是乙酸 D.D的分子式C7H10O3
(2)A的结构简式_____________________________。
(3)上述循环流程中有机物的所有含氧官能团除羧基、酯基外还有____________________。
(4)C参与的这步反应的反应类型_____________________。
(5)E的同分异构体中能发生银镜反应的有______________种。
(6)写出D生成E的化学反应方程式 ________________________________。
(7)参考题中流程写出F到A的流程图(写出F、G、H、A的结构,注明反应条件)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去括号内的杂质,所选用的试剂或方法不正确的是
A. Na2CO3溶液(NaHCO3),选用适量的NaOH溶液
B. NaHCO3溶液(Na2CO3),应通入过量的CO2气体
C. Na2O2粉末(Na2O),将混合物在氧气中加热
D. Na2CO3溶液(Na2SO4),加入适量Ba(OH)2溶液,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,C、D、E、F、X、Y都是惰性电极,A、B为电源。将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色.
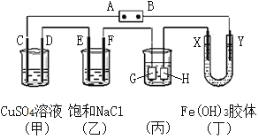
(1)若用CO、氧气燃料电池作电源,电解质为KOH溶液,则A为____极,A电极上的反应为__________________,B电极上的反应式为:__________________________________。
(2)若甲中装有100ml 1 molL-1的硫酸铜溶液,工作一段时间后,停止通电此时C、D两极上产生的气体体积相同.甲中D极产生的气体在标准状况下的体积为_____________L,欲使溶液恢复到起始状态,可向溶液中加入____。
A.CuO B.Cu2(OH)2CO3 C.Cu(OH)2 D.CuCO3
(3)通电后乙中反应的化学方程式:__________________________________。
(4)欲用(丙)装置给铜镀银,反应一段时间后(用CO、氧气燃料电池作电源)铜制品质量增加43.2克,理论上消耗氧气的质量_______克。
(5)工作一段时间后,丁中X极附件的颜色逐渐变浅,Y极附件的颜色逐渐变深,这说明__________________在电场作用下向Y极移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.鉴别氢氧化铝胶体(无色)和食盐水,可以不用任何试剂
B.鉴别白糖水和食盐溶液,可以不用任何试剂
C.鉴别粉笔末与水、豆油与水组成的浊液,可以不用任何试剂
D.鉴别氯化钠溶液与硫酸铜两种溶液,可以不用任何试剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com