
【题目】奥美拉唑主要用于十二指肠溃疡和胃溃的治疗,静脉注射可用于消化性溃疡急性出血的治疗,反应中间体F和奥美拉唑的合成路线如图:
I>中间体F的合成:
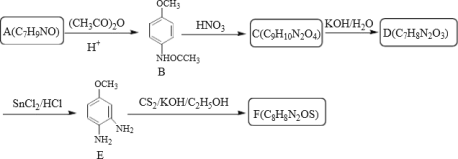
II.奧美拉唑的合成:
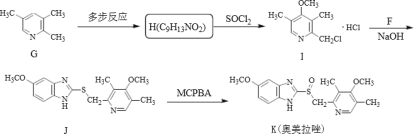
已知:R-OH![]() R-Cl
R-Cl
R1-SH+R2-X![]() R1-S-R2
R1-S-R2
结合上述合成路线,请回答:
(1)下列说法正确的是_____。
A.奥美拉唑的分子式为C18H19N3O3S
B.J生成K的反应类型为加成反应
C.化合物C可以发生的反应类型有取代、还原、加成
D.设计A转化为B的目的是保护其中的官能团
(2)化合物F的结构简式为_____;
(3)请写出A→B的反应方程式_____;
(4)试写出同时满足下列条件的化合物H的同分异构体:_____。
①分子中含苯环,遇FeC13显紫色
②分子中含有4种不同化学环境的氢原子。
(5)利用已有知识和题中涉及的反应,设计从乙烯合成![]() 的路线_____。(用流程图表示,无机试剂任选)
的路线_____。(用流程图表示,无机试剂任选)
【答案】C、D ![]()

 、
、 、
、 、
、
![]()
【解析】
根据A到B反应和B的结构简式得到A结构简式为![]() ,B到C发生硝化反应得到C为
,B到C发生硝化反应得到C为![]() ,C到D发生水解反应得到D为
,C到D发生水解反应得到D为![]() ,D反应生成
,D反应生成![]() ,根据信息2和I和F反应生成J,推出化合物F的结构简式为
,根据信息2和I和F反应生成J,推出化合物F的结构简式为![]() 。
。
⑴A. 根据奥美拉唑的结构简式得出分子式为C18H18N3O3S,故A错误;B. 加氧去氢是氧化反应,因此J生成K的反应类型为氧化反应,故B错误;C. 化合物C(![]() )含有苯环与氢气发生加成反应,也叫还原反应,有肽键能够发生水解反应,也叫取代反应,故C正确;D. 设计A转化为B的目的在硝化反应时保护—NH2,故D正确;综上所述,答案为CD。
)含有苯环与氢气发生加成反应,也叫还原反应,有肽键能够发生水解反应,也叫取代反应,故C正确;D. 设计A转化为B的目的在硝化反应时保护—NH2,故D正确;综上所述,答案为CD。
⑵根据信息2和I和F反应生成J,推出化合物F的结构简式为![]() ;故答案为:
;故答案为:![]() 。
。
⑶A→B的反应方程式 ;故答案为:
;故答案为: 。
。
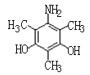
⑷①分子中含苯环,遇FeC13显紫色,说明含酚羟基;②分子中含有4种不同化学环境的氢原子;满足下列条件的化合物H的同分异构体: 、
、 、
、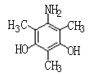 、
、 ;故答案为:
;故答案为: 、
、 、
、 、
、 。
。
⑸乙烯与溴的四氯化碳溶液发生加成反应得到![]() ,
,![]() 和氨气反应生成
和氨气反应生成![]() ,
,![]() 在CS2/KOH/C2H5OH作用下反应生成
在CS2/KOH/C2H5OH作用下反应生成![]() ,合成路线为
,合成路线为
![]() ;故答案为:
;故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下面是以环戊烷为原料制备环戊二烯的合成路线:
![]()
(1)X的名称为__,Y的结构简式为__,反应②的反应试剂和反应条件为__。
(2)金刚烷是一种重要的化工原料,工业上可通过下列途径制备:

环戊二烯分子的分子式为__;
二聚环戊二烯的同分异构体中,属于芳香烃且苯环上的一氯代物有3种的同分异构体的结构简式为__,__。
金刚烷的一氯代物有__种;金刚烷与四氢二聚环戊二烯的关系是___。(填字母)
a.互为同系物 b.互为同分异构体 c.均为烷烃 d.均为环烃
(3)写出环戊二烯在一定条件下生成高聚物的结构简式:__。
(4)烯烃也能发生如下反应:![]() R1CHO+
R1CHO+![]() +HCHO。
+HCHO。
请写出下列反应的有机产物的结构简式:![]() __。
__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述中,不正确的是( )
A. 淀粉![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
B. 纤维素![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
C. 油脂![]() 甘油和高级脂肪酸
甘油和高级脂肪酸![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
D. 蛋白质![]() 氨基酸
氨基酸![]() 人体所需的蛋白质(人体生长发育)
人体所需的蛋白质(人体生长发育)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. NO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构
B. P4和CH4都是正四面体形分子且键角都为109°28′
C. NH4+的电子式为 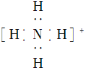 ,离子呈平面正方形结构
,离子呈平面正方形结构
D. NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法正确的是
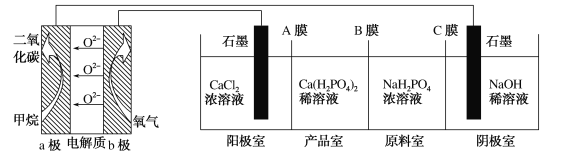
A.a极反应:CH4+8e-+4O2-=CO2+2H2O
B.A膜和C膜均为阴离子交换膜
C.可用铁电极替换阴极的石墨电极
D.a极上通入2.24 L甲烷,阳极室Ca2+减少0.4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸氨溴索(H)对于治疗老年重症肺炎有良好的疗效,其合成路线如下(部分反应条件及产物已略):
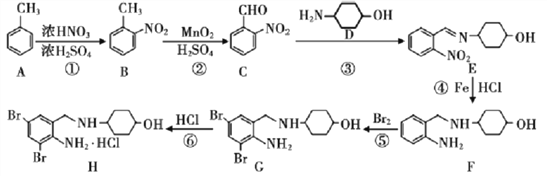
(1)B的名称为_________;反应①-⑥中为取代反应的是___________(填序号)。
(2)B的芳香族同分异构体J满足下列条件:
①可水解 ②可发生银镜反应 ③1mol J最多消耗2mol NaOH
J有________种;B的另一种芳香族同分异构体可与NaHCO3溶液反应,并有气体生成,其核磁共振氢谱有4组吸收峰,则它的结构简式为____________。
(3)可用碱性新制氢氧化铜悬浊液检验C中的特征官能团,写出该检验的离子反应方程式:____________________________。
(4)关于E的说法正确的是_________。
A.E难溶于水 B.E可使酸性KMnO4溶液褪色
C.1molE最多与1molH2加成 D.E不能与金属钠反应
(5)邻氨基苯甲酸甲酯(L)具有塔花的甜香味,也是合成糖精的中间体,以甲苯和甲醇为原料,无机试剂自选,参照H的合成路线图,设计L的合成路线____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂被誉为“高能金属”,是锂离子电池的电极材料。工业上常用β锂辉矿(主要成分为Li2O·Al2O3·4SiO2以及少量钙、镁杂质)和氟磷灰石(Ca5P3FO12)为原料制取锂离子电池正极材料LiFePO4,工艺流程如图:
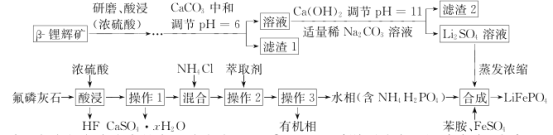
已知:①残留在溶液中的离子浓度小于10-5 mol·L-1 说明该离子沉淀完全;
②常温下,Ksp[Al(OH)3]=2.7×10-34、Ksp[Mg(OH)2]= 1.2×10-1 ;
③LiFePO4难溶于水。
回答下列问题:
(1)氟磷灰石(Ca5P3FO12 )中磷元素的化合价为______ , 滤渣2的主要成分是______(写化学式)。
(2)操作I所需的玻璃仪器名称有烧杯____________,操作 3的名称是_____________。
(3)蒸发浓缩Li2SO4溶液的目的是_____________________。
(4)写出合成反应的离子方程式:____________________________________。
(5)一种锂离子电池的反应原理为LiFePO4![]() Li+FePO4。写出放电时正极电极反应式:_____________________________。
Li+FePO4。写出放电时正极电极反应式:_____________________________。
(6)若某企业制备110.6 t纯净的LiFePO4,需要300t含氧化锂5%的β锂辉矿石,则锂元素的利用率为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A;其结构如下:

为了研究X的结构,将化合物A在一定条件下水解只得到 和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应 B.加成反应
C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式______________________________。
(3)C可通过下图所示途径合成,并制取冬青油和阿司匹林。

(ⅰ)写出有机物的结构简式:D:______________,C:________________,E:______________。
(ⅱ)写出变化过程中①、⑥的化学方程式(注明反应条件)
反应①__________________________________;反应⑥_____________________________。
(ⅲ)变化过程中的②属于____________反应,⑦属于________反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com