
��ͭ�����Ҫ�ɷ�X����Cu��Fe��S����Ԫ����ɵĸ��Σ�����Cu��Fe����Ԫ�ص�������Ϊ8:7����m g X��ĩȫ������200 mL��ŨHNO3����Ӧ�����Һ��ˮϡ����2��12 Lʱ�����pHΪ0����ϡ�ͺ����Һ��Ϊ���ȷݣ�������һ����Һ�еμ�6��05 mol/L��NaOH��Һ������һ����Һ�еμ�0��600 mol/L Ba(NO3)2��Һ������Һ�о����ɳ������ҳ�����������������Һ������仯����ͼ��ʾ��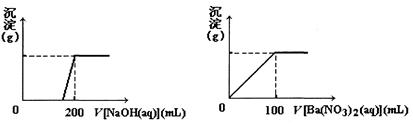
��1����ͨ������ȷ��m��ֵ��
��2��X��Ħ������Ϊ368 g/mol����ȷ��X�Ļ�ѧʽ��
��1���⣺�����⣬m g X�У�n(Cu):n(Fe)��1:1
2n(Cu2��)��3n(Fe3��)��6��05mol/L��0��2 L��2-1 mol/L��2��12 L
�ʣ�n(Cu)��n(Fe)��0��06 mol ��2�֣�
�֣�n(S)��0��6 mol/L��0��1 L��2��0��12 mol
��ˣ�mg��m(Cu)��m(Fe)��m(S)��0��06 mol��64 g/mol��0��06 mol��56 g/mol��0��12 mol��32 g/mol�� 11��04 g
��m��ֵΪ11��04��2�֣�
��2���⣺��X�Ļ�ѧʽΪ(CuFeS2)n����(64��56��32��2)��n��368 n��2����X�Ļ�ѧʽΪCu2Fe2S4��2�֣�
���������������1�������⣬Cu��Fe����Ԫ�ص�������Ϊ8��7����m g X�У�n��Cu����n��Fe��=8/64��7/56=1��1������ˮϡ���� 2��12 Lʱ�����pHΪ0������������Ũ��Ϊ1mol/L������ͼʾ���ݣ������������к������ӣ�Ȼ��������ת��Ϊ����������2n��Cu2+��+3n��Fe3+��=6��05mol?L-1��0��2L��2-1mol?L-1��2��12L��
�ʣ�n��Cu��=n��Fe��=0��06mol��n��S��=0��600mol?L-1��0��1L��2=0��12mol��
���mg=m��Cu��+m��Fe��+m��S��=0��06mol��64g?mol-1+0��06mol��56g?mol-1+0��12mol��32g?mol-1=11��04g����m��ֵΪ11��04��
��2���⣺��X�Ļ�ѧʽΪ��CuFeS2��n����64+56+32��2����n=368����ã�n=2����X�Ļ�ѧʽΪCu2Fe2S4��
���㣺���ͼ��֪ʶ����ѧ��ȷ�����ӻ�ѧʽ�ļ��㷽����


 ���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
Ԫ�����ڱ���ѧϰ���о���ѧ����Ҫ���ߡ���Ҫ��ش��������⣺
A��B��C��D��E�Ƕ�����Ԫ�أ���ԭ��������������A��C��Ԫ�ص������ֻ��һ�����ӣ�C���ӵĵ��Ӳ�ṹ�����ڱ��зǽ�������ǿ��Ԫ�ص������ӵĵ��Ӳ�ṹ��ͬ��Ԫ��A���Ժ�B�γ�A2B��A2B2���ַ��ӣ���������ҵ�ÿ�������о�����5��ԭ�ӣ�������Ԫ��D��A��ɣ�����ӵĺ����������Ϊ18��������Ԫ��D��E��ɣ������������C��E��ɵġ�
��1��Ԫ��B��D��E��Ԫ�ط�������Ϊ_______��_______��______��
��2������5��Ԫ���γɵķ����У��������⣬�����������ҲΪ18����___(�����ʽ)
��3��D���������ڸ����¿�����C��̼���η�����Ӧ���仯ѧ��Ӧ����ʽΪ________������������ˮ���ҷ�Ӧ�а������ɣ��䷴Ӧ�Ļ�ѧ����ʽΪ___________��
��4����500mL����ƿ����400mL 1mol/L�ı���Һ����Ҫ��������Ϊ________�����ƹ����г��õ�����ƿ�⣬����Ҫ�IJ���������___________________����������Ƶ�400mL��Һ������·��ͨ��1mol����ʱ�������Ͽ��ռ����������ڱ�״���µ����Ϊ_________L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�����ձ��м�����ͬ�����1��5mol/L��ϡ���ᣬ������ƽ�������������ϣ�������ƽ��ʹ֮�ﵽƽ�⣬��һ���ձ��м���5��4gþ����һ���ձ��м���5��4g�����Ը��ݼ�����з�����������ȡ��ͬ���ʱ����Ӧ��Ϻ���ƽ���ܻᷢ���ı仯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��֪NaCl��s��+H2SO4��Ũ�� NaHSO4 + HCl��������117g NaCl�����������Ũ������ȫ��Ӧ����
NaHSO4 + HCl��������117g NaCl�����������Ũ������ȫ��Ӧ����
��1��������HCl�ڱ��ʱ�����Ϊ���٣�
��2��������HCl��������ˮ�У����500mL������Һ������������ʵ���Ũ��Ϊ���٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��7�֣����ⶨij��������Ҫ�ɷ�������������������̼������ɣ�����������ʵ�飺��ȡ��ĩ״��Ʒ8.50�ˣ�����ijŨ�ȵ�����100 mL ����ַ�Ӧ���ռ�����״��������2.24 L ��Ȼ��������Ʒ�м���ͬŨ�ȵ�����100mL ����ַ�Ӧ�����ռ�����״��������1.12 L ��
����д�����������̣�
��1����ȡ��������ʵ���Ũ�ȡ���2����������Ʒ��̼����������������3λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��һ����汻�����������ƵĽ����ƣ�������10.8g������Ͷ�뵽100gˮ����ȫ��Ӧ���ռ���0.2g�������õ��ܶ�Ϊ1.106g��cm3����Һ���Լ���(Ҫ��д����)��
��1��10.8g�����У������Ƶ������Ƕ��ٿ�?
��2����Ӧ��������Һ�����ʵ����ʵ���Ũ��Ϊ���٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��֪һ������������������ȼ�գ����û������100 mL 3.00 mol/L��NaOH��Һ���ܶ�Ϊ1.12 g/mL��ǡ����ȫ���գ������Һ�к���NaClO�����ʵ���Ϊ0.0500 mol��
��1��ԭNaOH��Һ����������Ϊ_______
��2��������Һ��Cl�������ʵ���Ϊ________mol
��3�����������Ͳμӷ�Ӧ�����������ʵ���֮��n(Cl2)��n(H2)��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��100 mLij�ִ���Ũ�ȵ� H2SO4��Һ��ȡ��25 mL������10 mL 0.5 mol��L-1 BaCl2��Һ��ǡ����ȫ��Ӧ����
�ٵõ� BaSO4�������ٿ� ?
�ڴ��� H2SO4��Һ�����ʵ����ʵ���Ũ���Ƕ��٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
ʵ����Ҫ��98%���ܶ�Ϊ1��84g��cm-3������������3��68mol/L��������Һ480mL��
��1����ȷ��ȡ98%������ mL��
��2��Ҫ����3��68mol/L��������Һ480mL�������õ����������ձ�������������Ͳ
��3��������3��68mol/L��������Һ��������������ȷ�����������д����������ʹ�����Ƶ�������ҺŨ��ƫ�͵��� ��
| A����ϡ�͵�������Һת��������ƿ��δϴ���ձ��Ͳ����� |
| B�����ձ��ڵ�ϡ����������ƿ��ת��ʱ�����������ʹ����ϡ���ὦ��ƿ�� |
| C���ý�ͷ�ι�������ƿ�м�ˮʱ��Һ���������ƿ�̶ȣ���ʱ�����õιܽ�ƿ��Һ��������ʹ��Һ��Һ����̶����� |
| D���ý�ͷ�ι�������ƿ�м�ˮʱ�����ӹ۲���Һ��Һ��������ƿ�̶����� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com