
【题目】Al2(SO4)3和MgSO4混和,加适量水溶解,再加入KOH溶液,析出的沉淀量(W)与KOH溶液体积(V)的关系如图,则Al2(SO4)3和MgSO4的物质的量之比是( )

A. 2:1 B. 1:2 C. 1:1 D. 1:3
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( ) 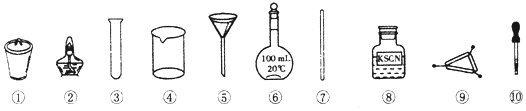
A.将茶叶灼烧灰化,选用②、④和⑨
B.用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④和⑦
C.过滤得到滤液,选用④、⑤和⑦
D.检验滤液中的Fe3+ , 选用③、⑧和⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是( )
A.AlCl3
B.Na2O
C.FeCl2
D.SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由FeO、Fe2O3和Fe3O4组成的混合物,测得其铁元素与氧元素的质量比为21∶8,
则混合物中FeO、Fe2O3和Fe3O4的物质的量之比可能是( )
A. 1∶2∶1 B. 2∶1∶1 C. 1∶1∶1 D. 2∶3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在2L恒容密闭容器中气态物质X、Y、Z的物质的量随时间变化的部分数据如表所示:
T/min | n(X)/mol | n(Y)/mol | n(Z)/mol |
0 | 0.80 | 1.00 | 0 |
1 | 0.70 | 0.80 | |
5 | 0.70 | ||
9 | 0.40 | ||
10 | 0.40 | 0.80 |
(1)写出该反应的化学方程式
(2)反应进行到10min,X的转化率为 , 0~5min内Y的平均反应速率为
(3)计算T℃时该反应的平衡常数K=
(4)T℃下向该密闭容器中通入一定量的X、Y、Z,反应到某时刻测得X、Y、Z的物质的量分别为1.00mol、0.50mol、1.60mol,则此时正逆反应速率大小:v正v逆(填“大于”、“等于”、“小于”)
(5)若在10min和t3、t5时刻分别改变该反应的某一反应条件,得到X、Z的物质的量及反应速率与时间的关系如图A、B所示: 
①10min时改变的反应条件是
②t3时刻改变的反应条件是t5时刻改变的反应条件是 , 理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制取冰晶石(Na3AlF6)的化学方程式如下:2Al(OH)3+12HF+3Na2CO3=2Na3AlF6+3CO2↑+9H2O
根据题意完成下列填空:
(1)在上述反应的反应物和生成物中,属于非极性分子的电子式 ,
属于弱酸的电离方程式
(2)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是(选填编号).
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸性
c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用下图所示的实验装置测定Na2O2试样的纯度。(可供选用的试剂只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
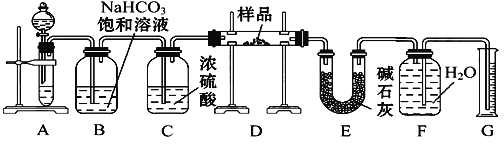
回答下列问题:
(1)装置A中液体试剂选用____ ;实验开始前盛装此药品的仪器名称是_____ ;B中饱和NaHCO3 溶液能否改为饱和Na2CO3 溶液 ______
(2)装置B的作用是________;装置C的作用是________;装置E中碱石灰的作用是___________。
(3)装置D中发生的主要反应的化学方程式是_________ 最后在F中收集到的气体是 _____
(4)若删去E装置,又会是什么后果:______(填偏高、偏低或无影响),
(5)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与氯元素同周期且金属性最强的元素位于周期表的第____周期___族。与该元素相邻的短周期主族元素原子半径从大到小的顺序是_____(用元素符号表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com