
【题目】现有一定量含有Na2O杂质的Na2O2试样,用下图所示的实验装置测定Na2O2试样的纯度。(可供选用的试剂只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
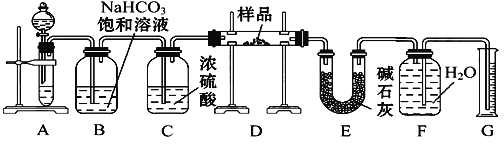
回答下列问题:
(1)装置A中液体试剂选用____ ;实验开始前盛装此药品的仪器名称是_____ ;B中饱和NaHCO3 溶液能否改为饱和Na2CO3 溶液 ______
(2)装置B的作用是________;装置C的作用是________;装置E中碱石灰的作用是___________。
(3)装置D中发生的主要反应的化学方程式是_________ 最后在F中收集到的气体是 _____
(4)若删去E装置,又会是什么后果:______(填偏高、偏低或无影响),
(5)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为____。
【答案】 6 mol·L-1盐酸 分液漏斗 不能 除去气体中的HCl 干燥CO2 吸收装置D中反应剩余的CO2 2Na2O2+2CO2==2Na2CO3+O2 ,Na2O+CO2 ==Na2CO3 O2 高 78%
【解析】试题分析:(1)装置A是碳酸钙和酸反应生成二氧化碳;B装置的作用是除去二氧化碳中的氯化氢,二氧化碳与碳酸钠溶液反应生成碳酸氢钠;(2)碳酸钙和盐酸反应生成的二氧化碳气体中含有氯化氢气体,可以用饱和碳酸氢钠来除去,浓硫酸具有吸水性,可以干燥二氧化碳气体,装置E中碱石灰的作用是吸收二氧化碳,防止对氧气的体积测量造成干扰;(3)氧化钠和过氧化钠都能和二氧化碳反应,反应后的气体有氧气和二氧化碳,二氧化碳被装置E中的碱石灰吸收;(4)若删去装置E,F中收集到的氧气体积偏大;(5)根据反应2Na2O2+2CO2=2Na2CO3+O2,反应结束后测得气体体积为224mL(标准状况),即生成的氧气的量0.01mol,过氧化钠的物质的量为0.02ml。
解析:(1)装置A是碳酸钙和酸反应生成二氧化碳,碳酸钙和硫酸反应时,生成的硫酸钙是微溶于水的,会覆盖在碳酸钙的表面,使反应不能持续,所以用盐酸而不用硫酸;根据装置图,实验开始前盛装盐酸的仪器是分液漏斗;B装置中碳酸氢钠的作用是除去二氧化碳中的氯化氢,二氧化碳能与碳酸钠反应,所以不能把B中饱和NaHCO3 溶液能否改为饱和Na2CO3 溶液;(2)碳酸钙和盐酸反应生成的二氧化碳气体中含有氯化氢气体,可以用饱和碳酸氢钠来除去,所以B的作用是除去二氧化碳气体中的HCl,浓硫酸具有吸水性,可以将二氧化碳干燥,所以装置C的作用是干燥CO2,装置E中碱石灰的作用是吸收装置D中反应剩余的CO2,防止对氧气的体积测量造成干扰;(3)氧化钠和过氧化钠都能和二氧化碳反应,反应方程式分别为2Na2O2+2CO2=2Na2CO3+O2、Na2O+CO2=Na2CO3;反应后的气体有氧气和二氧化碳,二氧化碳被装置E中的碱石灰吸收,所以装置F中收集到的气体是氧气;(4)若删去装置E,F中收集到的氧气体积偏大,计算出的Na2O2的质量偏大,试样的纯度偏高;(5)根据反应2Na2O2+2CO2=2Na2CO3+O2,反应结束后测得气体体积为224mL(标准状况),即生成的氧气的量0.01mol,过氧化钠的物质的量为0.02ml,过氧化钠的纯度=![]() =78%。
=78%。


 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S气体。
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华,氢硫酸为弱酸。他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:

①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封。
请回答下列问题:
(1)装置A中反应的化学方程式为_______________________________________。
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端。要使沉积的FeCl3进入收集器,第④步操作应该是__________________________________。
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)____________。
(4)装置B中冷水浴的作用为_______________________________________________;装置C的名称为________;装置D中FeCl2全部反应后,因失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂_______________________________________________。
(5)在虚线框中画出尾气吸收装置E并注明试剂。(在答题卡上画)____________
(6)FeCl3溶液与H2S气体反应的离子方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、MgSO4和少量Fe、Al的氧化物)为原料制备MgCO33H2O.实验过程如图1 
(1)酸溶需加热的目的是;过滤时用到的玻璃仪器有
(2)加入H2O2氧化时发生发应的离子方程式为 .
(3)用如图2所示的实验装置进行萃取和分液,以除去溶液中的Fe3+ . 
①实验装置图2中仪器A的名称为 .
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有溶液的仪器A中加入一定量的有机萃取剂,、静置、分液,并重复多次.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Al2(SO4)3和MgSO4混和,加适量水溶解,再加入KOH溶液,析出的沉淀量(W)与KOH溶液体积(V)的关系如图,则Al2(SO4)3和MgSO4的物质的量之比是( )

A. 2:1 B. 1:2 C. 1:1 D. 1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐田法是把海水引入盐田,利用日光、风力蒸发浓缩海水,使其达到饱和,进一步将食盐结晶出来,这种方法在化学上称为
A.蒸发结晶B.冷却结晶C.重结晶D.蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将pH=1的盐酸平均分成2份,1份加入适量水,另一份加入与该盐酸物质的量浓度相同的适量NaOH溶液后,pH都升高了1,则加入的水与NaOH溶液的体积比为( )
A.9:1
B.10:1
C.11:1
D.12:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将相同状况下的下列气体分别充满一干燥烧瓶中,把烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度大小关系为( )
①NH3;②NO2;③体积比4:1混合的NO2和O2;④NO(用导管向烧瓶中缓缓通入O2至气体恰好完全吸收)
A.①=②>③>④
B.①=②=③=④
C.①=②=④>③
D.①>③>②>④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识回答下列问题:
(1)A与NaOH溶液反应,有如下转化关系(若产物中有水生成则省略,未表示出来)。

①若A为常见金属单质,C为气体,写出向B溶液中通入过量CO2反应的离子方程式:_______________;
②若A为空气的成分之一,能造成温室效应,当向100mL1mol/LNaOH溶液中通入1.344L气体(标准状况下)充分反应后,生成B和C的物质的量之比为______(B的摩尔质量大于C);
③若A为AlCl3,写出A与NaOH按物质的量之比3:10混合时发生反应的离子方程式:______________。
(2)氯化铁溶液可用于腐蚀印刷铜电路板,请写出相关的离子方程式: ______________,如何检验溶液中的铁离子已经完全反应: ______________。
(3)现有AlCl3和FeCl3混合溶液,其中A13+和Fe3+的物质的量之和为0.1mol,向此溶液中加入80mL浓度为4mol/L的NaOH溶液,使其充分反应,设原混合溶液中A13+的物质的量与A13+和Fe3+的总物质的量的比值为x。当最终生成的沉淀中只有Fe(OH)3时,x的取值范围是______,请在图中画出沉淀总量(mol)随x(0→1.0)变化的曲线:______________

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com