
【题目】将相同状况下的下列气体分别充满一干燥烧瓶中,把烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度大小关系为( )
①NH3;②NO2;③体积比4:1混合的NO2和O2;④NO(用导管向烧瓶中缓缓通入O2至气体恰好完全吸收)
A.①=②>③>④
B.①=②=③=④
C.①=②=④>③
D.①>③>②>④
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案科目:高中化学 来源: 题型:
【题目】某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是( )
A.AlCl3
B.Na2O
C.FeCl2
D.SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用下图所示的实验装置测定Na2O2试样的纯度。(可供选用的试剂只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
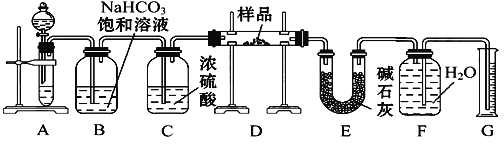
回答下列问题:
(1)装置A中液体试剂选用____ ;实验开始前盛装此药品的仪器名称是_____ ;B中饱和NaHCO3 溶液能否改为饱和Na2CO3 溶液 ______
(2)装置B的作用是________;装置C的作用是________;装置E中碱石灰的作用是___________。
(3)装置D中发生的主要反应的化学方程式是_________ 最后在F中收集到的气体是 _____
(4)若删去E装置,又会是什么后果:______(填偏高、偏低或无影响),
(5)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与氯元素同周期且金属性最强的元素位于周期表的第____周期___族。与该元素相邻的短周期主族元素原子半径从大到小的顺序是_____(用元素符号表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况,设计了如下图所示装置进行有关实验。
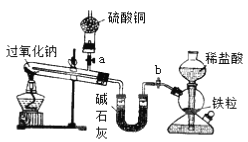
(1)此装置中,怎样检查除启普发生器之外的装置的气密性?_________________________________。
(2)请完成该实验的有关操作步骤。
①检查装置气密性;
②打开a、b产生氢气,观察试管内物质的颜色变化;
③____________________________________________________;
④加热过氧化钠,观察试管内物质的颜色变化;
⑤反应完全后,__________________________________________;
⑥拆卸装置。
(3)该装置中,碱石灰的作用是_________________________ 。
(4)实验过程中观察到(2)中步骤②无明显变化,步骤④Na2O2熔化后,黄色粉末立即变成白色,干燥管内硫酸铜未变成蓝色。则Na2O2与H2反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 
(1)从实验装置上看,图中尚缺少的一种玻璃用品是;
(2)用相同浓度和体积的醋酸代替稀盐酸溶液进行实验,求得的中和热数值(填“偏 大”、“偏小”或“无影响”);
(3)实验中改用60mL 0.50mol/L 盐酸跟50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等”或“不相等”),所求中和热(填“相等”或“不相等”),简述理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体.
已知:①CO(g)+NO2(g)═NO(g)+CO2(g)△H=﹣akJmol﹣1(a>0)
②2CO(g)+2NO(g)═N2(g)+2CO2(g)△H=﹣bkJmol﹣1(b>0)
若用标准状况下4.48L CO还原NO2至N2(CO完全反应),整个过程中转移电子的物质的量为 , 放出的热量为kJ(用含有a和b的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL HNO3和H2SO4的混合溶液中,两种酸的物质的量浓度之和为0.6mol/L.向该溶液中加入足量的铜粉,加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大值为(反应前后溶液体积变化忽略不计)( )
A.0.225mol/L
B.0.30mol/L
C.0.36mol/L
D.0.45mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com