
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸的物质的量浓度为______molL-1.
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______.
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400molL-1的稀盐酸.
①该学生需要量取______mL上述浓盐酸进行配制.
②所需的实验仪器有:胶头滴管、烧杯、量筒、玻璃棒,配制稀盐酸时,还缺少的仪器有_________________________.
(4)①假设该同学成功配制了0.400molL-1的盐酸,他又用该盐酸中和含0.4gNaOH的NaOH溶液,则该同学需取______mL盐酸.
②假设该同学用新配制的盐酸中和含0.4gNaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是___________.
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出.
【答案】 11.9 BD 16.8 500mL容量瓶 25 C
【解析】(1)依据c=1000ρω/M 计算浓盐酸的物质的量浓度;
(2)根据该物理量是否与溶液的体积有关判断;
(3)①依据溶液稀释过程中所含溶质的物质的量不变计算需要浓盐酸体积;
②根据配制过程中需要的仪器分析解答;
(4)①根据n(HCl)=n(NaOH)计算;
②盐酸体积减少,说明标准液盐酸体积读数减小,据此解答。
(1)浓盐酸的物质的量浓度c=1000×1.19×36.5%/36.5 mol/L=11.9mol/L;
(2)A.溶液中HCl的物质的量=cV,所以与溶液的体积有关,A不选;
B.溶液具有均一性,浓度与溶液的体积无关,B选;
C.溶液中Cl-的数目=nNA=cVNA,所以与溶液的体积有关,C不选;
D.溶液的密度与溶液的体积无关,D选;
答案选BD;
(3)①设需要浓盐酸体积V,则依据溶液稀释过程中所含溶质的物质的量不变得:V×11.9mol/L=0.400molL-1×0.5L,解得V=0.0168L=16.8mL;
②所需的实验仪器有:胶头滴管、烧杯、量筒、玻璃棒,由于是配制500mL溶液,则配制稀盐酸时,还缺少的仪器有500mL容量瓶;
(4)①n(HCl)=n(NaOH)=0.4g÷40g/mol=0.01mol,V(HCl)=0.01mol/0.400molL1=0.025L=25mL,即该同学需取25mL盐酸;
②消耗的标准液盐酸体积减少,说明读数时标准液的体积比实际体积减少了,则
A、浓盐酸挥发,浓度不足,配制的标准液浓度减小,滴定时消耗盐酸体积变大,A不选;
B、配制溶液时,未洗涤烧杯,标准液浓度减小,消耗体积增大,B不选;
C、配制溶液时,俯视容量瓶刻度线,配制的标准液浓度变大,滴定时消耗的体积减小,C选;
D、加水时超过刻度线,用胶头滴管吸出,标准液浓度减小,滴定时消耗标准液体积增大,D不选;
答案选C。


科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。一种合成阿魏酸的反应可表示为

下列说法正确的是
A. 可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
B. 香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应
C. 通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D. 与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电化学装置的说法正确的是

A. 利用图a装置处理银器表面的黑斑Ag2S,银器表面的反应为Ag2S+2e-=2Ag+S2-
B. 图b电解一段时间,铜电极溶解,石墨电极上有亮红色物质析出
C. 图c中的X极若为负极,则该装置可实现粗铜的精炼
D. 图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习和研究离不开元素周期表。表为元素周期表的一部分,表中①-⑩分别代表一种元素。回答下列问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
3 | ⑧ | ⑨ | ⑩ |
(1)上述元素中,有一种元素在自然界中形成的物质种类最多,该元素在周期表中的位置是______。
(2)⑧、⑨、⑩元素的离子半径由大到小的顺序为______(用离子符号表示)。
(3)写出由①、⑥、⑧三种元素形成的一种离子化合物的电子式___________。
(4)上述元素中有一种元素的氧化物和氢氧化物都有两性,画出该元素的原子结构示意图______;高温条件下,该元素的单质与铁红能发生反应,此反应常用于野外焊接钢轨,则该反应的能量变化可用图______表示。![]() 填“甲“或“乙”
填“甲“或“乙”![]()
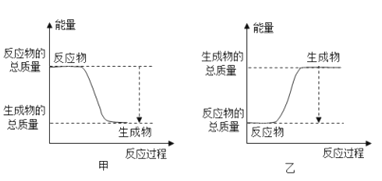
从①-⑩中任选元素,按下面要求写出一个置换反应:_____________________。要求:非金属单质1 + 化合物1→非金属单质2 + 化合物2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】节约资源、保护环境,共同守护我们赖以生存的地球是每个人的责任。下列做法值得提倡的是
A.大力开采化石燃料
B.交通出行优先使用私家车
C.超市购物使用一次性塑料袋
D.回收利用垃圾中的有用资源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化钠与过氧化钠的说法正确的是( )
A.它们属于碱性氧化物
B.它们都能与水反应产生氧气
C.它们都能与二氧化碳发生氧化还原反应
D.过氧化钠是潜水艇和呼吸面具的供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2mol X和2mol Y充入2L密闭容器中进行反应:X(g)+3Y(g) ![]() 2Z(g)+aQ(g)。2min末该反应达到平衡时生成0.8mol Z,测得Q的浓度为0.4mol·L-1,下列叙述错误的是( )
2Z(g)+aQ(g)。2min末该反应达到平衡时生成0.8mol Z,测得Q的浓度为0.4mol·L-1,下列叙述错误的是( )
A. a的值为2
B. 平衡时X的浓度为0.8mol·L-1
C. 平衡时Y的转化率60%
D. 0~2min内Y的反应速率为0.6mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素的部分性质数据如下:
元素 | T | X | Y | Z | W |
原子半径(mm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
最高或最低化合价 | +1 | +5,-3 | +7,-1 | +6,-2 | +3 |
(1)Z离子的结构示意图为_______________。
(2)关于Y、Z两种元素,下列叙述正确的是__________(填序号)。
a 简单离子的半径Y>Z
b 气态氢化物的稳定性Y比Z强
c 最高价氧化物对应水化物的酸性Z比Y强
(3)甲是由T、X两种元素形成的10e-分子,乙是由Y、W两种元素形成的化合物。某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是____________________________。一段时间后,观察到试管中的现象是_________________________,发生反应的离子方程式是___________________________。
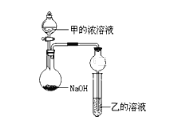
(4)XO2是导致光化学烟雾的“罪魁祸首”之一。它被氢氧化钠溶液吸收的化学方程式是: 2XO2+2NaOH=M+NaXO3+H2O (已配平),产物M中元素X的化合价为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 (1)如图所示,若溶液C为浓硝酸,电流表指针发生偏转,B电极材料为Fe,A电极材料为Cu,则B电极的电极反应式为_________,A电极的电极反应式为____________;反应进行一段时间后溶液C的酸性会____(填“增强”“减弱”或“基本不变”)。
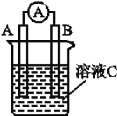
(2)我国首创以铝—空气—海水电池作为能源的新型海水标志灯,以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极材料是______(填化学名称),负极反应为___________;正极反应为_________。
(3)熔融盐电池具有高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,其负极反应式为2CO+2CO32---4e-![]() 4CO2,则正极反应式为_____,电池总反应式为______。
4CO2,则正极反应式为_____,电池总反应式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com